






【共识】食管癌加速康复外科技术应用专家共识2016






【共识】加速康复外科优化重型肝炎肝移植围手术期管理临床实践的专家共识2017

















【共识】加速康复外科围术期营养支持中国专家共识2019






【共识】加速康复妇科围手术期护理中国专家共识2019








【共识】腹腔镜肝切除术加速康复外科中国专家共识2017








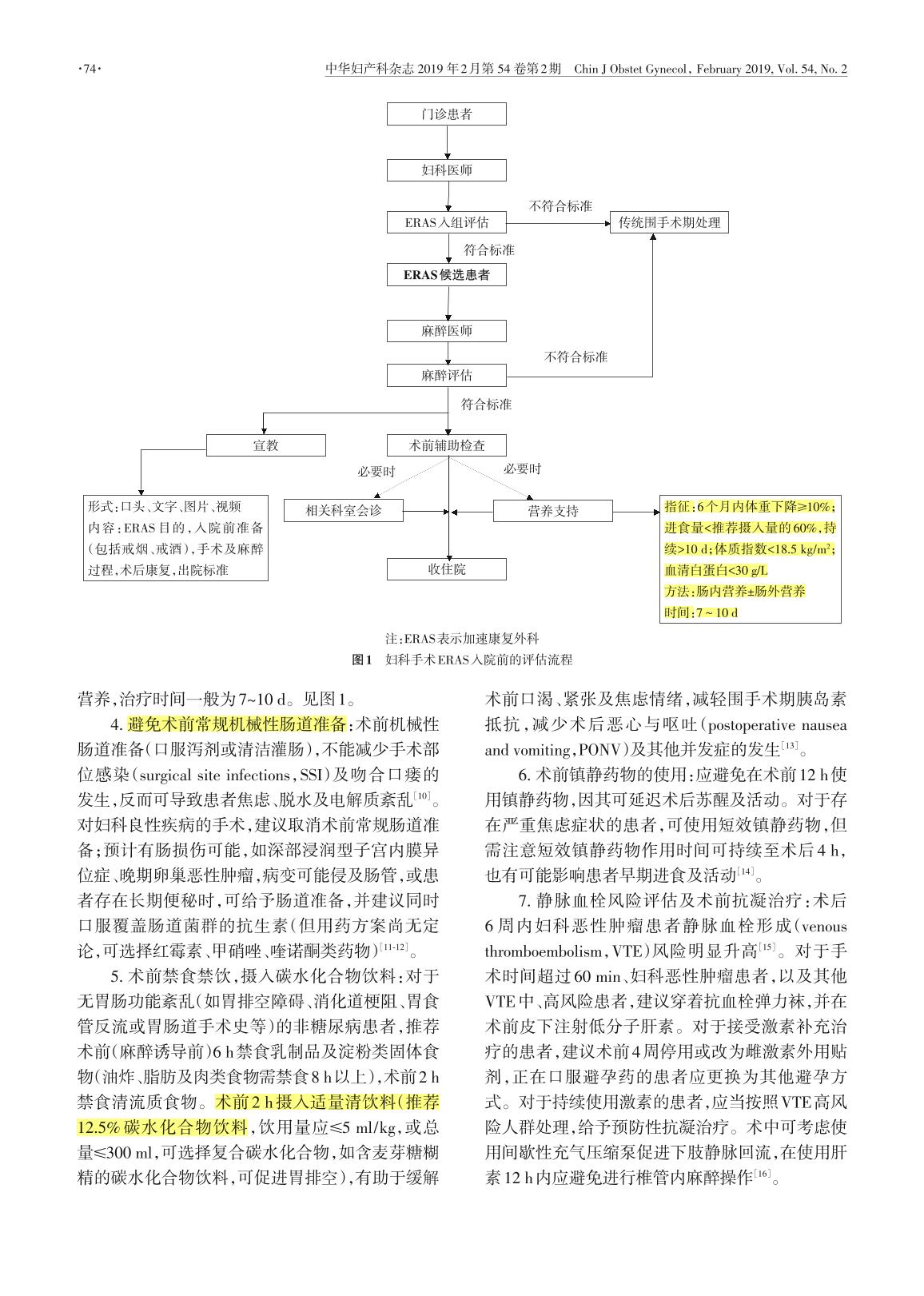
【共识】妇科手术加速康复的中国专家共识2019






【共识】胆道手术加速康复外科专家共识2016








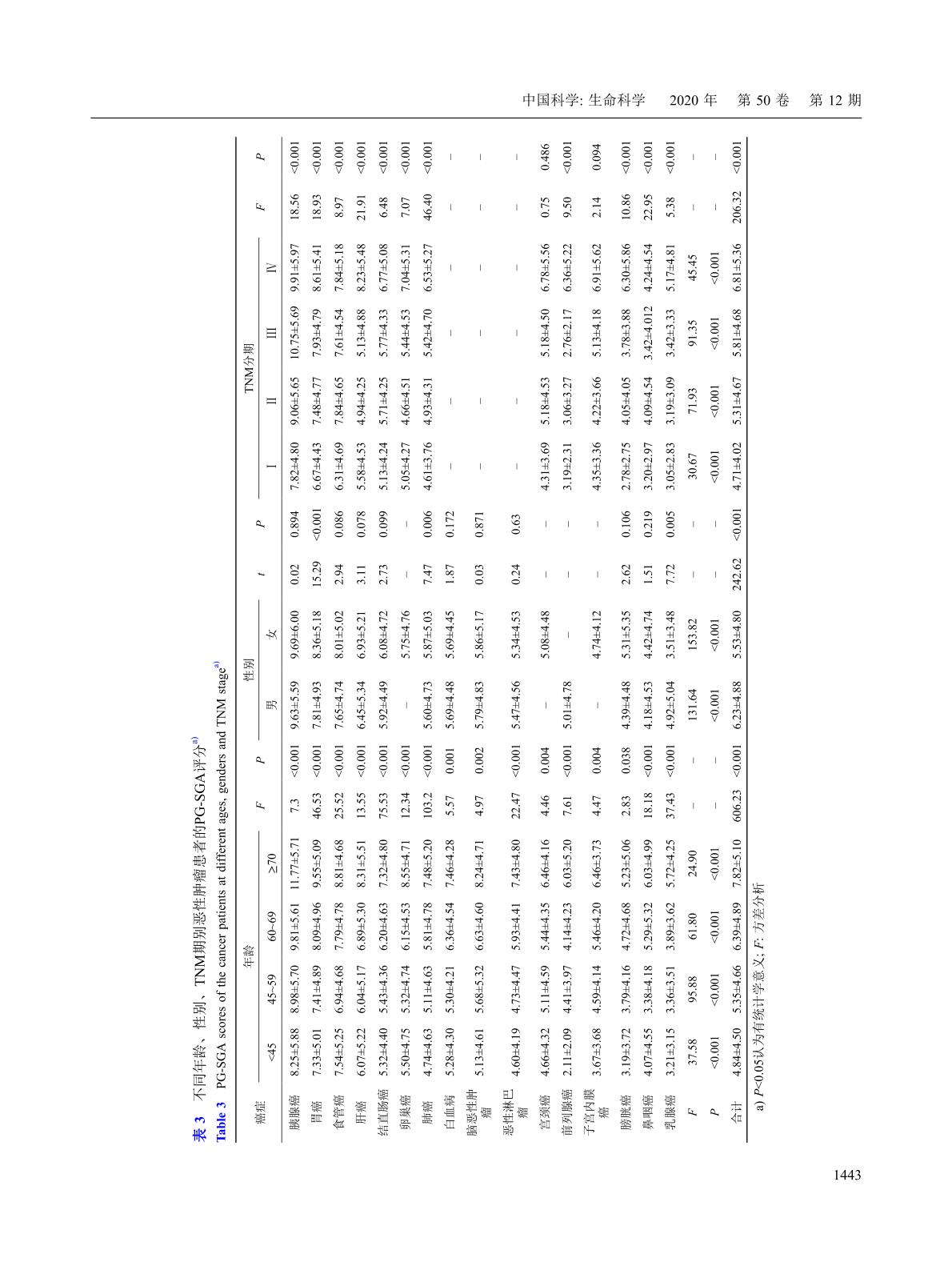
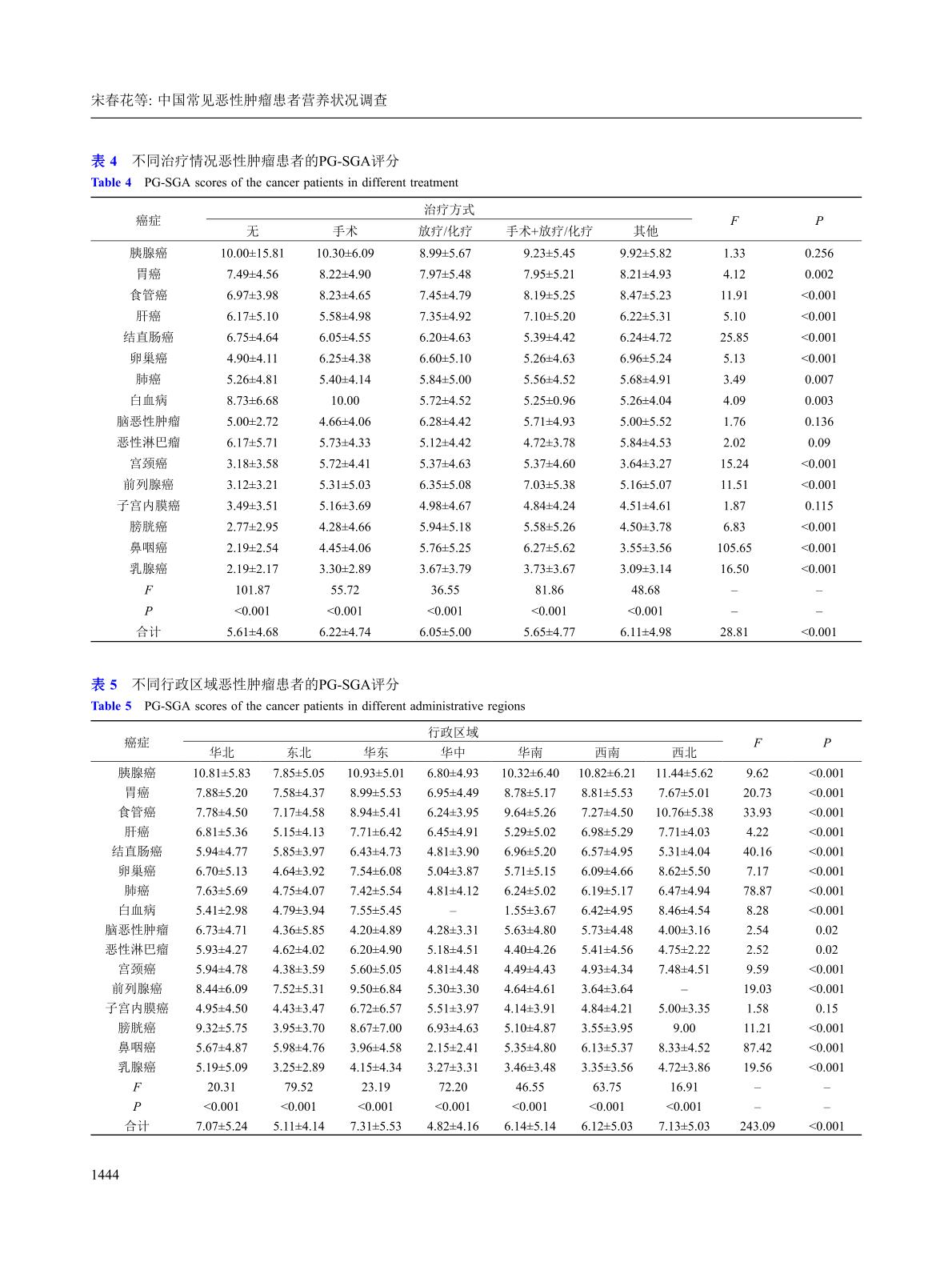
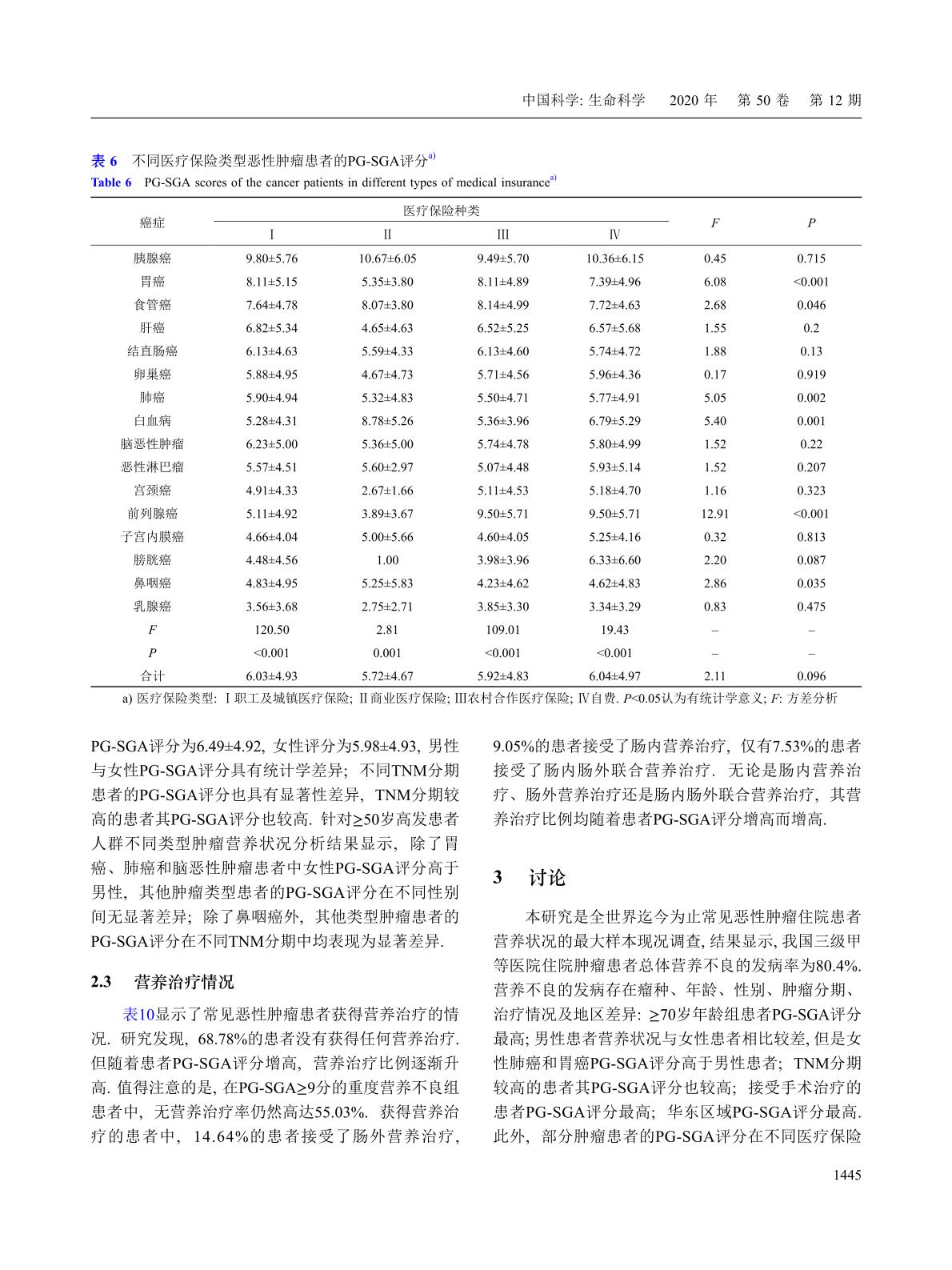
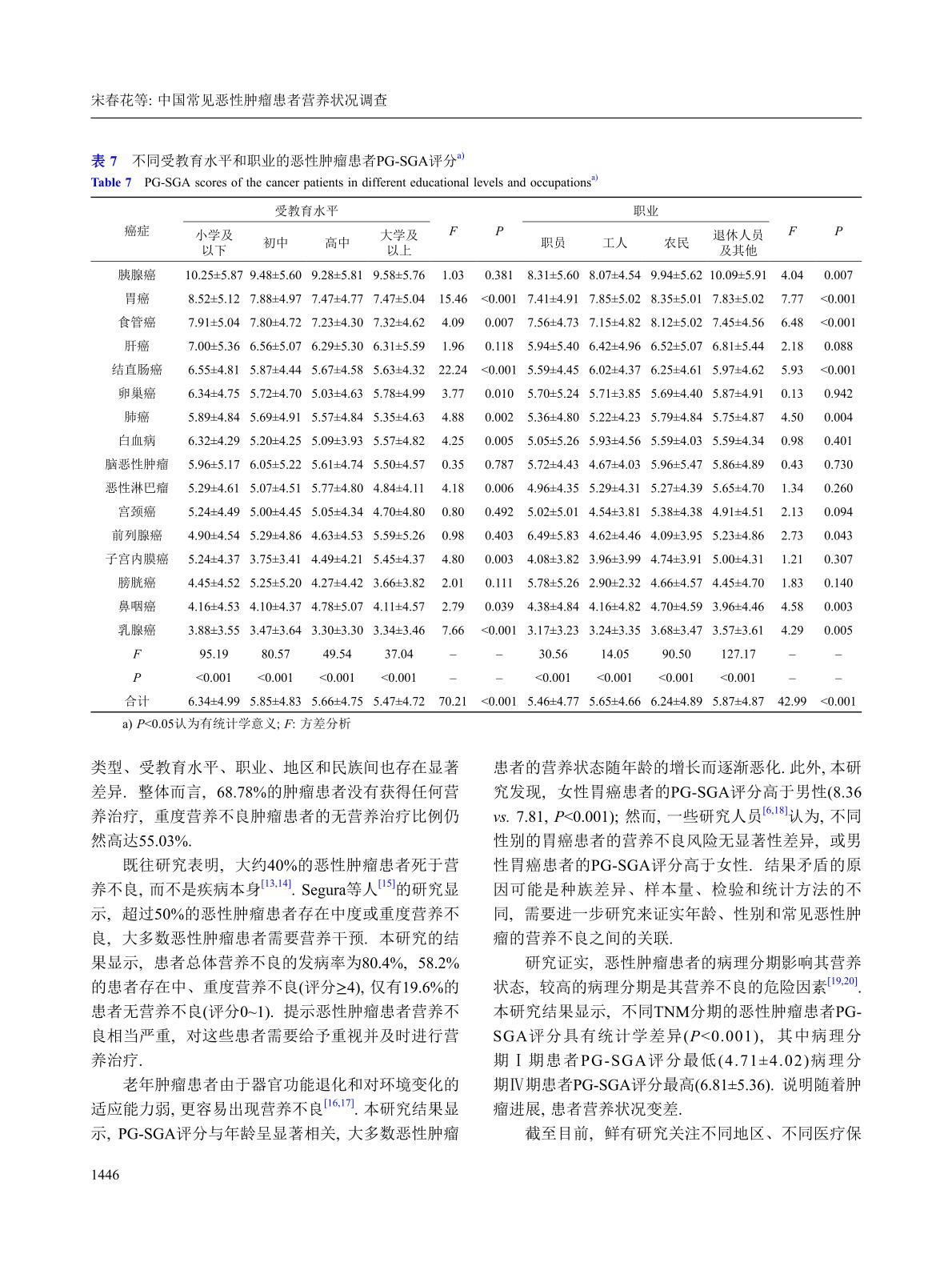
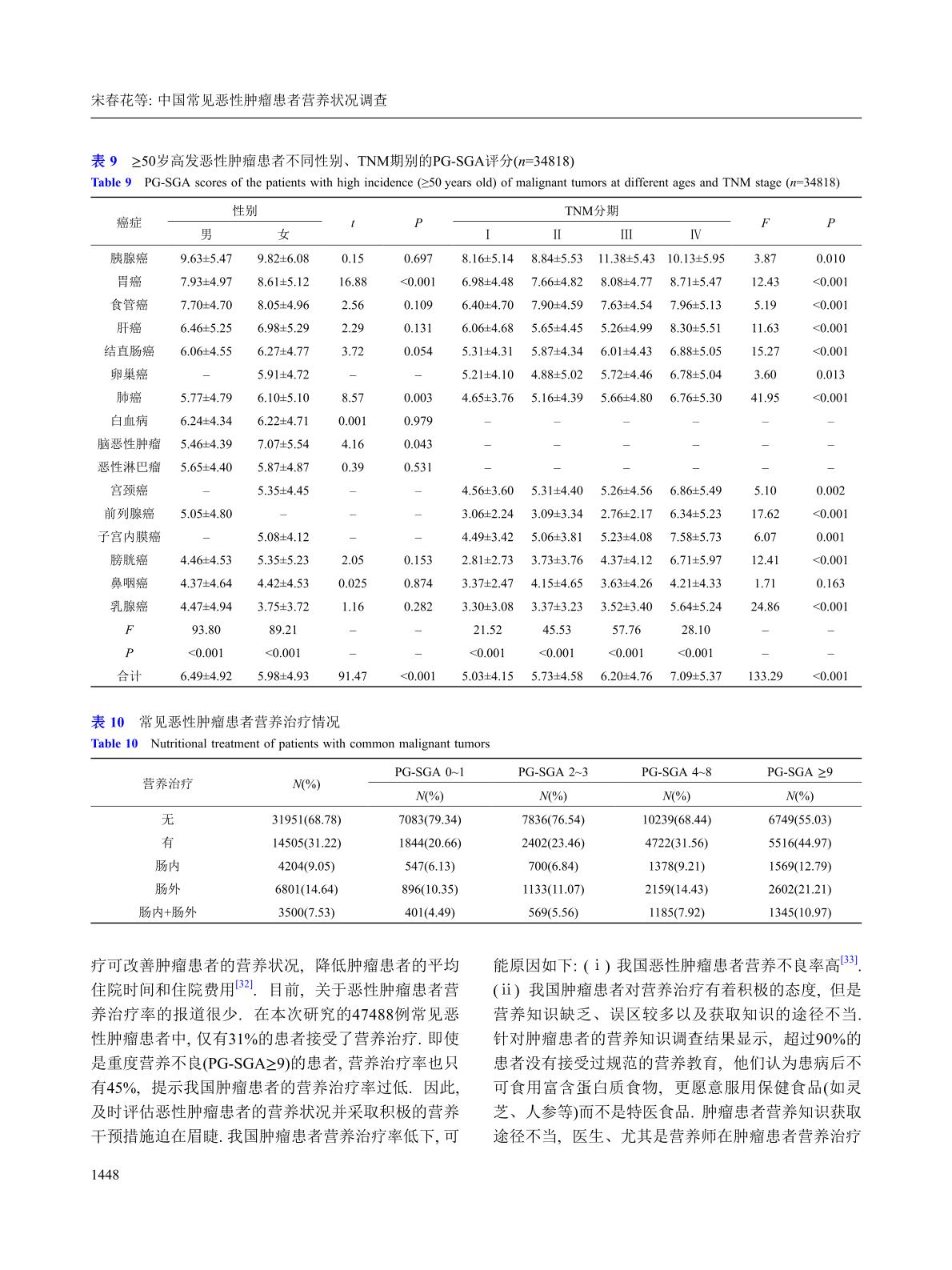
中国常见恶性肿瘤患者营养状况调查2020(共47488例16种常见恶性肿瘤住院患者)











【指南】肿瘤免疫营养治疗指南2016














