12月5日,君实生物发布公告,宣布其收到国家药品监督管理局核准签发的《受理通知书》,偌考奇拜单抗注射液(重组人源化抗IL-17A单克隆抗体注射液,产品代号:JS005)用于治疗适合系统治疗或光疗的中度至重度斑块状银屑病的成人患者的新药上市申请获得受理。

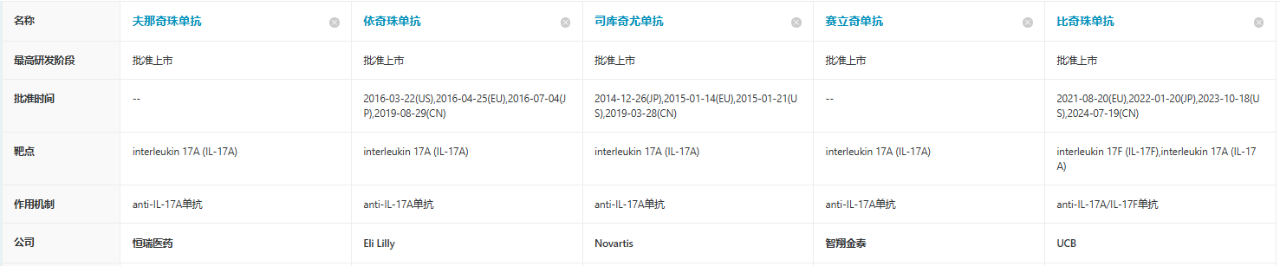
根据医药魔方数据库,此前已有5款靶向IL-17A的单抗在中国获批上市。
偌考奇拜单抗是公司自主研发的特异性抗IL-17A单克隆抗体。IL(白细胞 介素)-17A是一种具有多效性的细胞因子,其分泌失调与自身免疫性疾病如银 屑病、类风湿关节炎、强直性脊柱炎等疾病的发生发展密切相关。偌考奇拜单抗 通过与IL-17A高亲和力结合并选择性地阻断IL-17A与其受体IL-17RA/IL-17RC 的结合,从而阻断下游信号通路的激活和炎性因子的释放,能有效地缓解自身免疫性疾病的症状。
截至本公告披露日,除本次新药上市申请外,偌考奇拜单抗用于治疗活动性强直性脊柱炎的II期临床研究的所有参与者已完成治疗,进入安全随访期。
银屑病是一种免疫介导的常见慢性、复发性、炎症性、系统性疾病。根据中 国银屑病诊疗指南(2023版),在中国,银屑病的患病率在2008年已达0.47%,远高于1984年的0.12%。银屑病可以合并其他系统异常,中重度银屑病患者罹 患代谢综合征和动脉粥样硬化性心血管疾病的风险增加,抑郁、焦虑以及身体和精神痛苦导致的自杀倾向等精神疾病在银屑病患者中也较为常见。因此,银屑病是一种严重影响患者身心健康的疾病。
本次新药上市申请主要基于一项多中心、随机、双盲、平行、安慰剂对照的关键注册性III期临床研究(研究编号:JS005-005-III-PsO),该研究由北京大学人民医院张建中教授担任主要研究者,并在全国60家研究中心共同开展,共入组747例中重度斑块状银屑病患者。
研究结果显示,偌考奇拜单抗治疗12周显著改善了银屑病面积与严重程度指数(PASI)75/90/100 和静态医师全面评估(sPGA)评分0或1,疗效显著优 于安慰剂并在52周治疗期间维持稳定,且总体安全性良好。
目前已获批的IL-17A靶点药物较多,国内包括恒瑞医药的IL-17A单抗夫那奇珠单抗、智翔金泰的IL-17A 单抗赛立奇单抗;跨过药企在中国获批的药物包括诺华的司库奇尤单抗、礼来的依奇珠单抗、协和发酵麒麟的布罗利尤单抗、优时比的比吉利珠单抗等。
