医药反腐传来重磅消息,又有上市公司及实控人遭立案调查!
8月7日晚间消息,山东省纪委监委召开纪检监察机关配合开展全省医药领域腐败问题集中整治工作动员部署视频会议。会议指出,坚持严打开路,全面排查问题线索,注重突出查处重点,严厉打击行贿行为,精准把握政策策略,推动形成强力震慑。
同样是8月7日晚间,人福医药在上交所公告称,公司实际控制人艾路明收到证监会立案告知书,因涉嫌信息披露违法违规,证监会决定对其立案。人福医药是麻醉药龙头企业,公司市值一度超过500亿元。
值得注意的是,近期,人福医药、三特索道、*ST明诚接连公告上市公司主体或上市公司实控人,被证监会立案调查。三家公司原本全部列于武汉“当代系”旗下,曾经都是显赫一时的“当代系”旗下的上市平台,并且曾拥有共同的实际控制人艾路明。
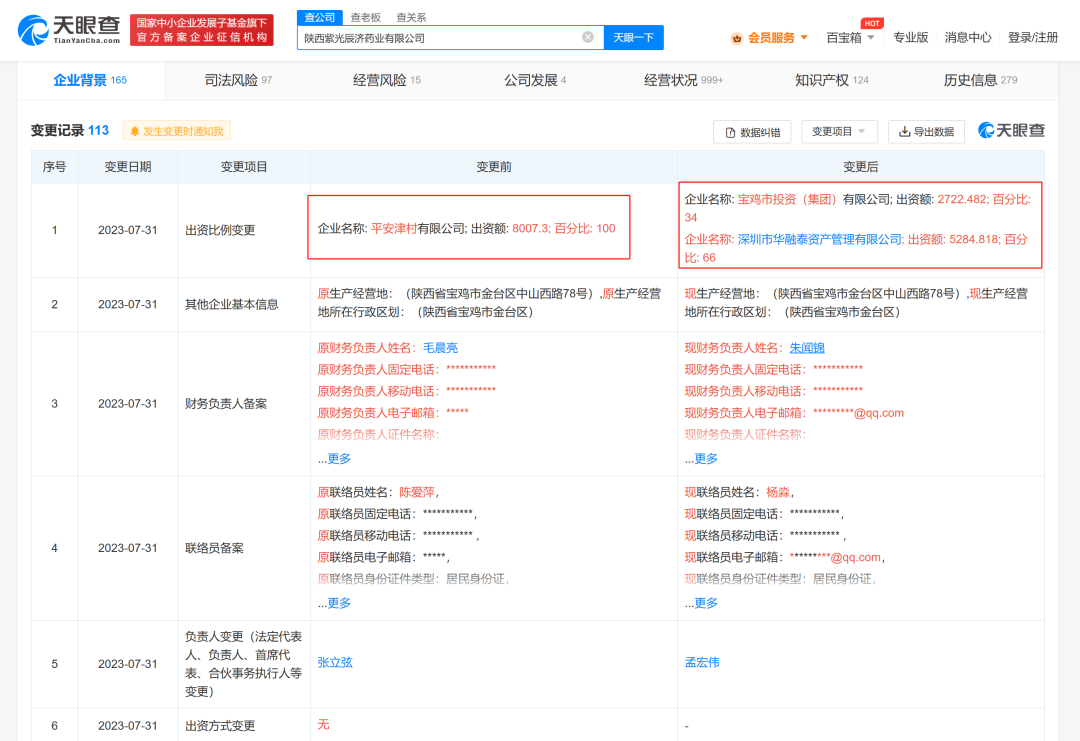
成立于1988年7月的武汉当代科技产业集团股份有限公司(简称“当代集团”)如今已经成立35年,集团业务覆盖医药、地产、文化等领域。根据公司官网显示,截至2020年9月30日,当代集团资产总额曾经逾1000亿元,参控股若干家上市公司。
而人福医药为当代集团仅剩的上市平台。
山东省纪委监委召开会议
据山东省纪委监委网站消息,8月7日,山东省纪委监委召开纪检监察机关配合开展全省医药领域腐败问题集中整治工作动员部署视频会议。

会议指出,配合开展医药领域腐败问题集中整治,是坚定拥护“两个确立”、坚决做到“两个维护”的实践检验,净化医药行业政治生态、推动医药卫生事业健康发展的迫切要求,回应群众关心关切、维护群众切身利益的具体行动。各级纪检监察机关要提高政治站位,切实增强做好配合开展医药领域腐败问题集中整治工作的责任感和使命感。要拉紧责任链条,压紧压实主体责任,切实扛牢监督责任,推动“两个责任”贯通联动,全力保障工作落实。
会议称,坚持严打开路,全面排查问题线索,注重突出查处重点,严厉打击行贿行为,精准把握政策策略,推动形成强力震慑。深化以案促改,以案为鉴强警示,建章立制堵漏洞,倡树新风树正气,全面推进长效治理。强化责任落实,加强组织领导,密切协作配合,严肃工作纪律,确保配合开展医药领域腐败问题集中整治工作取得实效。
人福医药实控人被立案
8月7日晚间,人福医药在上交所公告称,公司实际控制人艾路明于当日收到证监会《立案告知书》,因涉嫌信息披露违法违规,证监会决定对其立案。
人福医药表示,艾路明将积极配合中国证监会的调查工作,同时严格按照监管要求履行信息披露义务。公司董事、监事和高级管理人员目前均正常履职,上述事项不会对公司的日常运营造成重大影响。公司将严格按照监管机构相关规则的要求,及时履行后续进展情况的信息披露义务。

人福医药2022年财报显示,艾路明为当代科技董事长、武汉当代科技投资有限公司董事长兼总经理、武汉明诚金石科技有限公司董事长兼总经理、武汉当代乾源科技有限公司董事长兼总经理。
今年2月份,因当代科技及其关联方违规占用上市公司资金、当代科技大额违规减持股份、定期报告财务数据披露不准确等问题,人福医药、当代科技、艾路明等被上交所公开谴责。
据官网介绍,人福医药集团股份公司成立于1993年,于1997年在上海证券交易所上市。公司以医药工业为主、医药商业为辅。
人福医药是麻醉药龙头企业,在神经系统用药、甾体激素类药物、维吾尔民族药等细分领域形成领导或领先地位,近年来逐步拓展美国仿制药业务。该公司成立于1993年,1997年在上交所上市。2020年下半年,公司市值一度超过500亿元。
2022年度,该公司实现营业收入223.38亿元,较上年同期增长8.71%;归属于上市公司股东的净利润为24.84亿元,同比增长88.60%。截至2022年底,公司及下属子公司拥有548个药品生产批文,其中36个独家品规产品,共134个品规产品被纳入国家基药目录、287个产品被纳入国家医保目录(2022年)。同时,公司各子公司已累计获得近120个美国仿制药产品的ANDA批准文号。
截至7日收盘,人福医药报收21.69元/股,下跌0.96%,总市值354.12亿元。
三特索道及原实控人被立案
艾路明被立案,还涉及另一家公司——三特索道。
同样是8月7日晚间,三特索道发布公告称,公司及公司原实际控制人艾路明于2023年8月7日收到中国证监会下发的《立案告知书》(编号:证监立案字0052023013号)、(编号:证监立案字0052023014号)。因涉嫌信息披露违法违规,中国证监会决定对公司和艾路明立案。

三特索道表示,公司及艾路明将积极配合中国证监会立案调查工作,并严格按照相关法律法规的规定和监管要求及时履行信息披露义务。目前,公司各项生产经营活动正常有序开展。
此外,在两家公司之前,*ST明诚于7月26日宣布,上市公司被证监会决定立案,案由同为“涉嫌信息披露违法违规”。*ST明诚目前的实际控制人为武汉市国资委,在此之前*ST明诚的实际控制人同样为艾路明,双方的控制权交接完成于2021年8月24日。
来源:华夏时报
责编:Adam