
胰岛素抵抗(IR)是 T2DM、血脂异常、非酒精性脂肪性肝病、多囊卵巢综合症、动脉粥样硬化性心血管疾病(ASCVD)等多种慢性代谢相关性疾病的「共同土壤」[1]。临床上,2 型糖尿病(T2DM)与肥胖症、血脂异常、非酒精性脂肪肝等其他代谢性疾病共病十分常见。
因此,过去在制定治疗方案时,医生们常会面临一个选择,是针对不同疾病采取对应治疗方案各个击破,还是针对 IR 采取「一箭多雕」的治疗方法?
随着中国原创性 1 类降糖新药过氧化物酶体增殖物激活受体(PPAR)全激动剂西格列他钠面世,这一选择难题,被悄然打破。
本文将分享两个分别来自哈尔滨医科大学附属第一医院内分泌科刘殿新教授和开滦总医院内分泌科王彩宁教授的真实典型病例,还原其诊治过程,给 2 型糖尿病的临床诊疗治疗带来了新思路!更有来自同济大学附属东方医院冯波教授的精华点评,不容错过。一起来看看。
病例
01
刘殿新教授
哈尔滨医科大学附属第一医院内分泌科
患者,女性,46 岁。此次因「发现血糖升高半年,血糖不佳 1 周」就诊。
就诊前降糖方案:
二甲双胍 1,500 mg/d 治疗。一月前自行停药。
病例分析:
住院期间及出院后降糖方案调整:
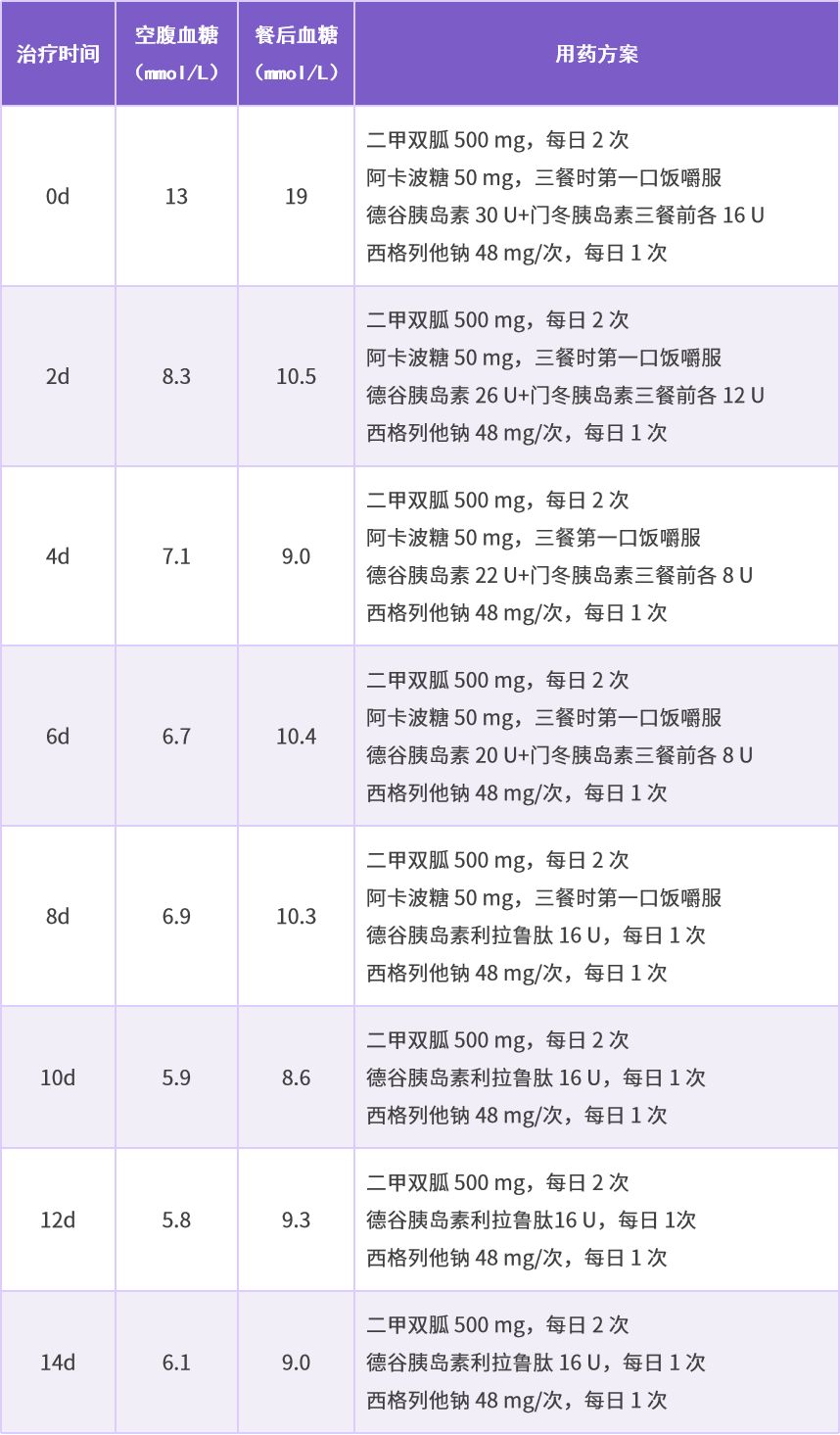
在生活方式干预的基础上,给予胰岛素泵强化二甲双胍治疗。治疗第 4 天,FPG 降至 8.9 mmol/L,2h PG 9~10 mmol/L,调整为基础-餐时胰岛素皮下注射,胰岛素总量达 53 U, 同时给予二甲双胍 0.5 g/次,每日 3 次,口服;治疗第 5 天,考虑患者胰岛素剂量大,IR 重,合并多种代谢性疾病,故加用西格列他钠 32 mg/次,每日 1 次,口服;治疗第 8 天,FPG 降至 5.8 mmol/L,2h PPG 9.0 mmol/L;治疗第 9 天,考虑患者 ASCVD 风险高,停用胰岛素,调整方案为司美格鲁肽 0.5 mg/次,每周 1 次;二甲双胍 0.5 g/次,每日 3 次,西格列他钠 48 mg/次,每日 1 次,并以此作为出院维持治疗方案。具体见表 1、表 2 为患者住院期间血脂变化。
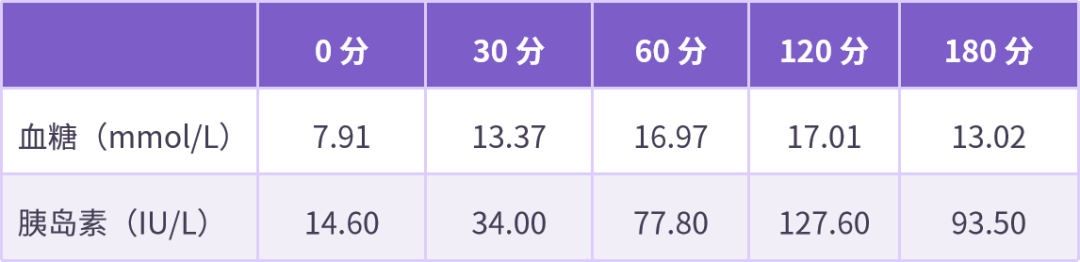
表 1 患者住院期间降糖方案调整过程(单位:mmol/L)
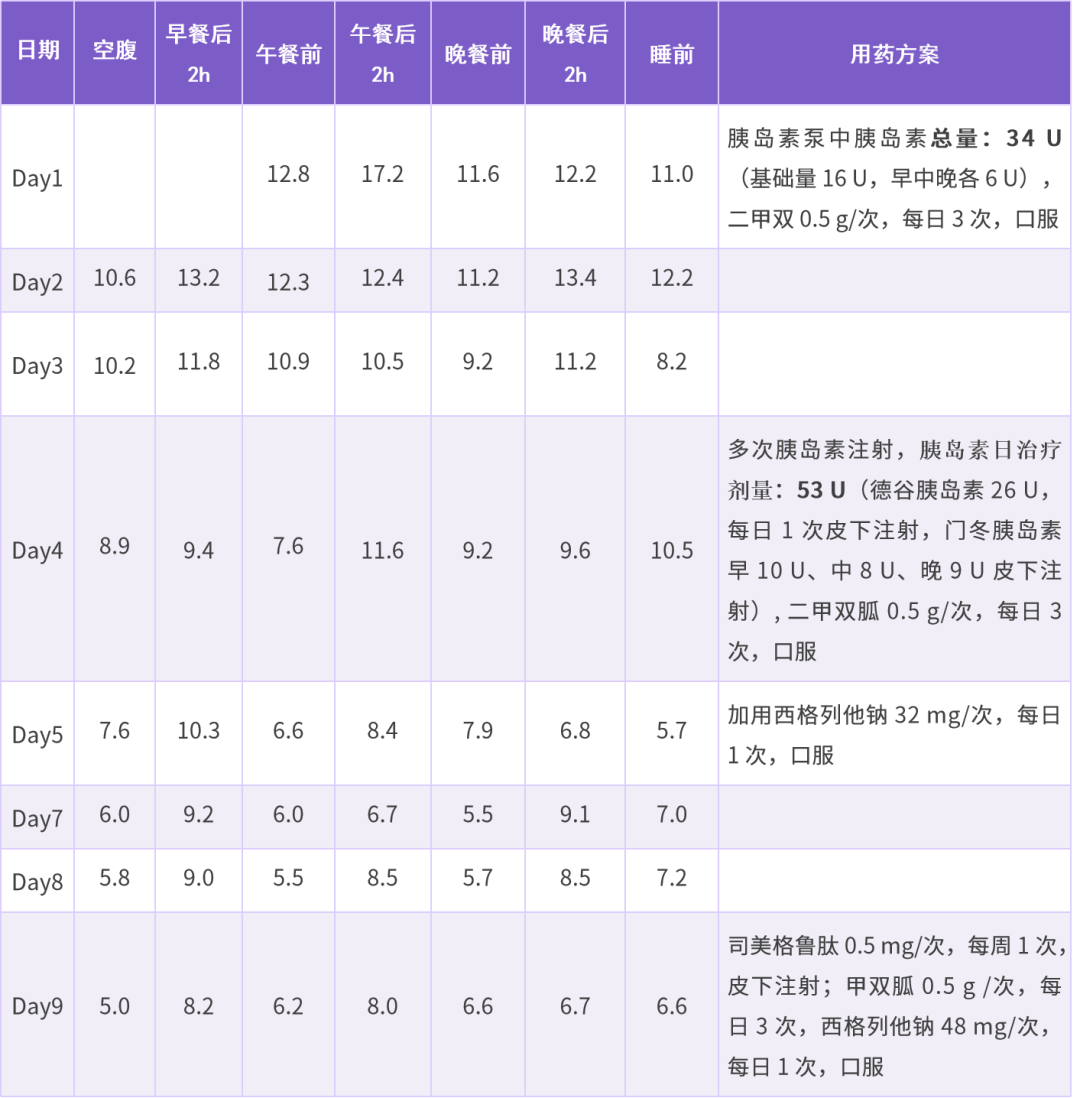
表 2 患者住院期间血脂变化(单位:mmol/L)
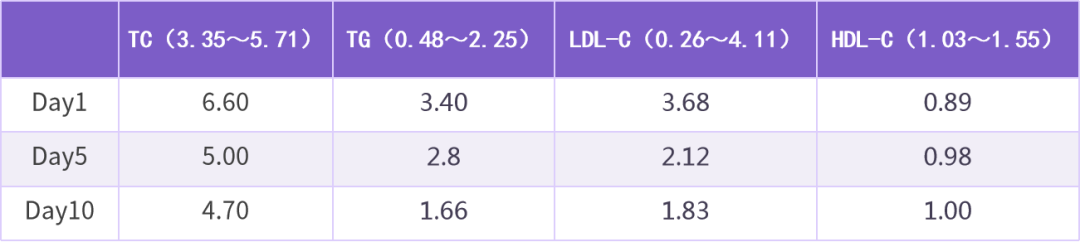
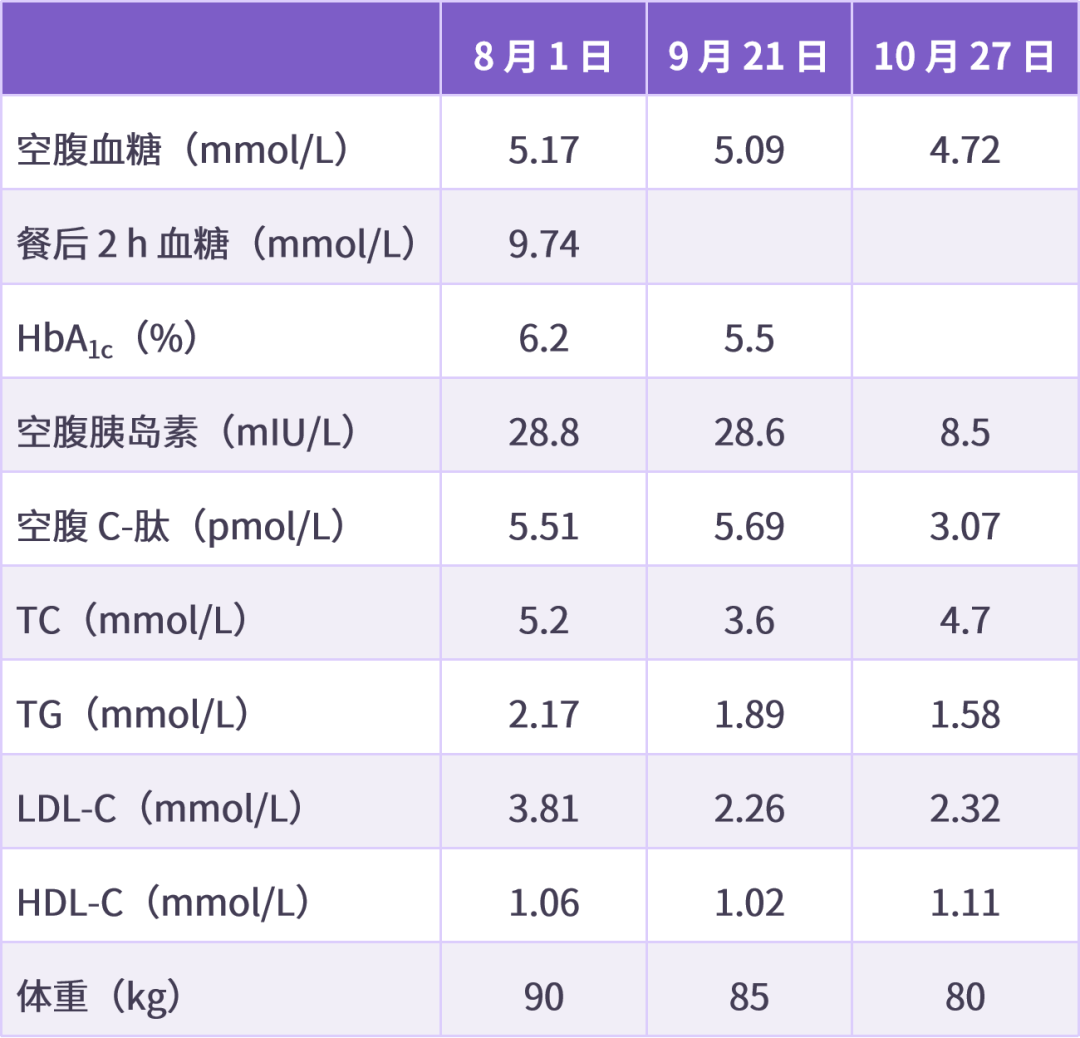
出院后,患者随访(治疗 2 个月)结果见表 3、表 4:
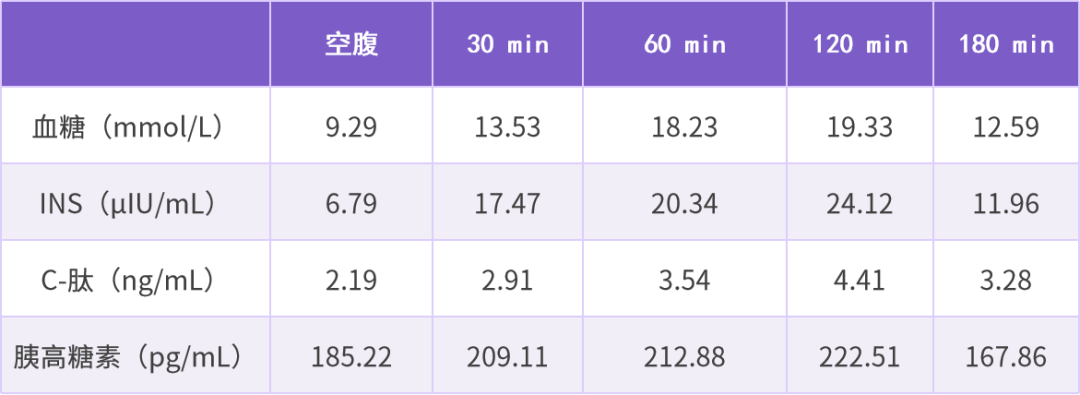
表 3 患者治疗 2 个月后血糖监测情况(单位:mmol/L)
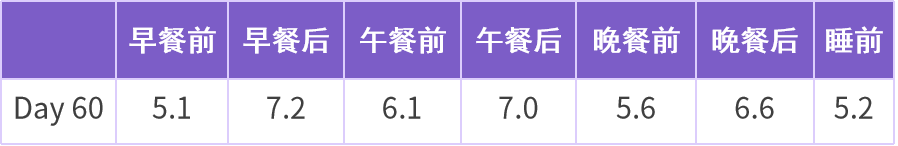
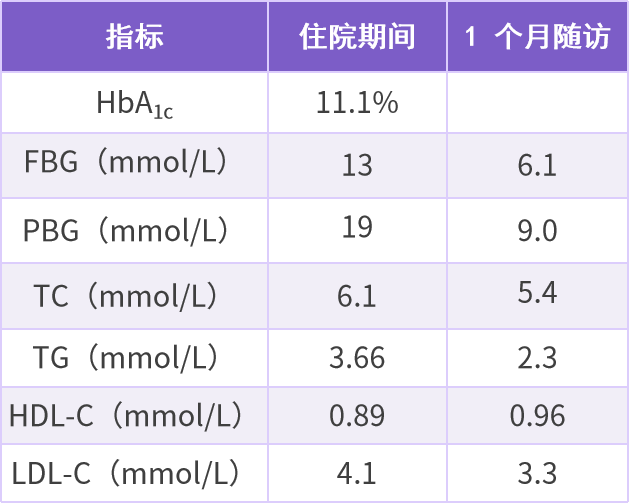
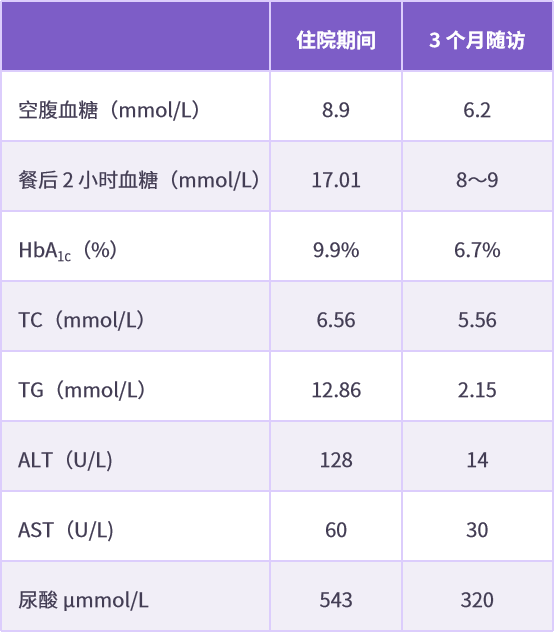
表 4 患者治疗 2 个月前后部分指标比较
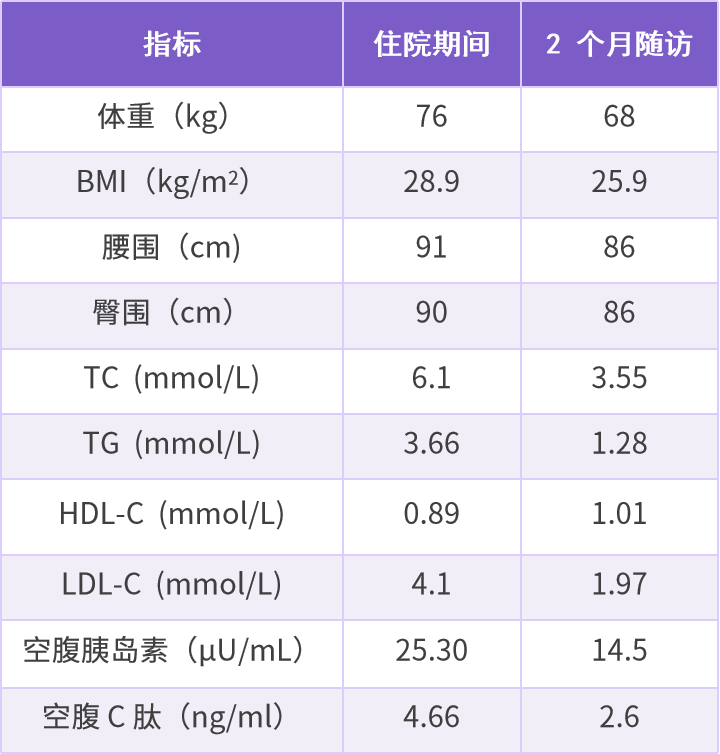
诊疗体会:
患者为中年 T2DM 患者,合并血脂异常、脂肪肝等多种代谢性疾病,IR 重,经胰岛素强化、二甲双胍治疗及加用西格列他钠改善 IR 以后,调整为每周一次注射胰高血糖素样肽-1 受体激动剂(GLP-1RA),联合西格列他钠和二甲双胍,使用简单,血糖控制良好,无低血糖发生,体重明显下降,血脂明显改善,生活质量得到提高,治疗满意度高。
病例
02
王彩宁教授
开滦总医院
患者,男,50 岁,此次因「多饮、多尿4年,加重伴头晕半年」就诊。
就诊前降糖方案:
二甲双胍缓释片 0.5 g/次,每日 1 次,达格列净 10 mg/次,每日 1 次,沙格列汀二甲双胍 1 片/次, 每晚 1 次。
病例分析:
血糖及血脂控制目标:
血糖控制目标为 FPG 4.4~6.1 mmol/L,2h PPG < 7.8 mmol/L,HbA1c < 7%,血脂控制目标为 LDL-C < 2.6 mmol/L,TG < 1.7 mmol/L。
降糖方案调整:
考虑患者合并 ASCVD 危险因素(高脂血症),伴有 IR,因此给予患者二甲双胍缓释片 1 g/次,每日 1 次,口服;西格列他钠 48 mg /次,每日 1 次,口服;度拉糖肽 1.5 mg/次,每周 1 次,皮下注射,联合抗血小板、降脂药物。
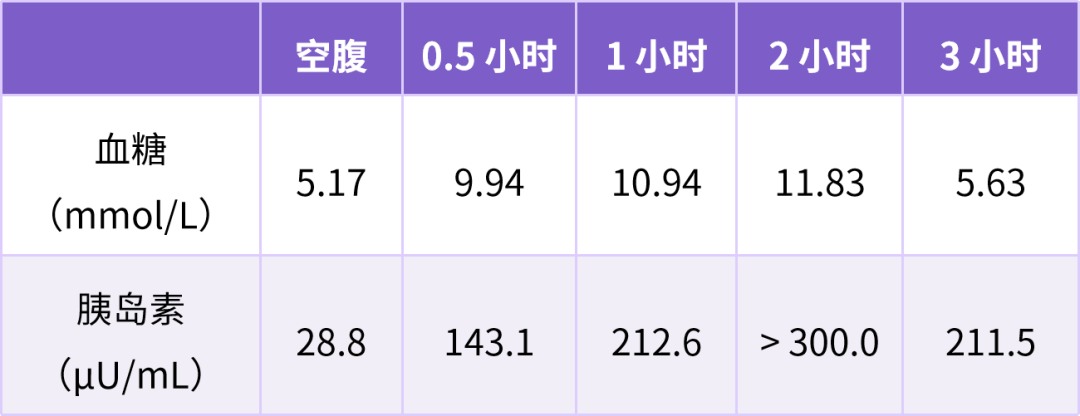
治疗 1 个月后,随访指标见表 6:
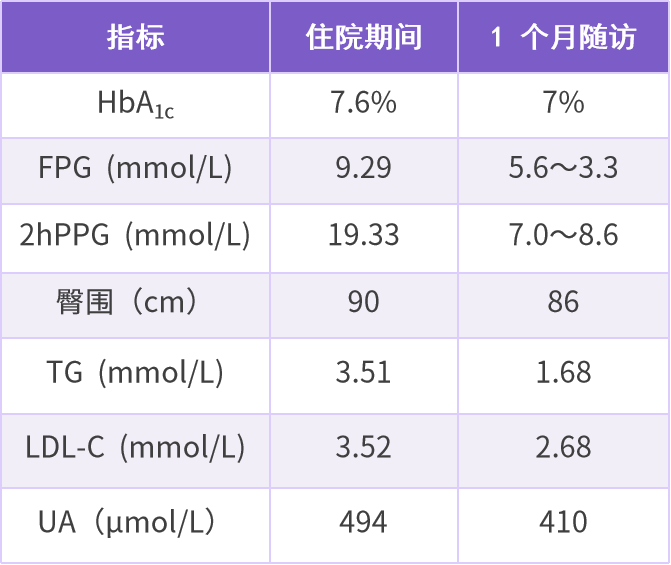
表 6 患者治疗 1 个月随访结果
诊疗体会:
本例患者为中年男性,T2DM 病史 4 年,伴有 IR 及 ASCVD 危险因素。西格列他钠可直接改善 IR ,有效持久降低 T2DM 患者的 HbA1c、FPG、2hPPG,同时能够调控血脂,整体安全性良好,联合二甲双胍、度拉糖肽治疗获得满意效果。
名家点评

临床上,由 IR 所引起的临床综合征称为胰岛素抵抗综合征(IRS),可分为两个临床类别[1]。其中一个类别是由 X 综合征演变而来,为代谢综合征的同义词[1],其组分较多,包括高胰岛素血症、高血压、T2DM、血脂异常、高尿酸血症、脂肪肝及肥胖等,IR 是 IRS 的共同病理生理基础,即共同土壤学说[2]。IR 和代偿性高胰岛素血症在分子病因学上能促进血管平滑肌细胞生长、增殖,导致炎症和动脉粥样硬化的发生,成为 ASCVD 发生、发展的危险因素之一[3]。
IR 是 T2DM 发生、发展的重要病理生理机制之一,T2DM 作为 IRS 的组分之一,常合并血脂异常、高尿酸血症、脂肪肝及肥胖等 IRS 的其它组分,因此,T2DM 患者不仅需要关注血糖达标,同时也要改善糖、脂、能量等代谢异常,以更好地预防和治疗因长期高血糖及相关代谢异常所导致的全身靶器官并发症,提高患者生活质量,延长预期寿命。
在本篇报导中的两个病例,非常好地体现了上述疾病特征及诊疗要点。这两个病例都合并体型超重/肥胖,以及 IR、高血糖、血脂代谢异常,高尿酸血症,并且都伴有脂肪性肝病。这些都是典型的 IRS 特点,并且均是 ASCVD 高危因素。
针对这两位患者的病例特点,缓解 IR 是治疗的当务之急,因此对于个疾病组分,除了常规给予降糖、降脂、抗血小板等对症治疗各个击破,都采用了以新型 PPAR 泛激动剂西格列他钠为基础、改善 IR 为主要手段的治疗方案,可「一箭多雕」,治疗效果也令人满意,两例患者治疗后均实现血糖平稳达标,血脂等代谢指标得到改善。
另外还有一个值得关注的是,本次报道的两个病例,均采用了二甲双胍 + 西格列他钠 + 胰高血糖素样肽-1 受体激动剂(GLP-1RA)的三联治疗方案。我们知道,理想的降糖方案应纠正 T2DM 发病机制的「八重奏」,兼具机制互补、有效降糖、安全性好等特点。从药物作用机制上,该三联方案对糖尿病的多重机制均有覆盖。二甲双胍可增加肌肉葡萄糖摄取及利用,并减少肝脏葡萄糖输出,改善外周 IR[4];PPAR 激动剂增强胰岛素敏感性,改善 IR;GLP-1RA 降糖的机制是通过激活 GLP‐1 受体以葡萄糖浓度依赖的方式刺激胰岛素分泌和抑制胰高糖素分泌,同时也可减轻体重[5]。因此,该三联方案在降糖、安全性和体重管理方面,具有明显优势。
前述治疗病例显示,新型的 PPAR 泛激动剂西格列他钠具备缓解 IR,全面改善糖、脂、能量代谢的作用,显示出良好的临床疗效和安全性[6]。当然,我们也需要更多的临床研究和实践来检验这一新药的长期疗效及安全性。
* 本文内容仅限医疗卫生人士观看,所述案例具有个性,仅供学术讨论与参考,不作为任何个人进行诊断与治疗的直接或间接建议。
内容策划:杨琤韵
内容审核:周洁
题图来源:图虫创意
参考文献


















![[BMT]T-ALL/LBL移植后西达本胺维持](https://cdn.thinkwit.com/unimm/cms/2023/09/frc-9fdb10af6e722e2467500ccfa1b513be.jpeg)
![[BMT]T-ALL/LBL移植后西达本胺维持](https://cdn.thinkwit.com/unimm/cms/2023/09/frc-159da8eee3eecbc3bf2a47da7da037ba.png)
![[BMT]T-ALL/LBL移植后西达本胺维持](https://cdn.thinkwit.com/unimm/cms/2023/09/frc-ee54827757e797376a2a70f6385b27d4.png)
![[BMT]T-ALL/LBL移植后西达本胺维持](https://cdn.thinkwit.com/unimm/cms/2023/09/frc-8f07e87e96bd6fc7438ed28f7b22e505.png)











