9月18日,GSK宣布高级副总裁兼研发负责人John Lepore已离职寻找外部机会。公开资料显示,John Lepore已在GSK任职近17年,担任GSK研发负责人超过5年。


又一个WordPress站点
9月18日,GSK宣布高级副总裁兼研发负责人John Lepore已离职寻找外部机会。公开资料显示,John Lepore已在GSK任职近17年,担任GSK研发负责人超过5年。


近期,诺华宣布其股东已经批准了仿制药与生物仿制药子公司山德士(Sandoz)100%分拆的提议,分拆后的山德士将作为一家独立公司在瑞士证券交易所上市。数据显示,2022年山德士营收为92.49亿美元。
诺华表示,此次剥离旨在使Sandoz成为欧洲一大仿制药公司和生物类似药企业,实现股东价值更大化,并使诺华股东充分参与Sandoz和诺华创新药的潜在未来发展 。同时,此次拆分将增强诺华专注力和独立发展战略的能力。
据了解,除了诺华,强生、默沙东、GSK等一众MNC企业近两年均有重大分拆改组动作。例如2022年7月,GSK旗下消费健康业务板块正式分拆,赫力昂横空出世。目前,赫力昂经营着一系列健康品牌,如钙尔奇、善存、舒适达、芬必得、扶他林、新康泰克、百多邦等。在分拆后,赫力昂业务进一步优化,2022年赫力昂全年实现有机收入增长9%,年收入达到109亿英镑。2023年上半年,赫力昂营收有机增长10.4%。
2022年9月,强生宣布将消费者健康业务分拆,作为独立公司上市,取名“Kenvue”。今年8月,Kenvue开始完全独立运营。当前,Kenvue旗下拥有约4个10亿美元的超级品牌和20个超过1.5亿美元的品牌,如邦廸、李施德林、露得清、泰诺、强生婴儿和城野医生等。今年上半年,Kenvue的净销售额为78.63亿美元,同比增长6.3%。
综合来看,药企分拆子公司上市,可以降低子公司融资成本,缓解母公司财务压力,同时也有利于加速子公司业务的发展进程。值得一提的是,目前除了大型跨国药企,在国内,大批本土药企其实也长在掀起分拆上市热潮。据悉,2023年以来,国内已有信立泰、辰欣药业、科伦药业、乐普医疗、微创医疗等多家上市公司分拆子公司上市。
其中,今年1月,科伦药业筹划分拆科伦博泰至香港联交所主板上市。3月末,信立泰计划分拆旗下信泰医疗至科创板上市。5月,港股上市公司微创医疗拟分拆微创心律至港股上市。6月,辰欣药业计划分拆旗下佛都药业至深市主板上市。7月,药明生物计划分拆药明合联赴港上市。7月24日,乐普医疗抛出子公司秉琨医疗至创业板上市的方案。
从进度上来看,上述分拆上市的药企中,进度较快的为科伦博泰。7月11日,科伦博泰正式在港交所挂牌,公司以60.6港元/股的价格首发募资约12.59亿港元。其他5家公司的分拆计划仍在推进当中。
而从分拆数量上来看,微创医疗近几年十分频繁。今年5月,微创心律递表港交所主板申请上市,这是微创医疗分拆的第6家子公司,在此之前,微创医疗已经分拆了心脉医疗、心通医疗、微创机器人、微创脑科学及微创电生理5家子公司上市,分别对应主动脉及外周血管、结构性心脏病、手术机器人、神经介入、电生理等创新业务。
近日,国家知识产权局对于涉及乌帕替尼的核心化合物专利做出专利权全部无效或部分无效的决定。乌帕替尼核心化合物专利权预计于2030年12月到期,而国家知识产权局的决定将使得艾伯维需要在中国市场提前面对仿制药厂商的竞争。






近年来,随着癌症、心血管慢性病、神经系统疾病等对早期诊断以及精准治疗的高需求,核医学“翻红”成为“明星”学科。

9月21日,云顶新耀宣布与Kezar Life Sciences共同宣布,双方签订合作与授权协议,在大中华区、韩国和部分东南亚国家进行临床开发和商业化Kezar的选择性免疫蛋白酶体抑制剂药物zetomipzomib,该药主要治疗包括狼疮性肾炎(LN)在内的系列自身免疫性疾病。







通过专业汇报得到想要的支持是药械产品经理的基础功。面对不同背景、场合、对象,汇报时都应该做到有理有据、侃侃而谈,把节奏带到自己想要的方向,达成预设的目的。
眼下这一刻却令不少人犯愁,季度末和年底汇报分沓而至,客户见不到、会议全喊停、业绩一塌糊涂,本来能邀功讨赏的汇报,搞不好就要变成被讨伐的“背锅”现场了。
实际上,每个产品经理结合产品线不同动态和个人风格,都会有不同程度地精彩呈现。但当下困境时期的市场汇报,以下三个核心要点不可缺少。
第一要点
通过数据来呈现市场和产品线动态
市场汇报数据化和图表化是展现产品经理专业性的第一步,汇报PPT的开篇越简洁越容易引起关注。
例如:今年业务完成1000万,去年完成2000万这样的描述句,不如一页PPT直接写“-100%”,让老板、销售、支持部门更坐立不安,全神贯注听你接下来口若悬河的分析。
再比如:行业里自家与竞品市场占有率的变化,也一定是两张Before & After的饼图更有可读性。同比市场容量、疾病趋势、门诊量变化、手术量多少、病人数量和动态,都以最简洁的数字、图表来表达,更能体现你对市场的敏锐和了解,为接下来的介绍做好铺垫。
这开篇是鼓励性还是鞭策性,取决于你选了哪个数字作为开端。销量下降是为接下来和销售的合作博弈打响前奏,发病率提高是为后续为公司要更多的资源做好铺垫。
第二要点
通过案例来说明业务遇到的困难
眼下药械行业普遍很难,业绩不好是普遍情况,被支持国产、带量采购、产品限价、竞品无下限挤压导致丢失份额。市场不好、竞品价格低,这个普遍现象老板们已经听累听厌倦了。
想要邀功或者谈困难,此时需要从面看到点了,通过具体案例的分享,说说故事是好方法。
例如,A药品因为国采在大部分公立医院逐渐退出舞台,此时产品经理Eric要谈成绩。把A省销售大力开发民营医院,接洽非公组织、挖掘民营医院潜力、培养民营学术力量,逐渐做成业务的案例做了分享。此举是为了老板们能保住剩余不多的销售军,以民营作为未来战地。
再例如,B进口手术设备公司在C省受到进口限制令挑战极大,招标时连连落败,产品经理在业绩汇报时,详细阐述了某家医院原本通过大量学术沟通和投入,主任的报告都已经获得院内大部门支持,只因为在最后招标时,被“政策”这个条例一票否决,两三年的投入顷刻摧毁。但销售、市场在各个环节的努力体现满分,属于不可抗力的失败原因,获得了管理层的理解。
第三要点
通过政策来考虑后续的行动
政策解读已经不再是政府事务部的工作,业绩与政策是100%正相关的属性。药械产品的推广工作,如果不能符合政策的大帽子,很多都是无用功。所以有思路的产品经理,政策解读应该作为汇报PPT里单独的一页来展现。
以后续政策为线索,串联到市场的动态,来解锁后续的业务行动方案,是一条相对逻辑靠谱的路径。
例如:医保报销政策的变化,如果在某省份是持续走高,透露了后续该疾病的报销比例增大,那么比起价格,质量更容易是医生的选择要点。在战略上,将高价产品作为KPI产品,让销售对高价产品的关注度更高,更容易达成指标。
第四要点
通过规划达成共识,推动后续合作
产品经理是孤单的将帅之才,大部分都是孤身作战,难得有些大产品线时手下才会放一两个人头。所以寻求合作,是所有汇报尾声的重中之重,也是所有完美战略能落地的重点。
没有人才不能成事,产品经理对于后续想达成的活动、项目、目标订单,应该在汇报时提议成立小组来分工突破,明确分工和职责,确定时间线和完成节点,负责人和监督人。在汇报当下就明确做与不做,让自己的汇报尾声可以明确下一步的合作人和工作,这样才是一个有重点的汇报。
药械产品经理想要职场路风生水起,有一句真理要谨记:干得多不如干得好,干得好不如说得好。这份工作,七分靠思路和实干,三分是靠说出来的。
思齐俱乐部是医药人学习分享社区,为医药个人学习赋能。作者观点和案例仅供学习方法使用,不代表商业公司真实情况。
本文版权归思齐俱乐部(member_siqi)所有,未经授权,禁止转载引用。

专栏作者/Grace
医疗行业生态及人性观察家
791亿美元,这是全球10款最具价值在研新药的净现值。也就是说,平均“药价”79亿美元。

9月22日,国家医保局召开2023年下半年例行新闻发布会,通报今年1月-8月医保基金整体运行与门诊统筹报销情况,并就医保目录调整、药品及高值医用耗材集采落地、医保基金安全情况等多个问题答记者问。据悉,今年3-8月间,2022年版医保目录中的346个协议期内谈判药品累计为患者降负超1000亿元;2023年版医保目录调整结果预计在12月初公布。
据介绍,今年1–8月,基本医疗保险基金(含生育保险,下同)总收入20923.33亿元,其中职工基本医疗保险基金收入14738.06亿元;基本医疗保险基金总支出17864.77亿元,其中职工基本医疗保险基金支出11257.30亿元。为让更多参保群众感受到实实在在好处,国家医保局积极推动报销定点零售药店门诊购药费用。截至今年8月,全国99%的职工医保统筹地区建立普通门诊统筹待遇,32.09万家定点医疗机构开通普通门诊统筹结算服务,累计结算13.14亿人次,结算医保基金1240.24亿元;25个省份的约14.14万家定点零售药店开通了门诊统筹报销服务,累计结算1.74亿人次,结算医保基金69.36亿元。国家医保局还明确,有条件的地区可逐步将居民医保门诊用药从高血压、糖尿病扩大到心脑血管疾病领域。
在谈及国家医保目录调整工作时,国家医保局医药服务管理司司长黄心宇表示,2022年版医保药品目录已于今年3月1日落地实施,医保目录协议期内的谈判药品共计346种。今年3-8月间,协议期内的谈判药品累计报销1.23亿人次,平均实际报销比例达69.7%,叠加降价和医保报销的双重因素,346种谈判药品已累计为患者减负1097亿元。
“2023年版医保目录调整工作坚持‘保基本’的定位,并对目录调整的具体规则进行了优化和改进,以充分体现医保的价值购买,体现对医药创新的支持。”黄心宇说,“2023年版医保目录的调整结果预计将在12月初公布,计划从2024年1月1日起正式执行。”
在发布会上,国家医保局价格招采司副司长王国栋介绍了药品及高值医用耗材集采落地的最新情况。他表示,第八批国家集采药品已经在今年7月份落地实施,所涉及的39个品种平均降价降幅56%,预计节约医药费用167亿;第三批高值医用耗材集采也于今年5月份落地实施,共涉及颈椎固定融合术、胸腰椎固定融合术、椎体成形术等5个产品大类,平均降幅达到84%,预计节约医药费用260亿元,“下一步国家医保局将持续扩大集采品种范围,坚持上下联动,让集采成效惠及广大患者。”
针对公众较为关心的医保基金安全问题,国家医保局基金监管司副司长顾荣表示,今年上半年,全国医保部门共检查定点医疗机构39万家,处理违法违规机构16万家,追回医保资金63.4亿元。自2018年国家医保局成立以来,全国医保系统追回的医保资金已经达到835亿元。未来,国家医保部门将常态化开展飞行检查、专项整治等行动,坚决守护好人民群众的看病钱、救命钱。
在此次发布会上,国家医保局办公室、规财法规司等相关负责人还围绕长期护理保险制度、提升医保覆盖率等问题回应了公众关切。
近日,FDA召开了非处方药咨询委员会会议,专门讨论口服去氧肾上腺素作为非处方咳嗽和感冒产品活性成分的有效性。
委员会讨论了口服去氧肾上腺素有效性的新数据,最终得出一致结论:
当前的科学数据,并不支持口服去氧肾上腺素作为鼻减充血剂的有效性(投票结果16:0)。虽然FDA没有明确说明剂量,但大量文献指出,口服去氧肾上腺素(40毫克)无效。
这意味着Sudafed PE这样的名牌药物(Sudafed PE约占去氧肾上腺素市场的五分之一),可能并没有像广告宣传的那样发挥减轻鼻塞的效果。
FDA认定这一感冒成分无效,哪些药品受影响?
去氧肾上腺素的「生前身后名」
去氧肾上腺素是一种α-1肾上腺素能受体激动剂。它通过刺激鼻道血管内壁平滑肌上的受体,导致血管收缩(变窄)。去氧肾上腺素通常用于缓解由普通感冒、过敏或鼻窦炎等疾病引起的鼻塞和不适。去氧肾上腺素的作用是缩小鼻道中的血管,从而减少肿胀和充血,使呼吸更容易。
尽管对于口服去氧肾上腺素的有效性提出了否定,但这是否等同于”无效“,最终还需要FDA拍板定夺。咨询委员会只负责向FDA提供独立的意见和建议,但最终的决定权在FDA手中。
笔者在药智数据库查询发现,国内上市药品中,含有去氧肾上腺素的口服非处方药,包含柳酚咖敏片等品种,其去氧肾上腺素的剂量大多在2.5mg-5mg之间。
尽管FDA咨询委员会给出了“无法证明有效性”的结论,但仍然存在很多不确定因素:
FDA是否会正式将去氧肾上腺素除名?
下架的药物,仅限于去氧肾上腺素作为唯一有效物质的药物,还是牵连所有包含去氧肾上腺素的复方制剂?
美国以外的监管机构会做出如何反应?
通常来说,当一种OTC药物从OTC monograph中删除,可能会对消费者、制造商和监管环境产生重大影响。这些影响可能会因具体药物、除名原因以及可用替代品而异。
如果去氧肾上腺素最终遭到FDA除名的话,可以想象,伪麻黄碱的需求量可能会出现激增,以填补去氧肾上腺素身后留下的巨大空缺。而如何在确保伪麻黄碱这种管控药物不流向甲基苯丙胺的方向,将成为美国政府需要重点关心的事情。对于患者来说,如何更容易地获得伪麻黄碱这种所谓的behind-the-counter药物(柜台后药物),也是一件关乎顺利过渡的事情。
除了化学减充血剂药物之外,桉树油、薄荷醇、生姜、大蒜、蜂蜜等自然疗法也具有缓解鼻塞的潜力。不知道这对于拥有悠久草本入药历史的中国来说,是否意味着一个机遇?
FDA的声明中还涉及到一项关键内容,即咨询委员会的建议仅涉及“口服”去氧肾上腺素(片剂或胶囊),而不针对鼻喷雾剂。含去氧肾上腺素的鼻喷雾剂不会受到任何连带影响。
对此,佛罗里达大学药学博士Leslie Hendeles表示,“只有口服途径是无效的,因为99%的母体药物在肠道和肝首过代谢时就失活了”。Hendeles领导了佛罗里达大学2015年提交的公民请愿书,要求从OTC鼻减充血剂产品的OTC monograph中删除口服去氧肾上腺素。FDA还表示,含有去氧肾上腺素的药物,对于散瞳和手术期间使用同样有效,并不受到此次决定的影响。
除名去氧肾上腺素
哪些品种将受影响?
在FDA官方网站上发布的声明称,有些产品仅含有去氧肾上腺素,而某些产品则含有去氧肾上腺素和另一种活性成分(例如对乙酰氨基酚或布洛芬),可针对鼻塞之外的其它症状,例如头痛或肌肉酸痛等,这些产品中的去氧肾上腺素的存在,并不会影响其他活性成分治疗这些症状。
但在FDA正式将去氧肾上腺素认定对缓解鼻塞无效,并将其从OTC monograph中除名之后,含有去氧肾上腺素成分的复方药物的命运目前仍待观察。FDA表示,含有去氧肾上腺素成分的产品大约有250种,其在2022年的销售额约为18亿美元。
受到去氧肾上腺素牵连的知名药物包括 Tylenol 、 NyQuil 、 Mucinex 、 Theraflu 和 Benadryl 等感冒和流感产品。如果FDA最终做出下架的决定,将有250种以上的产品受到影响。如果FDA遵循咨询小组的建议,强生、拜耳和其他制药商可能会被要求从商店货架上撤下含有去氧肾上腺素的口服药物。这可能会迫使消费者转而使用非处方药,或者使用含有去氧肾上腺素的鼻喷雾剂和滴剂。
美国消费者保健产品协会(CHPA,The Consumer Healthcare Products Association) 于9月12日发表声明,对FDA咨询委员会的调查结果表示失望,并敦促FDA将去氧肾上腺素继续留在市场上。
CHPA表示,撤销去氧肾上腺素的非处方药资格将对医药市场造成明显的破坏性。除名去氧肾上腺素的决定将增加消费者负担,原本可以轻松从药店购买到的OTC可能会无迹可寻。患者需要寻求替代疗法,或者向医生寻求处方,这将导致就诊次数和医疗费用增加。
CHPA还认为,除名去氧肾上腺素,无论对医药成本、患者依从性、供应链,都将造成意义深远的影响。FDA数据显示,去年美国零售店销售了2.42亿瓶含有去氧肾上腺素的药物,比2021年增长了30%。这些产品去年的销售额为18亿美元。
剥夺非处方药资格后
巨大空缺谁来填补?
如果去氧肾上腺素最终被FDA剥夺了非处方药资格,那么它身后留下的巨大空缺将由谁来填补?
伪麻黄碱(Pseudo-ephedrine) 算得上一号。伪麻黄素是一种去除鼻塞和鼻窦充血的药物,通常用于治疗感冒、过敏性鼻炎和鼻窦炎等呼吸道疾病的症状。
它可以有效收缩鼻腔和鼻窦中的血管,从而减轻鼻塞和流感症状。而且作为鼻减充血剂,伪麻黄碱比去氧肾上腺素更加有效。但更有效的药物却没有获得相应的市场份额,其中必有蹊跷。
实际上,伪麻黄碱因为可以当作合成甲基苯丙胺的原料而无法做到洁身自好。甲基苯丙胺就是俗称的冰毒。受到甲基苯丙胺瓜田李下的影响,许多国家对伪麻黄素的销售和购买都有限制,并要求购买者提供身份信息,以确保合法使用。
含有伪麻黄碱的产品仍然可以作为非处方药购买,但获取伪麻黄素药物不可能像去氧肾上腺素那样轻而易举。
相比于去氧肾上腺素2022年2.42亿瓶和18亿美元的销售额,同期伪麻黄素的销量估计为5100万件,销售额为5.42亿美元。
除了去氧肾上腺素和伪麻黄素之外,获批的nasal decongestant还包括:
Levomethamphetamine(左旋甲基苯丙胺,甲基苯丙胺的L-对映体,亦称左旋甲基安非他命):一种拟交感神经血管收缩剂,用于美国的一些非处方(OTC)鼻减充血剂。不同于右旋甲基苯丙胺,它在低剂量没有造成欣快或成瘾的特性。
Oxymetazoline(羟甲唑啉):一种α-1A肾上腺素受体激动剂,可用于治疗鼻充血、眼睛过敏反应以及与红斑痤疮相关的面部红斑。羟甲唑啉可作为鼻减充血剂用于非处方鼻用产品中。羟甲唑啉具有良好的外周血管收缩作用,直接激动血管α-1受体,引起鼻腔黏膜血管收缩,从而减轻炎症所致的充血和水肿。它起效迅速,在几分钟内即可发生作用,可维持数小时,能有效地解除鼻充血。
Ephedrine(麻黄碱):一种α和β肾上腺素能激动剂,用于治疗麻醉下低血压、过敏性疾病、支气管哮喘和鼻塞。
Propylhexedrine(丙己定):一种α-肾上腺素能激动剂,常用于鼻减充血吸入剂。它用于暂时缓解感冒、过敏性鼻炎或过敏引起的鼻塞。
Xylometazoline(丁苄唑啉,亦称赛洛唑啉):一种直接作用的α-肾上腺素能激动剂,用于对过敏或感冒引起的鼻充血和轻微炎症的对症治疗。不建议使用超过七天。同样,不建议三个月以下的婴儿使用,有的说法甚至建议不要在6岁以下儿童使用。
小结
虽然当前的科学数据,并不支持口服去氧肾上腺素作为鼻减充血剂的有效性,但缺乏有效性支持,不等同于“无效确认”。等待FDA的下一步动作。

为进一步规范和完善T-LBL的诊疗策略,由中国抗癌协会血液肿瘤专业委员会、中华医学会血液学分会、中国抗癌协会血液肿瘤专业委员会T细胞淋巴瘤工作组组织编写的首部《成人T淋巴母细胞淋巴瘤诊断与治疗中国专家共识 (2023年版) 》1(以下简称共识)于《中华血液学杂志》2023年第5期发布。该共识通讯作者为陆军军医大学新桥医院张曦教授和江苏省人民医院徐卫教授,执笔专家为陆军军医大学新桥医院高力教授、饶军教授和中国医学科学院血液病医院邹德慧教授,通过参考国内外文献进展并由全国近40位血液领域权威专家参与讨论最终制定,对该疾病的鉴别诊断和治疗有重要的参考价值和临床指导意义。

凝聚共识
专家组对成人T-LBL的临床表现、诊断、治疗等方面进行了系统阐述
(下拉阅读)
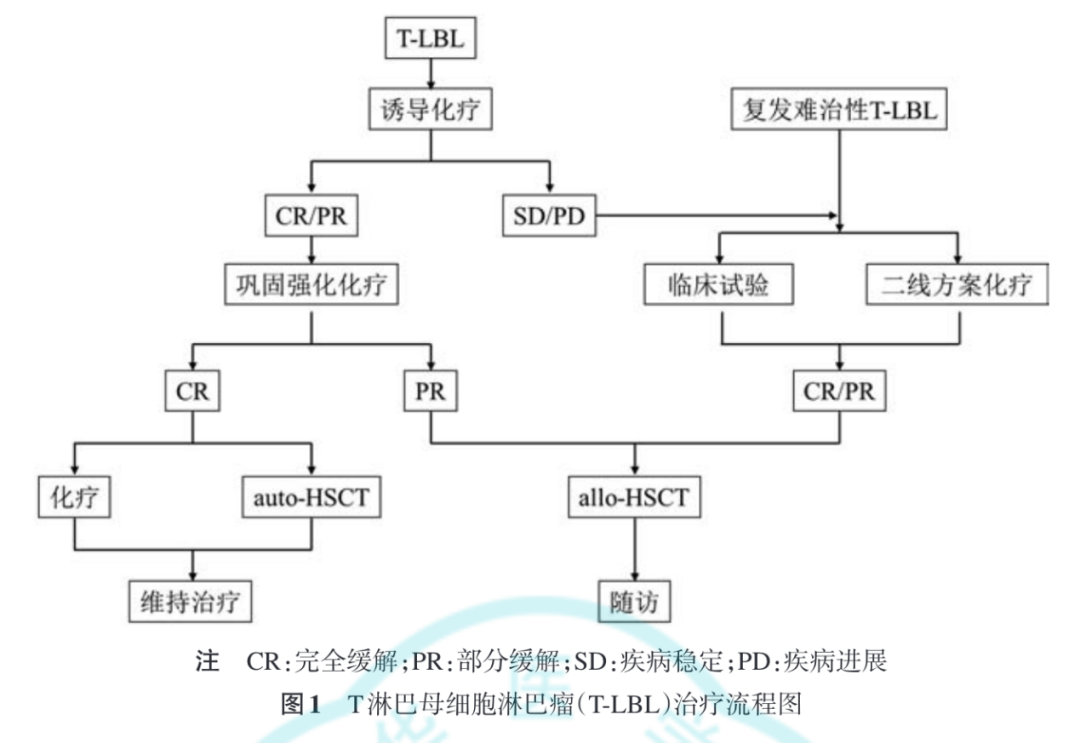

共识推荐
西达本胺维持治疗及复发难治患者西达本胺联合方案
"在共识推荐的成人T-LBL治疗方案中的维持治疗部分:表观遗传学药物(如西达本胺)值得尝试,需要更多的临床研究来证明其有效性。


"在共识推荐的复发难治(R/R)T-LBL的治疗再诱导方案包括西达本胺联合方案,ORR 71%, CR率47%,两个疗程CR率达65%。


聚焦循证
西达本胺在T-ALL/LBL的研究进展
一项基础研究2显示,西达本胺对T-ALL细胞系和原代细胞具有抗肿瘤作用,包括抑制NOTCH1活性。特别是,西达本胺通过下调细胞内形式的NOTCH1(NICD1)和MYC水平来抑制NOTCH1-MYC信号轴。研究还报道了临床试验的初步结果,支持西达本胺治疗可减少患者微小残留病灶(MRD)且耐受性良好。
一项临床研究3报道了T-ALL/LBL患者异基因造血干细胞移植后西达本胺维持治疗的可行性和安全性。18例高危T-ALL/LBL患者成功接受西达本胺作为异基因造血干细胞移植后维持治疗。此外,51例未接受任何维持治疗的患者纳入无维持治疗组。除无维持组中出现分子复发的3例患者外,所有患者均接受供体淋巴细胞输注(DLI)以预防血液学复发。中位随访时间为20.47(IQR, 12.77–22.80) 个月,与无维持组相比,西达本胺组1年EFSMRD显著改善(83.33% vs. 62.02%, P=.047)。
一项回顾性研究4分析了17例R/R T-LBL/ALL患者,接受西达本胺联合化疗作为挽救治疗。西达本胺+化疗1个疗程后,ORR为71%,CRR为47%。2个疗程后ORR为71%,CRR为65%,高于19例单纯化疗患者历史数据(1疗程CRR 16%, 2疗程CRR 37%)。西达本胺+化疗组与单纯化疗历史数据相比,2年PFS率显著改善(54.2%±16.2%和23.2%±17.6%, P=.0415)。
参考文献:
1. 中国抗癌协会血液肿瘤专业委员会,中华医学会血液学分会,中国抗癌协会血液肿瘤专业委员会T细胞淋巴瘤工作组. 成人T淋巴母细胞淋巴瘤诊断与治疗中国专家共识(2023年版)[J]. 中华血液学杂志,2023,44(05):353-358.DOI:10.3760/cma.j.issn.0253-2727.2023.05.001.
2. Xi M, Guo S, Bayin C, Peng L, Chuffart F, Bourova-Flin E, Rousseaux S, Khochbin S, Mi JQ, Wang J. Chidamide inhibits the NOTCH1-MYC signaling axis in T-cell acute lymphoblastic leukemia. Front Med. 2022 Jun;16(3):442-458. doi: 10.1007/s11684-021-0877-y. Epub 2021 Oct 20. PMID: 34669156.
3. Guo W, Cao Y, Liu J, Zheng X, Wang M, Zheng Y, Zhang X, Zhai W, Chen X, Zhang R, Ma Q, Yang D, Wei J, He Y, Pang A, Feng S, Han M, Jiang E. Chidamide maintenance therapy in high-risk T-ALL/T-LBL after allo-HSCT: a prospective, single-center, single-arm study. Bone Marrow Transplant. 2023 Jul 20. doi: 10.1038/s41409-023-02045-w. Epub ahead of print. PMID: 37474728.
4. Guan W, Jing Y, Dou L, Wang M, Xiao Y, Yu L. Chidamide in combination with chemotherapy in refractory and relapsed T lymphoblastic lymphoma/leukemia. Leuk Lymphoma. 2020 Apr;61(4):855-861. doi: 10.1080/10428194.2019.1691195. Epub 2019 Nov 22. PMID: 31755348.
责任编辑/校对:市场部医学支持小组/市场部