“华润系”中药、化药、生物药板块
多家药企高管生变
10月25日,华润三九发布公告,王雁飞因工作安排原因辞去副总裁一职。辞职后,王雁飞继续在华润三九担任其他职务。
不过,具体是什么职务,华润三九还未透露。
同日,华润三九董事杨旭东因工作变动辞去第九届董事会董事、董事会薪酬与考核委员会委员职务。杨旭东辞职后不再在华润三九担任职务。
王雁飞和杨旭东辞职后,华润三九很快确定了新的副总裁和董事,即黄先锋和梁柱强。
黄先锋曾任华润(集团)党群工作部专业总监、助理总监、副总监/副部长。更早之前,其任上海铁路局党校党史党建教研室助教、讲师,上海铁路局党委宣传部政工师、副科长、高级政工师、科长,国核工程党群工作部高级经理、副主任、主任等职务。现任华润三九副总裁。
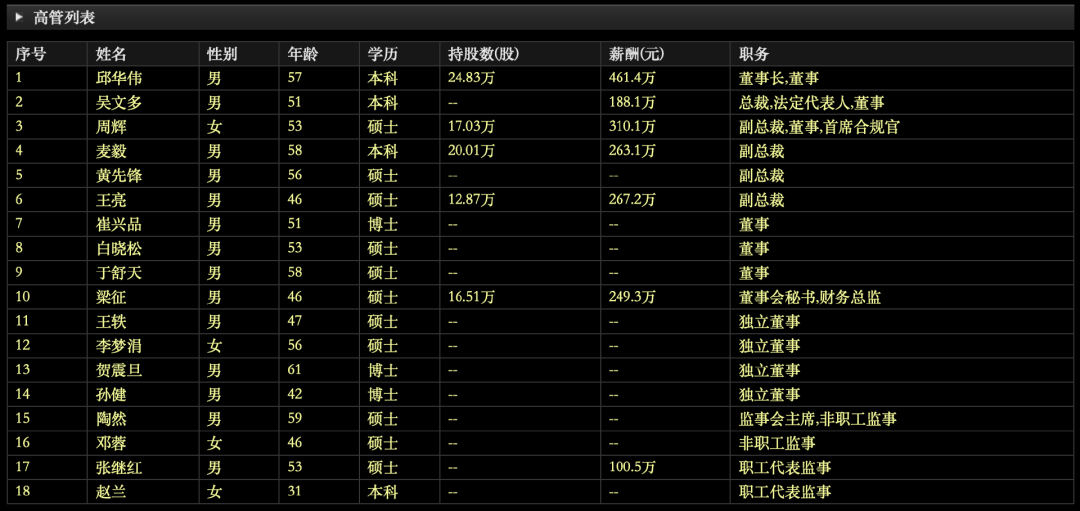
如今,华润三九依然有4位副总裁,即周辉、麦毅、黄先锋、王亮。
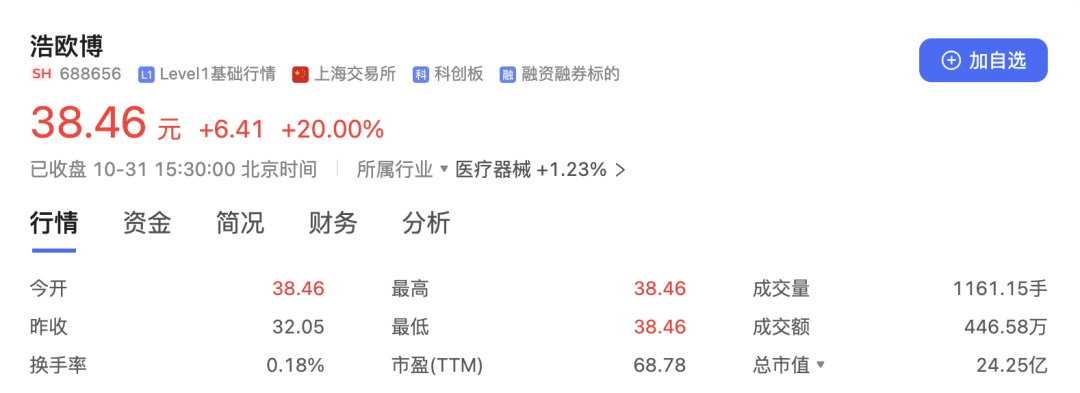
图源:东方财富网
不同于药企其它高管,副总裁往往在帮助企业制定战略、监督产品质量、管理销售团队、协调内部各部门和其它部门合作等方面发挥着重要作用。
今年来,华润三九已经发布过多次人士变动,涉及职位集中在副总裁、董事。值得一提的是,3月14日,时任华润三九董事、总裁的赵炳祥提交了辞职报告;9月,赵炳祥就任国药控股董事长。
此外,华润集团大健康领域的化药和生物药板块,华润双鹤和华润博雅生物的高管也发生了变化。
10月26日,华润双鹤发布公告,聘任赵骞担任总裁。另外,同意赵骞担任第十届董事会董事,杨战鏖不再担任董事职务。
加入华润双鹤之前,赵骞为湖北济川药业副总经理。今年10月1日,济川药业发布公告,因个人原因,赵骞申请辞去副总经理职务,辞职后不再担任其他职务。
赵骞曾任中国科学院上海有机化学研究所天然产物有机合成重点实验室助理研究员;江苏奥赛康药业药物研究院手性药物研究所所长助理,药物研究院院长助理、副院长;济川药业集团药物研究院院长、副总经理等。
10月25日,华润博雅生物发布公告,经总裁梁小明提名,华润博雅生物决定聘任任辉担任副总裁,任期自本次董事会审议通过之日起至本届董事会届满之日止。
加入华润博雅生物之前,任辉为东阿阿胶副总裁。10月23日,东阿阿胶发布多份公告,宣布其董事长、总裁等8人辞职的消息,除程杰就任董事长之外,其余7人不再担任东阿阿胶及控股子公司任何职务。
彼时,任辉申请辞去东阿阿胶副总裁职务,其中提到,任辉将前往东阿阿胶的关联单位任职。如今,终于尘埃落定。
华润医药帝国
麾下子公司共同推进“并购外延”战略
作为华润集团大健康板块的重要上市公司,华润三九、华润双鹤、华润博雅生物都有着不可替代的地位。
图源:华润医药官网
而这三家上市公司,在“华润系”并购外延的策略下,向外动作不断。
如华润三九,一是入主天士力。华润三九董事、副总裁周辉透露,通过天士力和华润三九整合,有助于三九双终端协同发展战略的有效落地。其称,预计争取明年1季度完成天士力收购交易工作。
对于天士力的发展,华润三九称未来其将保持独立的上市公司地位。未来三九将推动天士力在心脑血管、肿瘤、消化代谢、中枢神经等核心领域业务保持增长。
二是昆药集团与华润三九的融合变革,今年6月,昆药集团又收购了华润三九子公司,整合三七产业。昆药对华润三九业绩的辅助不言而喻,华润三九曾将2023年上半年业绩增长归因于CHC业务较快增长以及昆药集团自2023年1月19日起纳入合并报表范围。
截至10月31日收盘,华润三九总市值达577.95亿。相较于上个月赛柏蓝报道《华润三九新总裁上任》时,其总市值进一步上升。
近年来,华润三九不断提升其在中药领域的地位,2021年-2023年,其营收和净利润均实现了持续增长。今年前三季度,华润三九实现营收197.40亿元(+6.08%),实现归属于上市公司股东净利润29.60 亿元(+23.19%)。
在华润三九看来,发展需要持续关注行业合作及整合优质资源的机会。
华润双鹤则在今年上半年完成了31亿的收购,吞下华润紫竹,进行内部业务整合。华润系下女性健康平台华润紫竹的资源向华润双鹤集中。
华润双鹤曾称,积极通过外延发展方式加快产业整合、高质量产品获取。而华润紫竹的核心产品紧急避孕药毓婷、金毓婷多年来都稳居同行业市场第一。
综合来看,华润双鹤收并购的目光投向了合成生物领域、细分领域优质头部企业、创新孵化类企业。
此前,华润双鹤在《关于2024年度“提质增效重回报”行动方案的进展公告》中称,在研发创新方面,其按照“十年三步走”战略,已基本完成第一阶段“产品驱动期”核心能力构建,普仿药研发管线已形成一定数量项目的良性滚动循环,开启“技术驱动期”,并向“创新驱动期”迈进。
至于华润博雅生物,华润集团重要的血液制品平台,在今年7月,斥资18.2亿收购GC集团持有的绿十字香港控股有限公司100%股权,间接收购其在中国境内血液制品主体绿十字(中国)生物制品。
背靠华润集团后,华润博雅生物发展迅速。华润医药入主后,博雅生物曾设下目标,即力争在十四五期间(2021年到2025年)实现浆站数量30个以上,采浆规模1000吨以上。
不管是被收并购还是自身进行收并购,“华润系”下的多家药企都在大的并购外延政策下继续生长,而人才的更替也不可避免。
来源:赛柏蓝
作者:颜色