优药-AI市场计划助手,现已上线!
一站式BP生成服务,首个为处方药市场打造的AI驱动工具
好的 BP 工具,是帮你聚焦 “真正重要的事”。在医药市场,一份精准、可执行的市场计划(Business Plan, BP)往往需要团队数周甚至数月的调研、分析和撰写。政策频繁变动、竞争环境复杂、客户需求多元。这些因素使得传统BP制定过程充满挑战。
而现在
有一款工具正在悄然改变这一现状

技术持续突破,应用场景深度拓展
提升效率与创造力,重塑工作与生活方式
驱动创新,创造更大价值
从数据到策略,一站式生成
缩短80%时间,工作效率急速提升
如果你正卡在某份BP的环节
——不管是不知道怎么分析竞品新动作,还是凑不齐患者流数据,不妨打开它,输入你跟进的药品名称,先免费生成一份 “市场洞察简报”。这份简报里,可能有你没注意到的市场空白,也有最新政策提示
——或许,它能帮你少改2版方案,多留1晚休息时间。
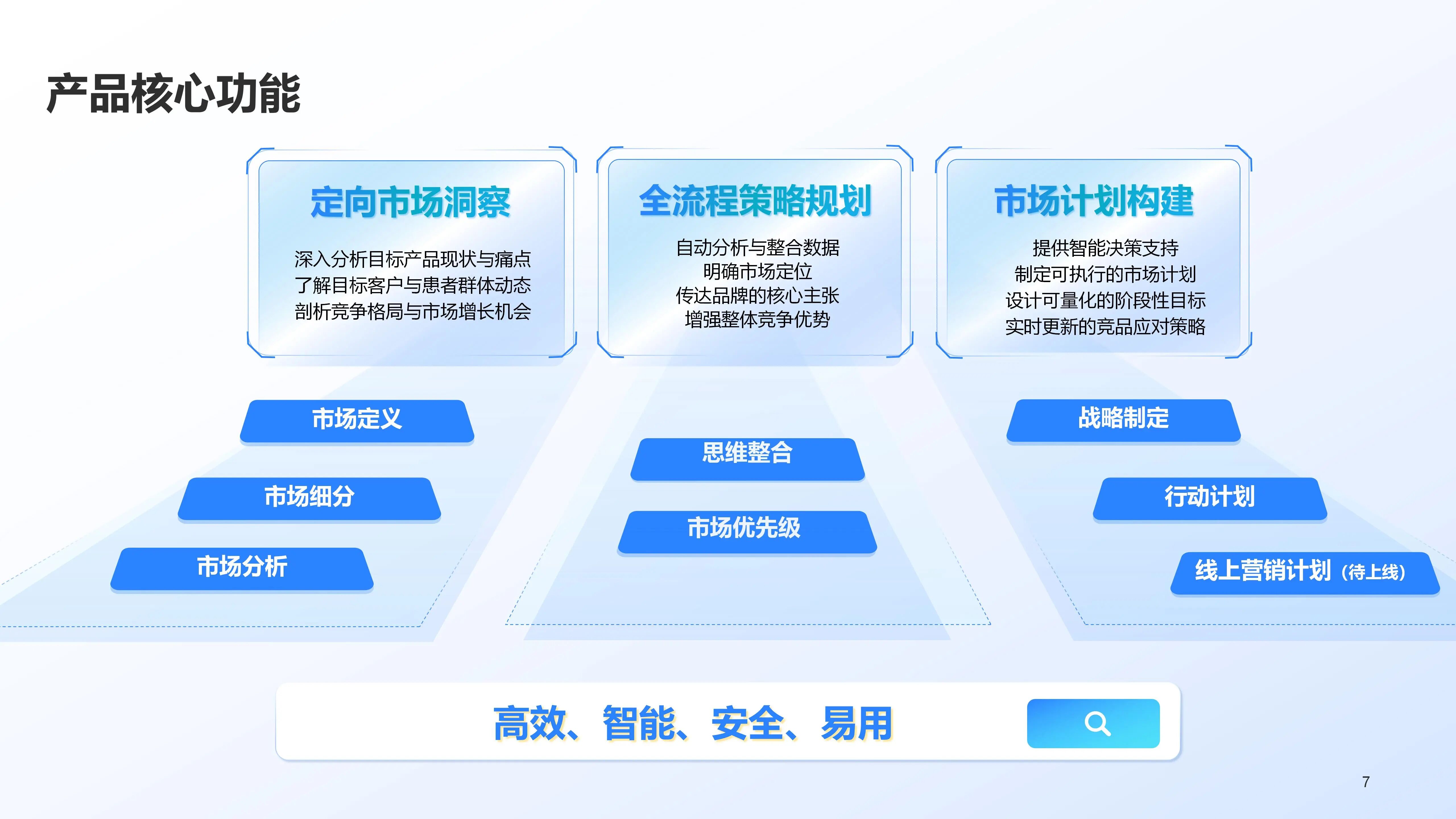
市场洞察
10分钟生成市场洞察:自动抓取政策、医保、竞品信息,输出结构化分析
思维整合
智能思维整合与优先级判断:帮助明确资源投放重点,避免“撒网式”策略;
落地计划
可落地市场计划输出:包含SWOT分析、关键成功因素、阶段性目标、执行时间表等
实时修正
支持多模块协作与实时修正:可基于实际反馈动态调整计划内容。
覆盖BP全生命周期
无论是新产品上市,还是成熟产品策略优化,这款助手都能提供支持:

市场
市场定义与细分:快速厘清适应症市场容量与患者流
格局
竞争格局分析:实时监控竞品动态与市场缺口
资源
资源分配计划:基于优先级生成预算、人力、渠道建议
团队
团队协作与汇报:一键导出结构化PDF,支持内部分享与评审
为什么医药市场需要它?
-
分析周期太长,市场变化太快
-
数据散落,整理成本太高
-
缺乏系统性的思维框架
-
独立完成高质量BP真不简单
优药-AI市场计划助手正是为了应对这些痛点而生:
不是替代人,而是赋能人——通过AI处理重复性、数据密集型工作,让你更专注于策略判断与决策。
如果你正在寻找一种更聪明、更高效的方式制定市场计划,欢迎体验“AI市场计划助手”,期待它为你的下一份BP带来改变。

复制下方网址至浏览器,即刻体验
仅网页端可以进入
手机端无法进入哦~
https://www.siqiquan.org/#/aiMarketHelper