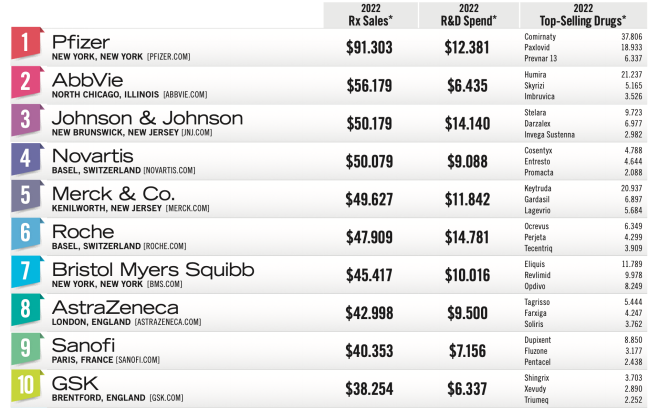
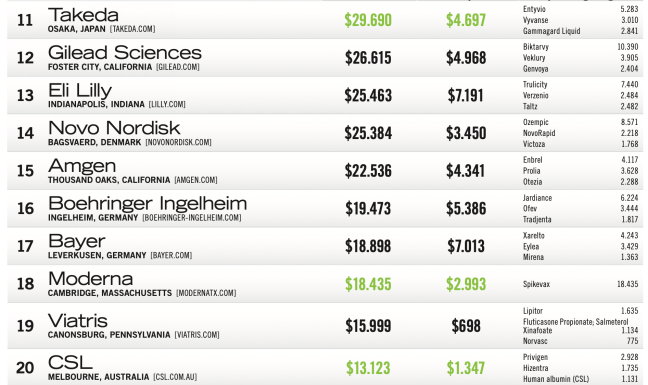
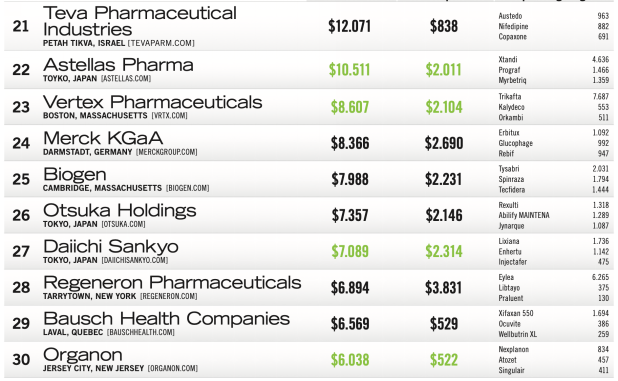
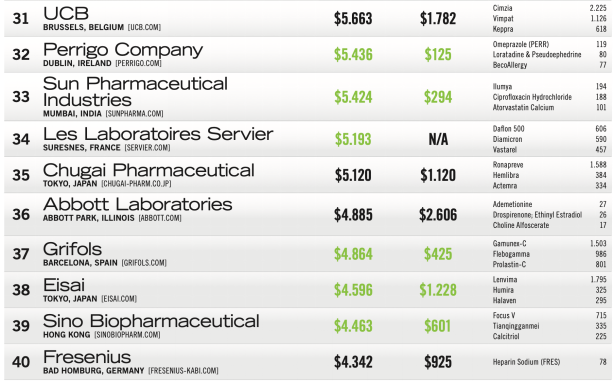
阿斯利康再次展开合作,布局Treg细胞疗法。
6月9日,阿斯利康宣布与Quell Therapeutics(一家专注于工程Treg细胞疗法的生物技术公司)达成协议,以开发多种Treg细胞疗法,这些疗法可能用于1型糖尿病(T1D)和炎症性肠病(IBD)的治疗。

Tregs具有抑制机体免疫反应、对自身抗原主动耐受、参与肿瘤免疫逃逸、抗炎等功能,可以通过多种机制阻碍抗肿瘤免疫反应,同时具备着抑制造成炎症的过度免疫反应的功能。
根据协议条款,阿斯利康将向Quell支付8500万美元的预付款,其中包括主要的现金支付和股权投资。后续Quell有资格获得超过20亿美元(按当前汇率计算,约为142.6亿元)的进一步开发和商业化里程碑。 与此同时,Quell保留一项选择权,可在研究性新药(IND)申请获得批准后或在I/II期临床研究结束时行使,与美国阿斯利康公司共同开发T1D计划的Treg细胞疗法,以换取额外的里程碑付款和美国净销售额的增加版税。
不完全统计,这也是阿斯利康今年来资金量排在最前列的一笔收购。
据悉,Quell Therapeutics于2021年完成1.56亿美元B轮融资,主要用于推进CAR-Treg细胞疗法实验以及临床管线开发等。2019年完成3500万英镑的A轮融资。目前为止,Quell已经筹集了约2.2亿美元。
阿斯利康表示,希望通过Quell合作,扩大其下一代治疗工具,并探索Treg细胞疗法在自身免疫适应症方面尚未开发的潜力。
Treg细胞疗法多用在开发自免、移植排斥等,受到业内广泛关注。
例如:2023年3月,再生元和Sonoma Therapeutics宣布合作,将其科学和临床专业知识以及各自的技术平台应用于发现、开发和商业化新型调节性T细胞治疗自身免疫性疾病,根据协议条款,Sonoma Biotheraputics将获得7500万美元的预付款,其中包括再生元对Sonoma的3000万美元股权投资,Sonoma也有资格获得4500万美元的开发里程碑付款,潜在交易金额达1.2亿美元。
2022年8月10日,百时美施贵宝与GentiBio达成合作,共同开发治疗炎症性肠病(IBD)的Treg疗法,BMS以高达19亿美元的总付款获得最高3个相关项目的开发与临床试验推进权利。
向外寻求合作
向内自我调整
大的跨国药企合作或者收购等动作一直是衡量生物医药行业热点的风向标。当前,医药市场不断变化,跨国药企之间的合作也越来越密集。
仅从今年看,阿斯利康已经与多家药企达成合作,交易金额均不小。
例如:5月18日,阿斯利康与Revvity公司签署了一项非独家授权协议,将使用该公司专有的基因编辑技术来开发针对癌症和免疫介导疾病的细胞疗法;
5月12日,礼新医药宣布与阿斯利康就临床前阶段的GPRC5D靶向抗体偶联药物LM-305项目达成全球独家授权协议,根据协议条款,阿斯利康将获得LM-305的研究、开发和商业化的独家全球许可。礼新医药将有资格获得包括首付款在内共计5500万美元的近期付款,以及最高达5.45亿美元的潜在开发和商业里程碑付款,外加全球净销售额的分级特许权使用费;
2月,阿斯利康宣布与KYM Biosciences(由康诺亚和乐普生物的关联公司成立的合资企业)就潜在世界首创Claudin18.2抗体偶联药物CMG901达成全球独家授权协议。根据许可协议,KYM Biosciences将获得6300万美元的预付款和超过11亿美元的潜在额外研发和销售相关的里程碑付款,以及高达低双位数的分层特许权使用费,阿斯利康将获得CMG901研究、开发、注册、生产和商业化的独家全球许可。
通过收购和引进药物等动作加注自身未来的发展,从阿斯利康的频繁动作来看,似乎已经是常事。而在每一次的“双向奔赴”中,阿斯利康基本都是基于自身原有领域的管线再次加注,进一步扩大相关领域的市场布局。
药企之间掀起了一股合作潮,医药上市公司聚焦主业、寻求未来业绩增长点的争夺战越来越激烈。业内有人认为,药企之间合作主要是因为医药产品一般研发周期长、投入大,和已经研发了一段时间、市场潜力大的产品企业合作,可以加速药品的商务化布局,节省资金。
强强联合已成趋势,行业集中度正逐步提高。
此前,商务部发布的《关于“十四五”时期促进药品流通行业高质量发展的指导意见》表示,到2025年,培育形成 “1-3家超五千亿元、5-10家超千亿元的大型数字化、综合性药品流通企业”。
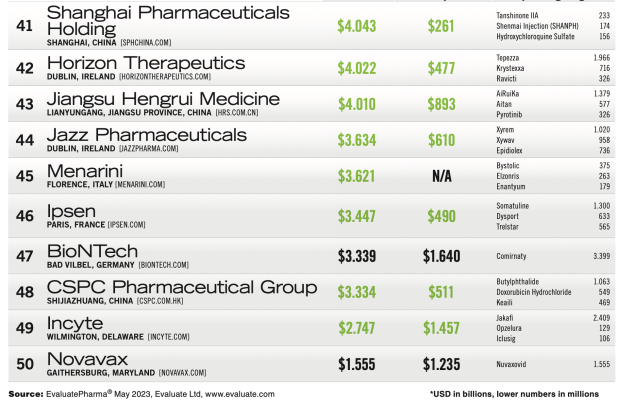
2023年一季度业绩报告显示,阿斯利康实现营收108.79亿美元,按固定汇率计同比持平。排除疫情形势变化后新冠产品组合的下滑,阿斯利康实现了营收同比15%的增长。
合作、追逐新的疗法,“阿斯利康”们还在继续……不过,不管是一窝蜂追逐某个疗法,还是放弃某个领域,技术永远在更迭。
来源:赛柏蓝
作者:颜色
责编:Adam