9月9日,A股细胞和基因治疗相关上市公司股价突然暴涨。济民健康、冠昊生物、中源协和等股价纷纷涨停。
商务合作
130 6172 3098
zakk.cui@siqibest.com
又一个WordPress站点
9月9日,A股细胞和基因治疗相关上市公司股价突然暴涨。济民健康、冠昊生物、中源协和等股价纷纷涨停。

商务合作
130 6172 3098
zakk.cui@siqibest.com
据“罗湿兄”9月7日消息,欧加隆零售业务负责人辛丽即将离职,零售团队将由沈斌带领。
沈斌目前所负责的团队,包括经销商团队、CSO团队和KAM团队,汇报线保持不变。
此前,欧加隆还进行过一次架构调整。
今年6月底,欧加隆大客户管理和女性健康销售高级总监傅江安离职。
自7月1日起,女性健康销售团队将与经典品牌医院销售团队合并,成立医院事业部,由贾敏领导;女性健康市场团队将与经典品牌及非处方产品市场团队合并,成立市场部,由林玉玮领导;大客户管理团队将与商务运营与创新商业模式发展部合并,由沈斌领导。
欧加隆于2021年6月正式从默沙东独立出来,至今已经三周年。目前,欧加隆在全球提供超过60种药物和医疗解决方案的产品组合,覆盖一系列疾病治疗领域。
据最新业绩数据,欧加隆在今年第二季度的营收为16.07亿美元,上年同期为16.08亿美元;季度净利润1.95亿美元,上年同期为2.42亿美元。
参考资料:
[1] 罗湿兄:《欧加隆业务负责人离职》
[2] 医药健闻:《强生、辉瑞、罗氏、礼来、诺和诺德、武田等35家大药厂2024年第二季度财报汇总》
[3] 默沙东中国:《默沙东宣布完成对欧加隆的分拆》

商务合作
130 6172 3098
zakk.cui@siqibest.com
巧用商业画布图,解决BP制作中最大难点——内外部营销情况回顾与总结。
内外部营销情况回顾与总结是BP制作的开场大戏,这个环节的困难点在于如何巧妙概括纷繁复杂的各种信息,又如何清晰凝练作者的观点。概括时往往很难面面俱到——有时候写了很多,却不是重点;凝练时又很难条理清晰——有时候想了很多,却说不清楚。
商业画布图是营销里经典的分析工具,但药械行业却很少应用。就BP制作来说,这个分析工具可以帮助产品经理梳理思路,形成分析营销情况的系统性框架,非常容易上手且实用。
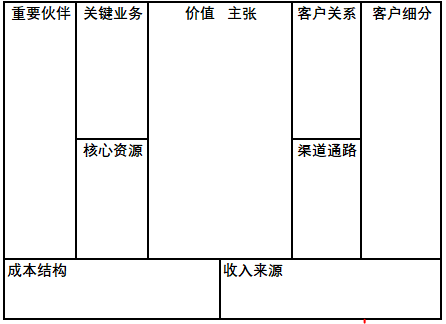
商业画布图的应用方式和逻辑思路
产品经理们在填写时,可以把每个版块作为独立的思考,用简单的数据来归纳总结每个版块的现状,再有逻辑地阐述这张图表。
它的逻辑点在于:左边的“重要合作伙伴”“关键业务”“核心资源”,包含了业务现阶段内部的现状;右边的“客户关系”“客户细分”“渠道通路”,包含了产品线外部的运营状况。而成本结构、收入来源,这两项是检验工作成果的,简单来说就是检验付出与得到之间是否平衡。
对于所有的组织、业务、产品来说,价值主张是不可缺少的“精神支撑”。产品的价值主张决定了业务投资的方向、合作伙伴的选择、项目的建立标准,所以放在商业画布图的核心位置,也是平衡左边的付出、右边的得到是否合理的“砝码”。
如何妙用商业画布图?
以BP中的使用为例,针对药械这个赛道,笔者做了细微调整,在维持商业画布图精髓的前提下,进一步细化了每个版块可以归纳总结的重点。
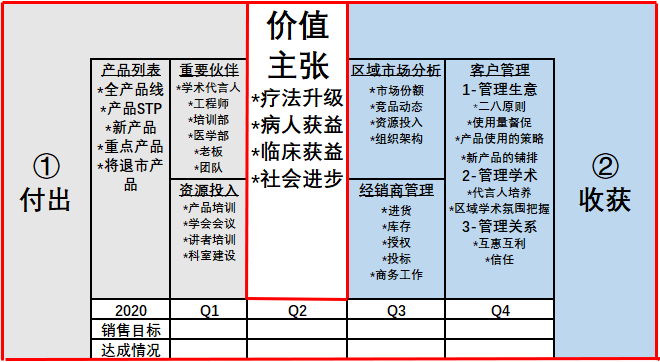
注:此图为作者版权所有,如有转载请注明。
整个商业画布图的结构依然分为两大板块:盘点内部的情况——即左边的付出,总结外部的运营状态——即右边的收获;以价值主张为判定左右两边是否在正确赛道上的标志。
在资源投入、重要伙伴、产品列表上可以简单地罗列目前事项进度,在市场分析、客户管理、经销商管理则可以判断业务是否健康,市场是否向上。
在原图的成本与营收上,考虑到药械行业很多会议、资源很难量化,那么判定产品线的销售目标和达成情况,是业务做得好不好的金标准。虽然简单粗暴,却一目了然地让汇报对象搞清业务现状。
归纳和总结是PM的两个基本功力,尤其对于复杂的内外部情况,往往容易捡了芝麻丢了西瓜。内外部运营所带来的业绩表现是老板们关注的重头戏,巧用商业画布图,就可以做到逻辑完整、表达清晰。
思齐俱乐部是医药人学习分享社区,为医药个人学习赋能。作者观点和案例仅供学习方法使用,不代表商业公司真实情况。
本文版权归思齐俱乐部(member_siqi)所有,未经授权,禁止转载引用。

专栏作者/Grace
医疗行业生态及人性观察家



时隔半年,华润三九新总裁终于确定。
华润三九总裁确定
高管团队生变
9月6日,华润三九发布公告称,聘任吴文多担任总裁。

华润三九时隔前任总裁赵炳祥辞职半年后,迎来新总裁。
3月13日,华润三九对外公告称,董事、总裁赵炳祥提交辞职报告,因工作变动,赵炳祥辞去华润三九第八届董事会董事、董事会战略投资委员会委员以及总裁职务。其后很快(4月1日),赵炳祥被提名为国药集团总经理。
同一天(9月6日),华润三九还发布了多个管理层变动的公告。副总裁徐永前由于工作变动原因,辞去副总裁职务;梁征辞去董事职务,不再出席董事会会议,辞职后继续担任财务总监、董事会秘书职务。
现如今,华润三九高级管理人员包括总裁吴文多;副总裁麦毅、周辉、王雁飞、王亮,以及财务总监、董事会秘书梁征。
从履历看,吴文多和华润系很多人的晋升之路一样,都离不开在华润系多家公司的历练。
吴文多曾任北京赛科昌盛医药业务部经理、总经理助理兼策划部经理、人力资源部经理、副总经理、常务副总经理、总经理,北京赛科药业营销部经理、副总经理、总经理,华润赛科药业总经理,华润双鹤副总裁,华润三九副总裁,华润江中总经理。
除任华润三九总裁外,吴文多还是江中药业的董事,并拟任华润三九董事。
国企通过轮岗交流,让不同人员在不同岗位和环境中得到全面锻炼,或许这也是华润系一直以来培养综合能力较强的复合型人才的重要策略。
市值上升
归母净利润已连续三年增长
截至9月9日14:49,华润三九总市值达575.38亿。相较于今年3月份(3月14日,华润三九总市值为531.64亿元),华润三九的总市值进一步上升。
作为A股市值仅次于片仔癀(1221.66亿元)、云南白药(944.41亿元)的中药巨头,华润三九近三年来的营收和归母净利润均实现了增长。
2021年-2023年,华润三九营收分别为155.44亿元(+13.98%)、180.79亿元(+16.31%)、247.39亿元(+36.83%);归母净利润分别为20.55亿元(+28.65%)、24.49亿元(+19.16%)、28.53亿元(+16.50%)。
走出2020年营收和归母净利润双双下降的华润三九,此后业绩均在向上。
今年上半年,华润三九营收为141.06亿元,同比增长7.30%;归母净利润为23.98亿元,同比增长27.77%。
分产品来看,2024上半年,华润三九的自我诊疗(CHC)收入77.73亿元,同比增长14.00%,占总营收的55.11%;处方药收入24.17亿元,同比下降13.07%,占总营收的17.13%;传统国药(昆药)收入19.56亿元,同比增长5.14%,占总营收的13.87%。
CHC依然是牵动华润三九业绩增长最“大头”的业务之一。对于华润三九CHC板块的发展,其董事长邱华伟在9月2日回应投资者称,未来将围绕“大品种-大品牌-大品类”的思路持续推进。
外延并购继续
业务范围延伸至更细分领域
作为华润系下重要的中药公司,华润三九一直秉承华润医药的外延并购战略。
继6月份昆药集团收购华润三九子公司,整合三七产业后;8月,华润三九入主天士力。据赛柏蓝不完全统计,截至目前,今年华润三九在收并购领域花费的金额已经在百亿元左右。
收购昆药对华润三九整体业绩的提升不言而喻,2023年上半年,华润三九在公告中称其业绩增长归因于CHC业务较快增长以及昆药集团自2023年1月19日起纳入合并报表范围。
而天士力对华润三九的发展会有怎样的帮助,在华润三九联合昆药集团举行2024年半年度业绩说明会上,华润三九董事、副总裁周辉透露,通过天士力和华润三九整合,有助于三九双终端协同发展战略的有效落地。其称,预计争取明年1季度完成天士力收购交易工作。
对于天士力的发展,华润三九称未来其将保持独立的上市公司地位。未来三九将推动天士力在心脑血管、肿瘤、消化代谢、中枢神经等核心领域业务保持增长。
天士力拥有心血管赛道的重磅产品复方丹参滴丸,并以此带动了养血清脑颗粒(丸)、芪参益气滴丸、注射用益气复脉、注射用丹参多酚酸等系列独家品种。米内网数据显示,近年来在中国三大终端六大市场心脑血管中成药厂家排名中,天士力均名列前茅。
华润三九在心血管赛道的野心,从2016年收购昆明圣火100%股权时已经显露。今年6月,华润三九将昆明圣火51%的股权划入昆药,解决血塞通软胶囊的同业竞争问题。
在心血管赛道,华润三九可以为天士力旗下的心血管赛道产品、渠道、市场发展铺垫。而华润三九继在胃肠、呼吸、皮肤类赛道领先外,又直接冲入了心血管赛道前列。
自2012年来,华润三九完成了超10项并购交易,将触角伸向了慢病管理、儿童维矿等不同领域。对于并购,华润三九依然通过渠道和终端优势,寻找优质标的并加速自身发展。
来源:赛柏蓝
作者:颜色

商务合作
130 6172 3098
zakk.cui@siqibest.com
加州普莱森顿2024年9月11日 /美通社/ — FlowPhysix™ Inc (前身为Expanse ICE )欣然宣布与3comma Medical/3comma Medical GmbH建立战略合作伙伴关系,后者将成为FLOWRUNNER™抽吸系统的国际商业合作伙伴。
3comma是一家国际商业化机构,在为早期医疗器械公司建立和扩展全球收入来源方面拥有深厚的专业知识。 FlowPhysix和3comma之间的这种合作关系将使美国以外的医生能够获得血栓切除术技术的新标准,从而使FlowPhysix能够专注于美国的商业化。
3comma管理合伙人兼Penumbra, Inc.前国际副总裁Marc Paris认为, FLOWRUNNER系统将对外设血栓切除术领域产生直接影响。 “我们可以迅速启动我们现有的国际商业基础设施,以加速FLOWRUNNER系统的采用。 我们有信心FlowPhysix将成为全球血栓切除术市场的下一个主要破坏者,我们很高兴能成为这一努力的一部分。”
FLOWRUNNER系统利用FlowPhysix专有技术克服了限制传统抽吸导管的特征性真空衰减。 抽吸导管通过抽吸鞘并从远端瓣膜向前推进,以直接向血栓施加完全且未腐烂的抽吸力。 然后将导管缩回到抽吸鞘中。 然后重复抽吸导管的伸展和缩回过程以完全抽吸凝块。 在每个循环中,血栓段被剪切并通过集成生理盐水冲洗通过导管有效排空。 该设备已成功去除大范围和大体积的血栓,并有效恢复血流。
“我们改变游戏规则的技术有可能改变目前的血栓切除术护理标准。 此次合作扩大了FlowPhysix的覆盖范围,为全球患者提供独特的解决方案。 我们坚信, 3comma久经考验的领导力和深厚的专业知识将推动国际商业成功,并提高公司的股东价值, ”FlowPhysix首席执行官Jeff Hopkins表示。
巴黎2024年9月11日 /美通社/ — ProductLife Group (PLG),作为生命科学行业监管、科学、合规及数字化转型咨询服务的全球供应商,欣然宣布收购Outcomes'10。Outcomes'10是西班牙顶尖的生命科学咨询公司,专注于提供患者准入和证据生成服务。
Outcomes'10成立于15年前,提供全面可靠的西班牙市场准入服务,涵盖定价与报销、健康经济学、结果研究以及真实世界数据生成等方面,是深受客户信赖的合作伙伴。 此次收购紧随PLG在意大利收购Intexo和在澳大利亚收购Commercial Eyes之后不到一年,将进一步助力PLG实现构建全球市场准入服务的宏伟蓝图。 这一扩展平台将发挥协同效应,为PLG的客户提供全面的准入服务,与公司在监管领域的其他咨询服务相辅相成。
Outcomes'10创始人兼首席执行官Luis Lizán:"加入PLG,对于Outcomes'10、我们的团队及客户来说,都是一个具有战略意义的里程碑。 这一合作伙伴关系与我们对专业精神和卓越运营的承诺相契合,它将使我们能够持续推动创新,并提供最前沿的解决方案。 成为PLG的一部分,我们不仅将强化战略关系,还将为个人和职业发展开拓更多机遇。 此外,随着健康科学领域的迅速创新和全球法规的不断演变,对国际市场准入服务的需求日益增长,这使得我们的合作显得尤为关键。 我们期待通过这一合作伙伴关系,进一步拓展全球业务范围并丰富我们的服务内容。"
Xavier Duburcq,作为PLG首席执行官,着重指出:"将Outcomes'10与PLG整合,不仅增强了我们的服务产品,还巩固了我们在欧洲市场的竞争优势。 Outcomes'10带来了对西班牙市场的深刻洞察,这将有助于调整我们的战略,以满足不同的区域需求。 这一联盟将使我们能够提供更细致有效的市场准入解决方案,确保我们能够精确地应对不同医疗保健系统的复杂性。"
PLG市场准入业务部门负责人Mariangela Prada表示:"收购Outcomes'10是我们全球市场准入团队成长和发展的又一重要里程碑,这要归功于他们扎实的专业知识和对西班牙市场的深入了解。"
上海2024年9月11日 /美通社/ — 优锐医药今日宣布完成恩司芬群(Ohtuvayre™)的ENHANCE – CHINA(NCT05743075)中国三期临床研究的患者招募,计划数量的患者全部成功入组。ENHANCE – CHINA研究项目是一项随机、双盲、安慰剂对照的三期临床试验,旨在评估恩司芬群(Ohtuvayre™)治疗中度至重度慢性阻塞性肺病(COPD)成人患者24周的疗效和安全性。ENHANCE – CHINA试验正在中国大陆的46家医院进行。
恩司芬群(Ohtuvayre™)是一款全球同类首创的磷酸二酯酶蛋白吸入型双靶点PDE 3/4抑制剂,双重抑制机理使其能够凭借单个化合物同时实现支气管扩张和抗炎效应。恩司芬群(Ohtuvayre™)可通过雾化器直接输送到肺部,不需要复杂的协调操作。
2024年6月,优锐医药合作伙伴Verona Pharma plc (Nasdaq: VRNA)宣布,美国食品药品监督管理局(FDA)已批准恩司芬群(Ohtuvayre™)用于维持治疗中重度COPD成人患者的新药上市许可申请。
优锐医药创始人、首席执行官Mark Lotter先生表示:"我们很高兴地宣布,关键的三期试验患者招募已经完成,这意味着我们最快将于2025年公布研究结果。我们欣喜于能够在今年早些时候获得美国FDA的成功批准后,有望为中国的COPD患者群体提供新的治疗方法。
Ohtuvayre™的推出将为中国COPD患者提供一个新的治疗选择,这是一个重要的里程碑。衷心地感谢试验的主要研究者钟南山教授和所有站点为完成试验、将创新药物进一步带给中国患者所做的贡献。"
Verona Pharma总裁兼首席执行官David Zaccardelli博士表示:"我们对优锐医药开展的ENHANCE – CHINA研究进展和患者招募完成感到非常高兴。我们期待将于2025年公布的研究结果以及将Ohtuvayre™带给数以千万的需要创新治疗方式的COPD患者的持续进展。"
2021年,优锐医药与Verona Pharma签订协议,获得在大中华区域(中国大陆、香港、澳门、台湾)开发与商业化恩司芬群(Ohtuvayre™)的独家权利。
苏州2024年9月11日 /美通社/ — 2024年9月10日,苏州博腾生物制药有限公司(简称博腾生物)宣布与微光基因(苏州)有限公司(以下简称"微光基因")达成战略合作,在基因编辑系统、基因编辑融合蛋白(Cas12蛋白)及非整合类病毒颗粒(VLP)递送系统等方面进行深度合作,共同推动基因编辑疗法的开发及商业化。
博腾生物建立了端到端的基因与细胞治疗CDMO平台,覆盖质粒、病毒载体、mRNA以及各类自体和异体免疫细胞。同时,博腾生物也非常注重研发和技术平台的建设投入,依托特有的CRISPR/Cas基因编辑体系以及高效稳定的细胞转染系统,已经成功帮助客户在不同细胞系实现基因编辑。微光基因已开发国际领先且全面的底层自主知识产权的基因编辑/表观遗传工具包和结构独创且具备底层专利的VLP递送系统,可实现体外/体内的高效目的基因编辑或长效目的基因抑制以及高效且特异的蛋白、mRNA或RNP蛋白复合物递送。
本次双方达成战略合作,这将进一步拓展博腾生物的技术平台能力,借助微光基因强大的基因编辑工具及VLP递送系统,从平台创新到项目交付,从CRO到CDMO,拓展基因编辑技术在细胞与基因疗法的应用,让好药更早惠及大众。
微光基因首席执行官胡洋博士表示:"我们很高兴与博腾生物达成合作。微光基因自主专利的CRISPR/Cas编辑器及VLP递送系统在细胞基因治疗领域上呈现出优秀的效率及优良的安全性。双方的合作将发挥协同效应,加速微光自主专利的CRISPR/Cas编辑器、碱基编辑器、表观编辑器和VLP递送系统的研究和应用,为中国细胞基因治疗的研发和产业化做出贡献。"
博腾股份副总经理、博腾生物首席财务官陈晖表示:"我们非常高兴能与微光基因达成战略合作。微光基因在新型基因编辑工具及递送系统方面拥有Cas蛋白、碱基编辑器、表观编辑器和VLP递送系统等基础知识产权,平台与技术的创新给我们留下了深刻的印象。博腾生物致力于在基因与细胞治疗领域为全球客户提供端到端的CDMO服务,并协同产业链上下游企业实现合作共赢。我们相信博腾生物和微光基因能够达成良好的伙伴关系,并将新型基因编辑技术的合作扩展到尚被满足的新领域,共同赋能细胞与基因疗法的开发和商业化。"
济南2024年9月10日 /美通社/ — 9月07-10日,肺癌领域的年度盛会世界肺癌大会(WCLC)在美国圣迭戈举办。当地时间8日,齐鲁制药伊鲁阿克片(启欣可®)在克唑替尼耐药的间变性淋巴瘤激酶(ALK)阳性非小细胞肺癌患者中II期临床试验(INTELLECT研究)的最新数据以壁报形式展示。
伊鲁阿克是由齐鲁制药研发的新一代ALK/ROS1激酶抑制剂,2023年6月获批用于治疗既往接受过克唑替尼治疗后疾病进展或对克唑替尼不耐受的ALK阳性的局部晚期或转移性非小细胞肺癌患者,并于今年1月获批用于一线治疗ALK阳性的非小细胞肺癌患者。
本研究的牵头研究者为中国医学科学院肿瘤医院的石远凯教授。INTELLECT研究的目的是评价伊鲁阿克在克唑替尼耐药的ALK阳性晚期非小细胞肺癌患者中的疗效和安全性。该INTELLECT研究结果曾于2023年在著名期刊《BMC Medicine》上发表,本次WCLC会议报告的是延长两年随访时间的更新数据。
本研究共入组146例受试者,截至2023年12月29日,中位随访时间为42.41个月,中位总生存期(OS)达到41.79个月。研究者评价的客观缓解率(ORR)和疾病控制率(DCR)分别为63.7%和94.5%,中位缓解持续时间(DoR)和无进展生存期(PFS)分别为14.06个月和14.55个月。
根据RECIST v1.1评价标准,基线有中枢神经系统转移亚组(90例)的ORR和DCR分别为55.6%和93.3%,中位DoR和PFS均为17.25个月,中位OS为43.01个月。
根据RANO-BM评价标准,在90例基线有中枢神经系统转移的患者中,有17例(18.9%)达到颅内完全缓解(CR)。在42例基线有颅内可测量病灶的受试者中,颅内客观缓解率(iORR)和颅内疾病控制率(iDCR)分别为64.3%和95.2%。
安全性方面,治疗相关不良事件(TRAE)的发生率为93.8%(137例),3级或4级TRAE的发生率为30.8%(45例)。最常见的TRAE为天门冬氨酸氨基转移酶升高(45.2%)、高胆固醇血症(37.7%)和丙氨酸氨基转移酶升高(37.0%),未发现新的安全性信号。
INTELLECT研究的长期随访结果显示,伊鲁阿克为克唑替尼耐药的ALK阳性晚期非小细胞肺癌患者带来了OS获益,且无新的安全性信号。
Beamion LUNG-1 Ib期研究达到了主要终点,研究数据显示,客观缓解率(ORR)为66.7%,这一结果由中央独立盲态审查(BICR)评估。[1]
在脑转移患者中也观察到初步疗效,颅内缓解率为33%,疾病控制率(DCR)达到74%。
Zongertinib 整体耐受性良好,主要为轻度且可控的治疗相关不良事件(TRAE),因毒性导致的停药率较低,仅为3%。
截至数据截止时,仍有三分之二的患者在接受治疗。更为成熟的数据,包括无进展生存期(PFS)和缓解持续时间(DoR),将在今年晚些时候公布。
上海2024年9月10日 /美通社/ — 今日,勃林格殷格翰公布Beamion LUNG-1试验Ib期队列1主要分析结果,评估Zongertinib(BI 1810631)在携带人表皮生长因子受体-2(HER2)突变阳性晚期非小细胞肺癌(NSCLC)经治患者中的疗效。Zongertinib在队列1患者中展现出显著的客观缓解率(ORR),且整体耐受性良好。该结果在国际肺癌研究协会(IASLC)2024世界肺癌大会(WCLC)主席研讨会上公布,并纳入2024年WCLC官方报道。
截至2024年5月,共有132名患者接受了每日120 mg或240 mg的Zongertinib治疗(n=75/n=57)。在中央独立盲态审查(BICR)评估下,确证客观缓解率(ORR)为66.7%,97.5% CI (53.8–77.5), (p<0.0001),队列1(120mg;n=75)的主要终点达成。根据研究者评估,所有剂量组中94%的患者观察到了不同程度的肿瘤缩小。试验设计包括剂量递增,以确定该患者群体中Zongertinib的最佳剂量。患者以1:1的比例随机分配至120mg(n=58)或240mg(n=55)组。在中期无效性分析后,选择了120mg作为在队列1中进一步评估的剂量,并额外招募了17名患者。在1:1随机分组的试验部分,接受Zongertinib每日120mg治疗的患者显示出72.4%的缓解率,接受每日240mg治疗的患者中缓解率为78.2%,且疾病控制率(DCR)分别为95%和100%。
Ib期队列1的数据还初步显示出Zongertinib对脑部病变的活性。根据独立中央盲态审查(BICR)和RANO-BM(神经肿瘤反应评价-脑转移)标准,在无症状脑转移的患者中,33%(120mg;n=27)和40%(240mg;n=25)的患者获得了确认的客观缓解,疾病控制率(DCR)分别为74%和92%。中枢神经系统是非小细胞肺癌(NSCLC)常见的转移部位,且与预后不良和生活质量下降密切相关。[2]在确诊时,约30%的HER2突变阳性的NSCLC患者存在脑转移。[3]
"这些新数据可能为未来HER2突变阳性的非小细胞肺癌患者的治疗带来积极的消息,"该试验的主要研究者、德克萨斯大学MD安德森癌症中心的John Heymach博士(MD, PhD)表示。"虽然这些突变较为罕见,但它们是部分非小细胞肺癌病例中的关键驱动因素,而现有的治疗选择极为有限。患有此类癌症的患者通常预后较差,约50%的患者对一线治疗有反应,只有约20%的患者对二线治疗产生反应。"[4], [5], [6], [7]
Zongertinib是一种正在开发中的口服HER2酪氨酸激酶抑制剂(TKI),目前正在研究其在HER2突变阳性的晚期非小细胞肺癌(NSCLC)患者中的疗效。Zongertinib的设计旨在避免影响野生型EGFR,从而减少相关毒性。一项全球性III期临床试验Beamion LUNG-2,正在评估Zongertinib相对于标准治疗作为晚期HER2突变阳性NSCLC患者一线治疗的效果,该试验目前正在招募患者。
勃林格殷格翰董事会成员、创新事业部负责人Paola Casarosa表示:"Zongertinib的疗效和耐受性有潜力成为未来HER2突变肺肿瘤患者治疗前景中的一种。Zongertinib是我们在探索和开发新疗法中采用科学思维方法的完美典范。勃林格致力于为癌症患者提供突破性疗法,我们非常期待推进zongertinib的临床项目。"
Zongertinib 在120mg和240mg剂量下总体耐受性良好,未发生与治疗相关的死亡事件,且导致剂量减少的不良事件发生率(11%)和停药率为(3%)均较低。未观察到新的安全信号或与治疗相关的间质性肺疾病(ILD),3级或以上的治疗相关不良事件(TRAEs)发生率分别为17%(120mg)和19%(240mg)。最常见的治疗相关不良事件为1级或2级腹泻(分别为43%和11%)以及1级或2级皮疹(分别为19%和8%)。
试验数据仍在逐步成熟,截至数据截止时,仍有三分之二的缓解患者仍在继续接受治疗,无进展生存期(PFS)和缓解持续时间(DoR)的数据将在即将到来的会议上公布。