导言
Introduction
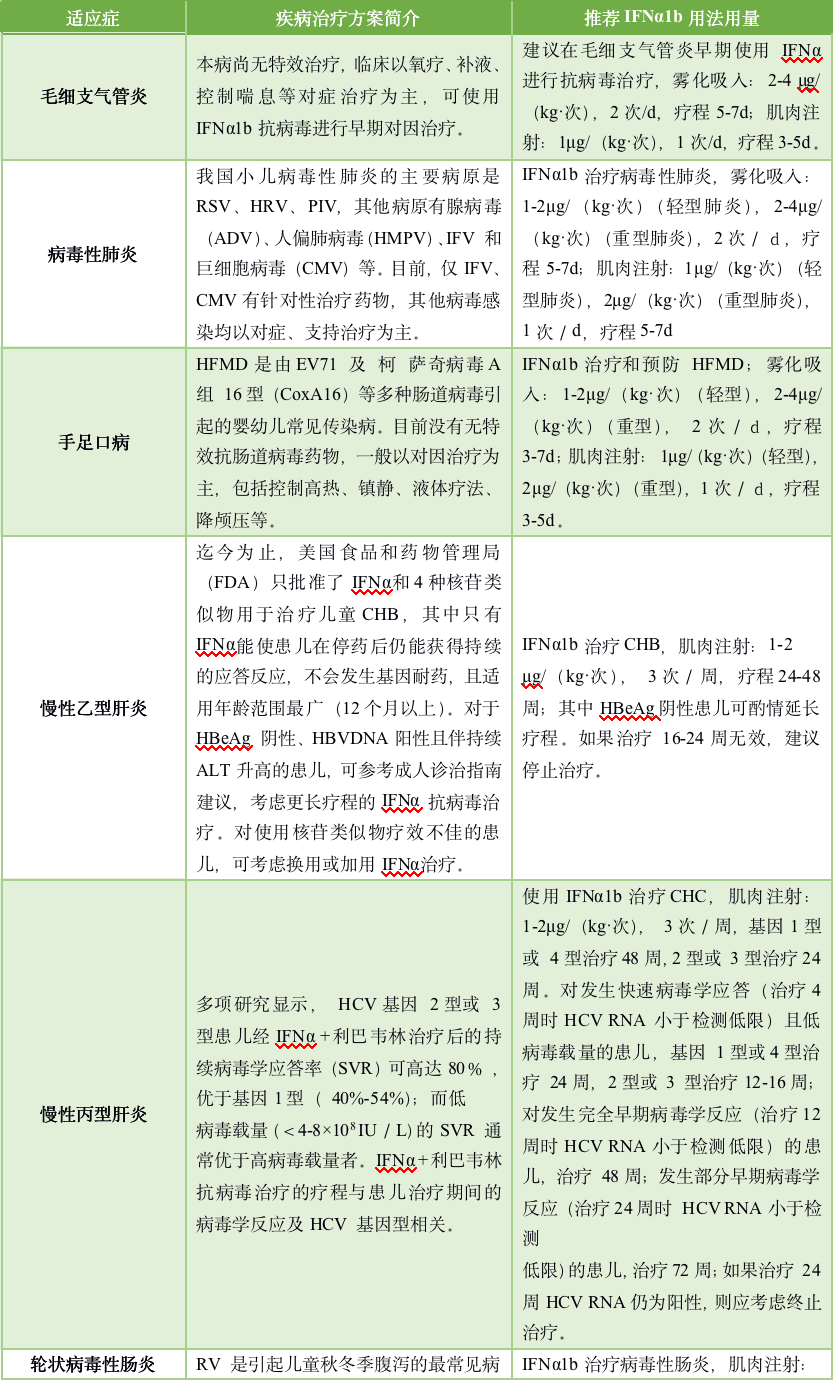
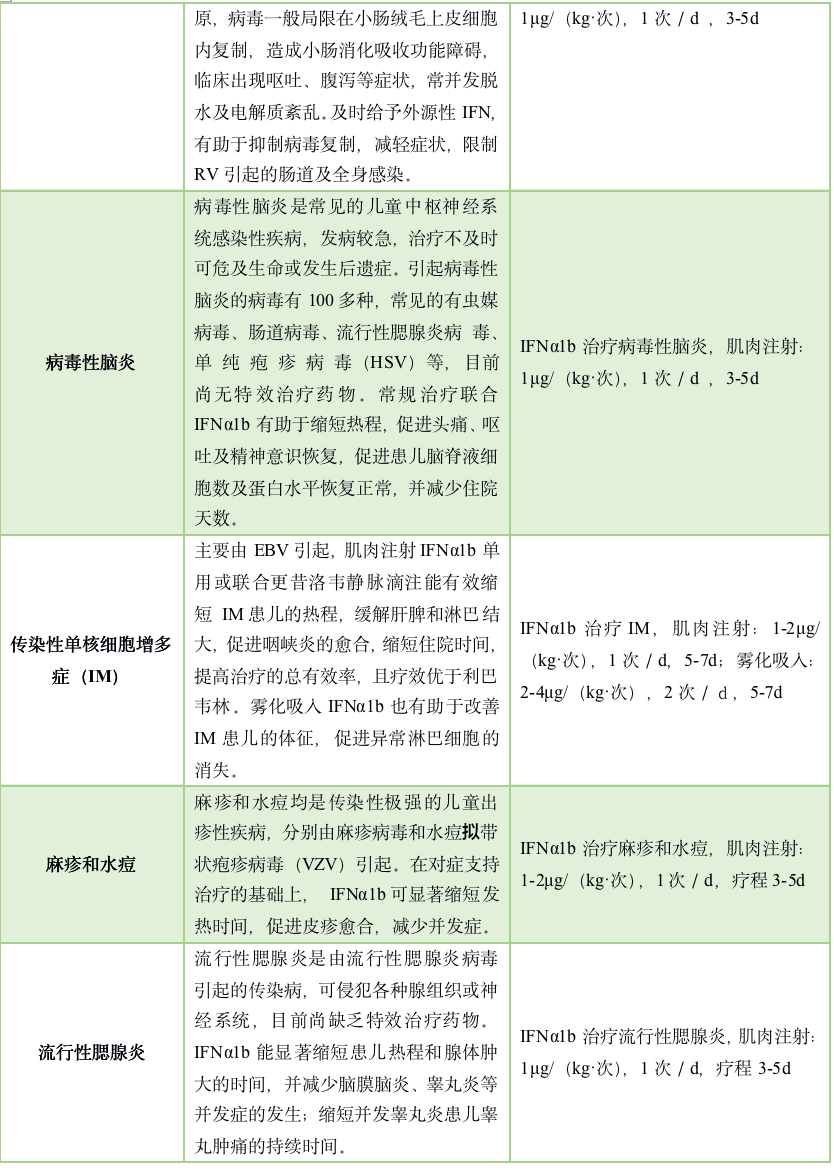
HBV感染是导致肝硬化和肝癌等慢性肝病的主要原因。据估计,目前我国全人群HBsAg 流行率为5%~6%,慢性HBV 感染者约7 000 万例,其中CHB 患者2 000 万~3 000 万例[1]。尽管HBV 相关疾病所致的医疗负担很重,CHB的治疗方法也不断发展,但大多数HBV感染者对自身感染状况知晓率仍较低,导致部分患者就医时已经进展到疾病晚期。因此CHB的早期筛查、诊断及后续的关怀管理是防治的关键环节。此基层乙肝诊疗指南由中华医学会牵头撰稿,旨在对基层慢性乙肝的诊疗跟踪做进一步指导说明。
一、
概述
1. 定义:
慢性乙型肝炎病毒(HBV)感染:指乙型肝炎表面抗原(HBsAg)和/或HBV 脱氧核糖核酸(HBV DNA)阳性6个月以上。
慢性乙型肝炎(CHB):指由HBV持续感染6个月以上引起的慢性肝脏炎症性疾病。
2. 传播
HBV主要经母婴、血液和性接触传播。在我国实施新生儿乙型肝炎疫苗免疫规划后,母婴传播已大幅度减少。HBV不经过呼吸道和消化道传播,因此日常学习、工作或生活接触不会传染HBV。
3. 自然史和发病机制
CHB 的发病机制较为复杂,迄今尚未完全阐明。大量研究表明,HBV不直接杀伤肝细胞,而是通过免疫应答导致肝细胞损伤及炎症坏死,而炎症坏死的持续存在或反复出现,是慢性HBV感染者进展为肝纤维化、肝硬化甚至肝细胞癌(HCC)的重要因素。

二、
检测
检测方法
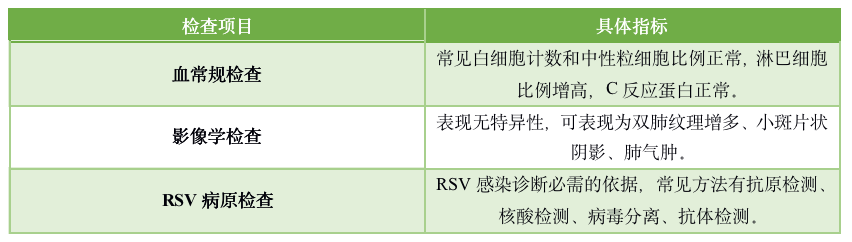
1. HBV血清学检测:目前为HBV 感染的首选检测方法
2. HBV DNA定量检测:主要用于判断HBV复制水平,用于抗病毒治疗适应证的选择和疗效判断。
3. 生物化学检查[5]:包括丙氨酸转氨酶(ALT)和天冬氨酸转氨酶(AST)、血清胆红素、外周血常规检测、甲胎蛋白(AFP)等。
4. 肝纤维化无创性诊断检查: APRI 评分可用于肝硬化的评估;FIB⁃4:FIB⁃4基于ALT、AST、血小板和患者年龄来计算,可用于CHB患者肝纤维化的诊断和分期;TE作为一种较为成熟的无创检查,其优势为操作简便、可重复性好,能够比较准确地识别轻度肝纤维化和进展性肝纤维化或早期肝硬化;


检测策略
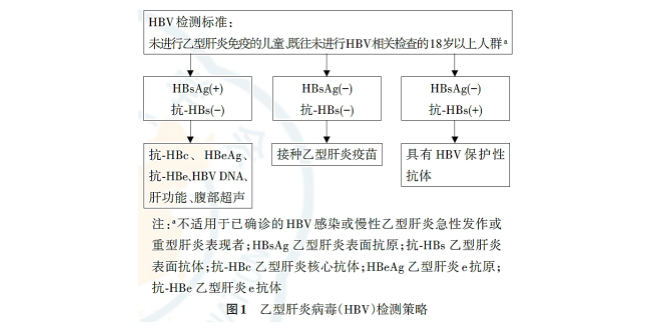
建议对未进行乙型肝炎免疫的儿童以及既往未进行HBV相关检查的18岁以上人群在健康体检或临床就诊时进行HBsAg 和抗⁃HBs 检测,如HBsAg 阳性,提示存在HBV感染,再进一步检查HBeAg、抗⁃HBe、抗⁃HBc、抗⁃HBc IgM、HBV DNA、肝功能和腹部超声。
三、
诊断
慢性HBV感染分类
1. 慢性HBV 携带状态:又称HBeAg 阳性慢性HBV感染。多为年龄较轻的处于免疫耐受期的HBsAg、HBeAg和HBV DNA阳性者,1年内连续随访3次,每次至少间隔3个月,均显示血清ALT 和AST 在正常范围,HBV DNA 通常处于高水平(>2×107 IU/ml),血清HBsAg 较高(通常>1×104 IU/ml),肝组织学检查无明显炎症坏死或纤维化。
2. HBeAg阳性CHB:患者处于免疫清除期。血清HBsAg 阳性,HBeAg 阳性,HBV DNA 阳性(通常>2×104 IU/ml),ALT 持续或反复异常,或肝组织学检查有明显炎症坏死和/或纤维化。
3. 非活动性HBsAg携带状态:又称HBeAg阴性慢性HBV感染。为免疫控制期,血清HBsAg阳性、HBeAg阴性、抗⁃HBe阳性或阴性,HBV DNA<2×103 IU/ml,HBsAg<1×103 IU/ml,1年内连续随访3次以上,每次至少间隔3个月,ALT和AST均在正常。范围。影像检查无肝硬化征象,肝组织学检查显示组织学活动指数(HAI)评分<4或根据其他的半定量计分系统判定病变轻微。
4. HBeAg阴性CHB:为再活动期。血清HBsAg阳性,HBeAg 持续阴性,HBV DNA 阳性(通常≥2×103 IU/ml),ALT持续或反复异常,或肝组织学有肝炎病变。
5. 隐匿性HBV感染(OBI):其定义为血清HBsAg 阴性,但血清和/或肝组织中HBV DNA阳性。除HBV DNA阳性外,80% 患者可有血清抗⁃HBs、抗⁃HBe 和/或抗⁃HBc阳性,称为血清学阳性OBI;1%~20%的OBI患者的血清学标志物均为阴性,称为血清学阴性OBI。诊断主要通过HBV DNA 检测,尤其对抗⁃HBc持续阳性者。其发生机制尚不完全明确。
6. 乙型肝炎肝硬化:乙型肝炎肝硬化的诊断符合下列(1)和(2)者为病理学诊断,符合(1)和(3)者为临床诊断。
1) 病史及血液检查有HBV现症感染(HBsAg阳性),或有明确的慢性HBV 感染史(既往HBsAg阳性>6个月,目前HBsAg阴性、抗⁃HBc阳性)且除外其他病因者。
2) 肝脏活组织检查病理学符合肝硬化表现。
3) 符合以下5项中的2项及以上者,并排除非肝硬化性门静脉高压者:
①影像学检查显示肝硬化和/或门脉高压征象。
②内镜检查显示食管胃底静脉曲张。
③肝脏TE测定显示肝脏硬度符合肝硬化。
④血生物化学检查显示白蛋白水平降低(<35 g/L)和/或凝血酶原时间延长(较对照延长>3 s)。
⑤外周血常规检查显示血小板计数<100×109/L等。
四、
转诊
当患者出现以下症状,建议转诊:
1.紧急转诊:当CHB患者出现急性发作,需要住院治疗时,应考虑及时紧急转诊。
1) CHB急性发作:患者有明显的腹胀、纳差、黄疸等明显的肝炎临床症状,肝功能化验明显异常,例如ALT>5倍ULN,或1周内血清总胆红素和ALT急剧升高。
2) 重型肝炎(肝衰竭):加强对重症肝炎的识别,如CHB患者出现极度乏力、食欲明显降低、重度腹胀等症状,神经、精神症状(性格改变、烦躁不安、嗜睡、昏迷等肝性脑病表现),有明显出血、扑翼样震颤等现象时,应紧急转诊。
2.普通转诊:
(1)初诊肝硬化、HCC患者建议转诊专科。
(2)免疫抑制剂治疗或癌症化疗的患者。
(3)CHB 经抗病毒治疗6个月,ALT仍持续异常和/或HBV DNA阳性患者,应转诊到专科,考虑药物治疗应答不佳,并寻找肝功异常其他原因。
(4)肾功能不全患者。
(5)HBV合并HCV、HIV感染。
(6)妊娠期女性(HBV DNA 阳性者)。
(7)青少年及儿童患者。
(8)其他:由于其他因素无法处理者。
五、
这个可以是个序号标题
Ø 抗病毒治疗的适应证
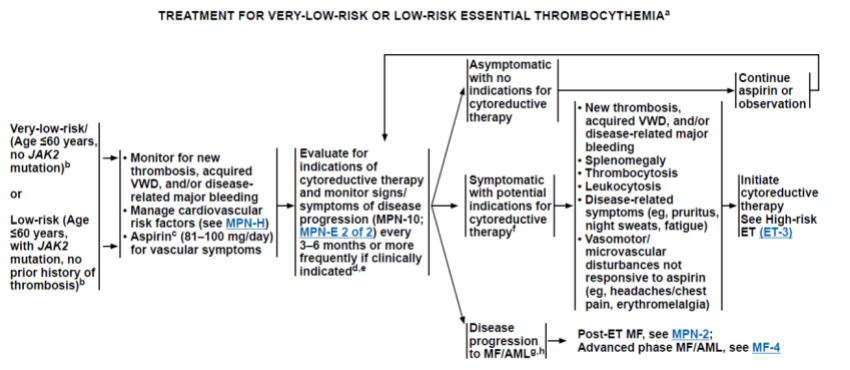
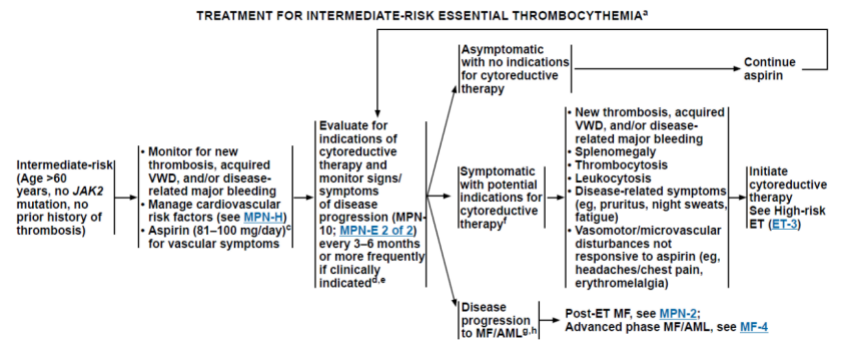
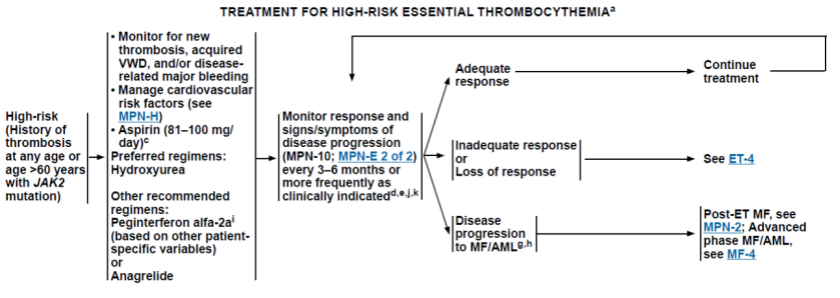
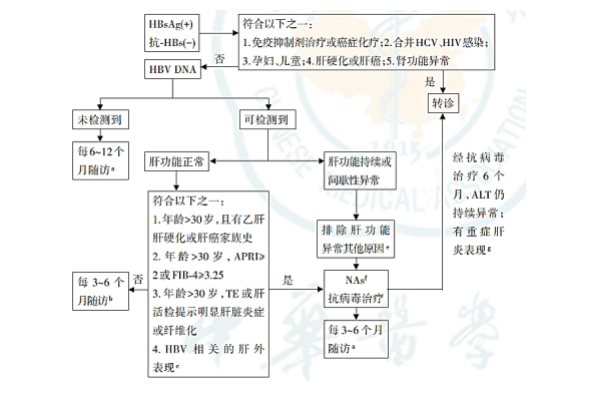
抗病毒治疗目前主要依据血清HBV DNA、ALT水平和肝脏疾病严重程度,同时需结合年龄、家族史和伴随疾病等因素,综合评估患者疾病进展风险,决定是否需要启动抗病毒治疗。
1. 血清HBV DNA阳性的CHB患者:若ALT持续异常(>1倍ULN)且排除其他原因导致的ALT升高,均应考虑开始抗病毒治疗。导致ALT升高的其他原因包括:其他病原体感染、药物性肝损伤、酒精性肝炎、脂肪性肝炎、自身免疫性肝炎、全身系统性疾病累及肝脏等其他因素。同时也应排除应用保肝降酶药物后ALT暂时性正常。
2. 肝硬化:代偿期肝硬化者,无论ALT 和HBeAg状态,只要HBV DNA可检测到,均建议积极抗病毒治疗。对失代偿期肝硬化者,只要HBsAg阳性者,均建议抗病毒治疗。
3. 血清HBV DNA 阳性、ALT正常者有以下情形之一者,疾病进展风险较大,建议抗病毒治疗:
1) 肝组织学存在明显的肝脏炎症(G2级及以上)或肝纤维化(S2级及以上)。
2) ALT 持续正常(每3 个月检查1 次,持续12个月),有肝硬化或肝癌家族史且年龄>30岁者。
3) ALT 持续正常(每3 个月检查1 次,持续12个月),无肝硬化或肝癌家族史,年龄>30岁者,建议行无创肝纤维化检查或肝组织学检查,存在明显肝脏炎症或纤维化者。
4) ALT 持续正常(每3 个月检查1 次,持续12个月),有HBV相关的肝外表现者(肾小球肾炎、血管炎、结节性多动脉炎、周围神经病变等)。
Ø 抗病毒治疗的药物
1) Nas治疗:恩替卡韦、富马酸替诺福韦酯、富马酸丙酚替诺福韦为首选的NAs药物,可强效抑制病毒复制,改善肝脏炎症,安全性较好,总体的耐药率发生较低,长期应用可显著减低肝硬化并发症和HCC的发生率,减低肝脏相关和全因死亡率。NAs总体安全性和耐受性良好,但在临床应用中确有少见、罕见严重不良反应的发生,如肾功能不全(服用阿德福韦酯或富马酸替诺福韦酯)、低磷性骨病(服用阿德福韦酯或富马酸替诺福韦酯)、肌炎或横纹肌溶解(服用替比夫定或拉米夫定)、乳酸酸中毒等(服用恩替卡韦和替比夫定),应引起关注。建议治疗前仔细询问相关病史,对肾功能进行评估,以减少风险。治疗中根据病情需要,定期检测血常规、血清肌酐和肌酸激酶(CK)等,必要时可检测血磷、乳酸和肾小管功能,若出现血肌酐、CK或乳酸脱氢酶明显升高,并伴相应临床表现者如全身情况变差、明显肌痛、肌无力等症的患者,应及时调整抗病毒方案,并给予积极的相应治疗干预。
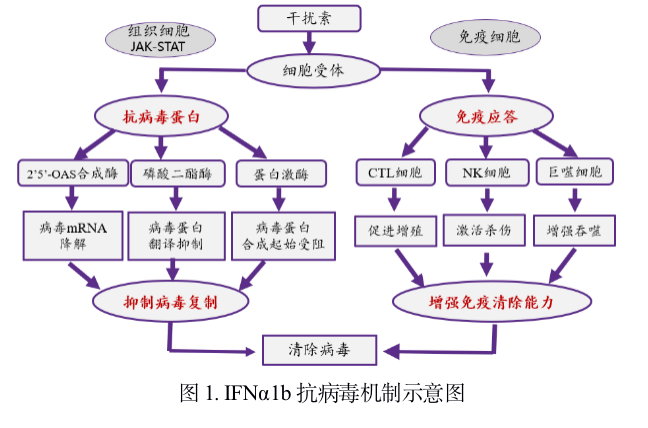
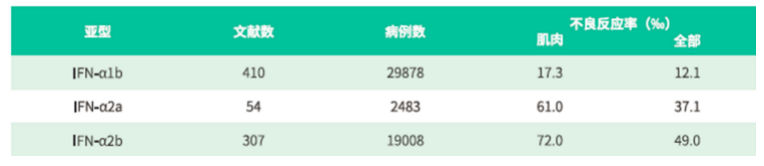
2) 干扰素⁃α治疗:我国已批准聚乙二醇干扰素(Peg⁃IFN⁃α)和普通干扰素(IFN⁃α)用于治疗慢性乙型肝炎,前者仅需1周注射1次。由于干扰素的治疗较复杂,建议专科治疗和管理。
六、
基层随访
1) 加强HBV检测,及早发现HBV感染者鼓励所有医疗机构、社区进行HBV检测服务,并制定和实施有关提高HBV检测率和上下联动管理的策略。一旦确诊慢性HBV感染者,即纳入慢性HBV感染分级管理,初次评估要询问患者的肝硬化和HCC家族史、饮酒史以及免疫接种史,并定期对患者评估和随访。根据各个地区和基层的条件及能力,扩展服务内容,建立起主要的诊断、治疗在医院,筛查、随访、管理在基层的上下联合管理系统。
2) 慢性HBV 携带状态和非活动性HBsAg携带状态患者的监测建议每6~12个月进行血常规、生物化学、HBV血清学标志物、AFP、腹部超声和肝纤维化无创诊断技术等检查,必要时进行肝活组织检查,若符合抗病毒治疗指征,及时启动治疗。
3) 抗病毒治疗中的监测定期监测治疗疗效、用药依从性,以及耐药情况和不良反应。应用NAs类药物患者,建议每3~6个月监测血常规、肝脏生物化学指标、HBV DNA 定量和HBV血清学标志物、肝脏硬度值测定;对于无肝硬化者建议每6个月1次腹部超声检查和AFP等,对于有肝硬化者则建议最好每3个月1次;必要时做增强CT或增强MRI 以早期发现HCC。服用富马酸替诺福韦酯治疗者,每6~12 个月监测1 次血磷和肾功能。
原文链接:慢性乙型肝炎基层诊疗指南(实践版·2020) (lcgdbzz.org)
参考文献:
[1] Liu J, Liang WN, Jing WZ, et al. Countdown to 2030: eliminating hepatitis B disease, China[J]. Bull World Health Organ, 2019, 97(3): 230‑238. DOI: 10.2471/BLT.18.219469.
[2] Terrault NA, Lok A, McMahon BJ, et al. Update on prevention, diagnosis, and treatment of chronic hepatitis B: AASLD 2018 hepatitis B guidance[J]. Hepatology, 2018, 67(4):1560‑1599. DOI: 10.1002/hep.29800.
[3] Hui CK, Leung N, Yuen ST, et al. Natural history and disease progression in Chinese chronic hepatitis B patients in immune‑tolerant phase[J]. Hepatology, 2007, 46(2):395‑401. DOI: 10.1002/hep.21724.
[4] Schillie S, Vellozzi C, Reingold A, et al. Prevention of Hepatitis B Virus Infection in the United States: Recommendations of the Advisory Committee on Immunization Practices[J]. MMWR Recomm Rep, 2018, 67(1):1‑31. DOI: 10.15585/mmwr.rr6701a1.
[5] 中国肝炎防治基金会, 中华医学会感染病学分会, 中华医学会肝病学分会和中国研究型医院学会肝病专业委员会. 瞬时弹性成像技术诊断肝纤维化专家共识(2018 年更新版) [J]. 中华肝脏病杂志, 2019, 27(3): 182‑191. DOI:10.3760/cma.j.issn.1007‑3418.2019.03.004.