日前,阿斯利康度伐利尤单抗联合曲麦利尤单抗(即STRIDE方案)在中国获批用于晚期或不可切除的肝细胞癌(HCC)成人患者的一线治疗。此外,度伐利尤单抗亦获批单药治疗作为晚期或不可切除的肝细胞癌(HCC)成人患者的一线治疗。
“肝癌一线”早已挤满对手,从罗氏的“T+A”到信达的“信迪利+贝伐”,再到恒瑞的“双艾”,阿斯利康此时入场,究竟底气何在?
60亿美元大单品的“中国焦虑”
过去五年,中国肝癌一线治疗经历了三轮迭代。第一轮是索拉非尼和仑伐替尼的单药时代;第二轮是“免疫+抗血管”方案的崛起,罗氏的“T+A”(阿替利珠单抗+贝伐珠单抗)在2020年全球获批,2021年进入中国;第三轮是国产方案的爆发,信达生物的信迪利单抗联合贝伐珠单抗类似物(SB方案)在2022年获批,恒瑞的“双艾”(卡瑞利珠单抗+阿帕替尼)紧随其后。到2024年,肝癌一线已经形成了“多强并立”的格局,且多数方案已进入医保。而阿斯利康的STRIDE方案此时在国内获批,整整落后了第一梯队3-5年。
度伐利尤单抗在全球的核心战场一直是肺癌,从III期不可切除NSCLC的PACIFIC方案,到可切除NSCLC的围手术期治疗,再到局限期和广泛期小细胞肺癌,阿斯利康在这四个肺癌场景中构建了坚实的护城河。2025年,度伐利尤单抗全球销售额达60.63亿美元(同比增长28.54%),其中绝大部分来自肺癌,肝癌只是其产品管线中的“后来者”。
尽管度伐利尤单抗在中国的肺癌适应症早已获批,但国产PD-1通过医保谈判已将年治疗费压至几万元区间,市场份额增长空间有限。阿斯利康需要为这个60亿美元大单品在中国找到第二增长支点,而肝癌正是这块拼图。
去年7月,阿斯利康中国成立了独立的消化道肿瘤事业部,将肝癌、胃癌、食管癌等打包作战,而这个时间恰好是该联合疗法的HIMALAYA研究中国队列数据在CSCO年会上发布前后。也就是说,阿斯利康为布局该赛道筹备了良久。此次获批,是为了补位度伐利尤单抗在中国产品组合中的结构性缺口。
用一针就够的CTLA-4
BMS的“O+Y”早在多年前就验证了CTLA-4+PD-1的协同效应。伊匹木单抗(Yervoy)作为全球首个获批的CTLA-4抗体,其标准方案是每3周一次、连续4个周期,通过持续阻断CTLA-4可以维持T细胞活化状态。然而,近十年临床实践发现:多周期给药的免疫相关不良事件(irAE)发生率显著升高,而疗效并未等比增加。
以肝癌为例,CheckMate-040研究中“O+Y”方案的3/4级治疗相关不良事件发生率约为36%,其中肝炎、结肠炎、垂体炎等严重irAE导致相当比例的患者中断治疗。这也是“O+Y”方案在全球多个瘤种中获批(2020年3月获FDA加速批准),但在中国肝癌一线获批(2025年3月获得NMPA批准)则晚得多的重要原因之一,NMPA对CTLA-4抑制剂的安全性审查极为严格。
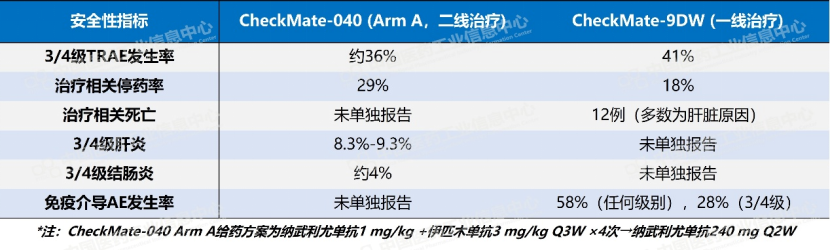
数据来源:Pharma ONE药物研发大数据平台-全球临床试验板块,中国医药工业信息中心
而STRIDE方案中,曲麦利尤单抗只需一针,300mg单次启动剂量,后续全交给度伐利尤单抗每4周一次维持。阿斯利康的免疫学逻辑是,CTLA-4抑制剂只需要在治疗初期“启动”T细胞扩增,后续T细胞功能维持可交由PD-L1抑制剂,不需要反复激活CTLA-4通路。
该逻辑的验证来自全球III期临床研究HIMALAYA,中国队列中位OS达25.3个月,3年OS率40.6%;且STRIDE方案的3/4级治疗相关不良事件发生率仅24.1%,远低于“O+Y”的历史数据,免疫介导的肝炎发生率仅2.3%。对中国75%伴有乙肝感染的肝癌患者来说,“肝友好”的安全性特征,是监管机构敢于放行的关键。
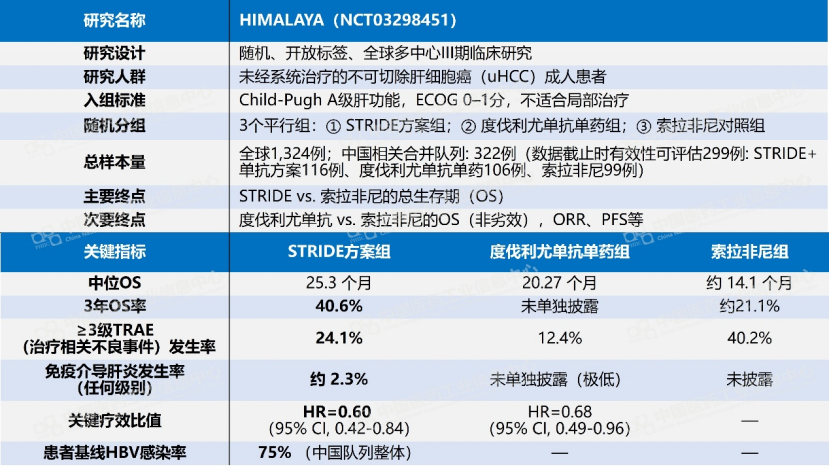
HIMALAYA研究:全球及中国队列基本信息汇总表,中国合并队列(中国大陆+中国香港+中国台湾):核心疗效与安全性数据
数据来源:Pharma ONE药物研发大数据平台-全球临床试验板块,中国医药工业信息中心
阿斯利康“一针策略”绕开CTLA-4多周期毒性陷阱,以单次给药重塑临床开发逻辑,CTLA-4,一次足矣。
STRIDE的优势,藏在门诊处方里
当前肝癌一线主流方案,“T+A”、信迪利+贝伐、“双艾”都离不开抗血管生成药物(贝伐珠单抗或TKI)。尽管疗效毋庸置疑,但临床管理负担也显而易见,贝伐珠单抗需要监测血压、尿蛋白、出血风险,TKI需要关注手足皮肤反应、腹泻、高血压等。对基层医院来说,这些都需要更高的住院频率和更复杂的随访流程。
STRIDE作为目前已获批的“纯双免疫、无抗血管”方案之一,有着门诊处方管理的便捷性。除了第一剂(曲麦利尤单抗+度伐利尤单抗)需要在院观察,后续每4周一次的度伐利尤单抗单药输注,在成熟的门诊化疗中心即可完成。不需要频繁监测血压、尿蛋白,不需要担心出血风险,不需要处理手足皮肤反应。对于肝功能储备尚可、没有活动性出血风险的患者,STRIDE方案可以做到“纯门诊管理”。
约20%-30%的晚期肝癌患者因食管胃底静脉曲张、高血压病史或凝血功能障碍,不适合使用贝伐珠单抗。该群体过去只能选择索拉非尼或仑伐替尼单药。STRIDE方案为他们提供了全新、不需要抗血管的强效选择。而对于适合抗血管治疗的患者,STRIDE方案可以提供“轻量化”的替代方案,帮患者减少住院次数、降低随访负担。
当然,挑战同样存在。国内临床医生对CTLA-4抑制剂的处方经验有限,市场教育需要时间。国产CTLA-4(如信达IBI310)的价格压力也不容小觑。
不卷入价格战,用“门诊友好”方式,争取被抗血管方案排除在外的患者,以及不愿被频繁监测拖累生活质量的患者。在红海里,不是只有疗效最高的人才能赢,有时最“不麻烦”的那个,也能获得处方。










