
历9弥新,全球首个口服选择性HDACi西达本胺自问世以来,一直以匠人之心根植表观遗传领域,探索之路漫不止,开拓之星火不熄,2023年第28届EHA年会中公布了多项表观遗传及HDACi西达本胺相关研究结果,值此之际,【EPI开拓者—2023 EHA HDACi相关进展】线上会议于6月8日召开,会议特邀北京大学肿瘤医院朱军教授和四川大学华西医院牛挺教授担任会议主席,以及多名血液肿瘤领域知名专家学者,细研国内外学者在表观遗传学征程上坚实脚印,洞悉表观世界,追溯疾病本源,不断对领域进展进行深度思考。
会议伊始,会议主席朱军教授和牛挺教授致辞道,正值EHA大会第一天,非常高兴作为大会主席担任“领航”任务,与大家相聚线上,针对第28届EHA会议中最新公布的表观遗传及HDACi相关研究进行探讨和学习,为此领域贡献更多属于中国学者的智慧。
首都医科大学附属北京同仁医院王亮教授以《2023 EHA Meeting 西达本胺/ HDACi 相关研究进展》为题,对多项西达本胺在T细胞淋巴瘤和白血病中应用的研究进行了详细解读和分享。
研究1:西达本胺与阿扎胞苷联合CHOP治疗初治外周T细胞淋巴瘤(PTCL)的2期临床研究
研究亮点:双表观联合CHOP诱导治疗PTCL缓解率高,尤其是AITL亚型,不仅为ASCT创造更多机会,也为长期无进展生存打下基础。
一项前瞻性、单中心、单臂、II期试验的中期分析纳入23例初治PTCL患者,旨在探索西达本胺与阿扎胞苷和CHOP联合诱导治疗达完全缓解/部分缓解(CR/PR)后,进行自体造血干细胞移植(ASCT)以及西达本胺维持治疗的有效性和安全性。研究结果显示,诱导治疗后,总缓解率(ORR)为84.2%,CR率为42.1%。ASCT后患者(n=8)的评估显示,ORR为100%,CR率为75%。研究者还注意到,12例可评估的血管免疫母T细胞淋巴瘤(AITL)患者在诱导结束时,ORR为92.3%,CR率为61.5%。安全性方面,中性粒细胞减少是最常见的不良反应,但可控制。本研究证明,西达本胺与阿扎胞苷+CHOP治疗PTCL是可行和安全的。特别是在AITL亚型的诱导治疗阶段获得了较高的CR率。

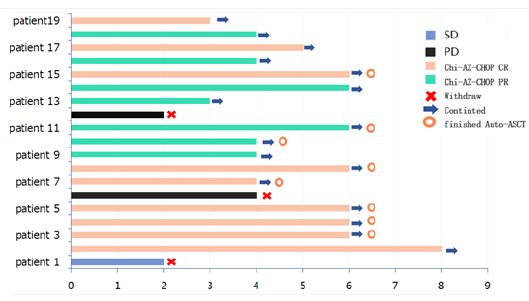
图1. 患者缓解情况



研究2:PTCL患者使用西达本胺的中国真实世界研究
研究亮点:通过真实世界回顾分析,进一步确认了西达本胺联合治疗的疗效及安全性。
一项中国真实世界观察性研究,纳入2015年6月至2022年4月期间的48例PTCL患者,其中III/IV期患者占比91.8%,初治患者占比77.6%,旨在探讨西达本胺治疗PTCL患者的疗效和安全性。研究结果显示,33例患者获得客观缓解,ORR为67.4%,其中21例患者达到CR。2年无进展生存(PFS)率和2年总生存(OS)率分别为51.5%和68.5%。在27例既往未经治疗的PTCL患者中,CR率为59.3%,ORR为85.2%, 4年OS率为67.7%,其中 AITL患者的ORR为100%。良好的疗效和安全性表明,西达本胺将成为PTCL患者的一种新的治疗选择。



研究3:西达本胺联合泼尼松、环磷酰胺和沙利度胺(CPCT)治疗复发难治性(R/R)PTCL
研究亮点:CPCT全口服节拍治疗方案为unfit或不耐受化疗的R/R PTCL患者提供了安全有效的治疗方案选择。
一项开放、多中心、前瞻性、单臂II期临床试验,纳入45例因各种原因不耐受标准化疗的R/R PTCL患者,使用全口服CPCT方案进行诱导治疗,以及西达本胺单药进行维持治疗,以探讨此方案的疗效和安全性。研究结果显示,最佳ORR和CR/未经证实的CR(CRu)率分别为71.1%和28.9%。中位随访56个月,中位缓解持续时间(DOR)、PFS和OS分别为8.5、8.5和17.2个月。

亚组生存分析表明,不同组织病理学之间无显著差异(图2 A和B),而达到CR/CRu(N=13)的患者的中位PFS(P<0.001)和OS(P<0.001)仍未达到(图2 C和D)。最常见的3/4级不良事件为中性粒细胞减少(24.5%),但未观察到治疗相关死亡。综上,对于因各种原因不能耐受标准化疗的R/R PTCL患者,全口服CPCT方案是一种耐受良好且有效的疗法。

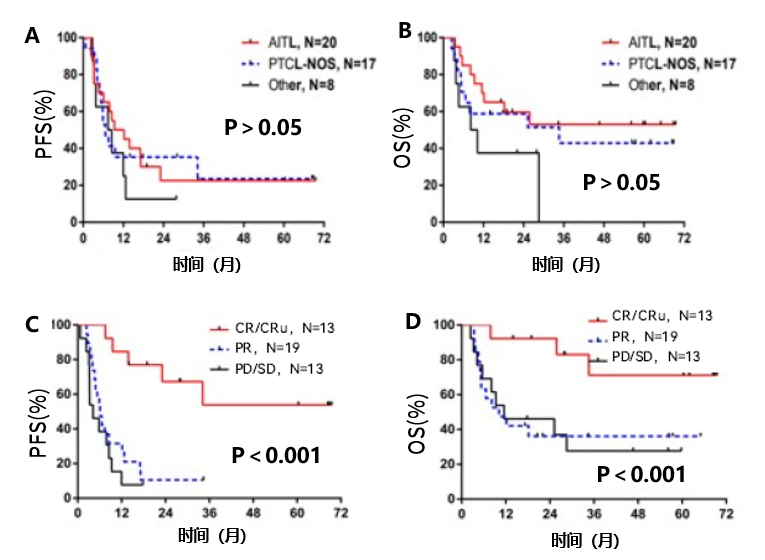
图2. CPCT方案治疗R/R PTCL亚组生存分析情况



研究4:西达本胺、替雷利珠单抗和培门冬酶(CTP)方案联合放疗一线治疗I/II期结外NK/T细胞淋巴瘤(ENKTL)的前瞻性研究
研究亮点:CTP方案联合放疗为早期伴高危因素的ENKTL提供了高缓解率、低治疗毒性的治疗选择,2年PFS率达85.7%。
一项前瞻性II期研究,旨在评估CTP方案联合放射治疗I期伴高危因素/II期早期ENKTL患者的疗效和安全性。37例患者入选,其中28例患者(75.7%)在放疗前至少进行一次疗效评估,其ORR为89.3%,CR率为71.4%。最终完成CTP+放疗治疗方案的24例患者,CR率达100%。对于28例可评估患者,中位随访24.1个月,中位PFS和OS均未达到。据估算,2年PFS率为85.7%(图3A),2年OS率为85.7%(图3B)。研究初步证实了CTP方案联合放疗作为一线治疗在I期伴高危因素/II期ENKTL患者中的有效性。患者的CR率较高,且不良反应可控。


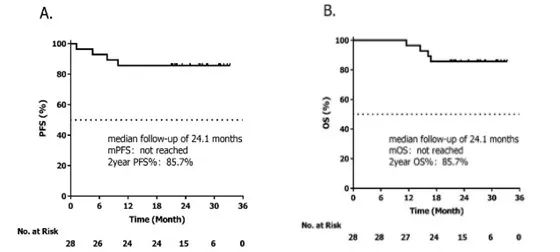
图3. A 可评估患者PFS率;B 可评估患者OS率



研究5:HDACi恢复AML细胞对维奈克拉的敏感性,导致不可逆的DNA损伤
研究亮点:HDACi逆转维奈克拉耐药,又添新证。
一项基础研究旨在确定维奈克拉和navitoclax潜在的联合用药选择,使用了53例复发性AML患者样本和51例新诊断AML患者样本的离体药物筛选数据(N=427种药物)。
研究发现如下所示:①在复发性AML患者样本中,对维奈克拉和navitoclax的敏感性与对HDACi Belinostat、Panobinostat和Vorinostat的敏感性相关。然而,在新诊断AML样本中未观察到这些药物之间的显著相关性。② BeatAML数据集中的维奈克拉耐药样本具有较高的HDAC4表达,但HDAC6和HDAC2水平较低。利用RNA测序数据,描述HDAC2、HDAC4和HDAC6的表达与对维奈克拉和navitoclax的敏感性之间的相关性。③ 维奈克拉耐药细胞系(OCIAML3、NOMO-1和NB-4)不依赖于BCL2,但对BCL2L1、MCL1和HDAC3敲除非常敏感。证明BCL2/BCL-xL和HDACi靶向不同的细胞群:高LSPC致敏评分定义了对维奈克拉和navitoclax的敏感性,而对HDACi的ProMono-like评分升高。④ 在100nM维奈克拉或navitoclax的情况下,采用无细胞毒作用浓度的HDACi处理维奈克拉耐药细胞系(MOLM-13和HL-60)可导致细胞大量死亡。⑤ HDACi和BCL-2i的双重作用是通过DNA损伤活性实现的。以上研究结果证明小剂量HDACi作为单药无毒,可通过诱导不可逆的DNA损伤使AML细胞对维奈克拉和navitoclax重新敏感。



研究6:维奈克拉联合阿扎胞苷和西达本胺(VAC)治疗新诊断急性单核细胞白血病(ND AML-M5)患者
研究亮点:VAC方案一周期可为ND AML-M5患者带来92.3%的复合完全缓解率,是一种低强度,耐受性良好的有效治疗选择。
一项队列研究,旨在评估VAC方案治疗不适合或拒绝接受强化疗的ND AML-M5患者的安全性和有效性。在第1周期,13例患者中有12例(92.3%)达到复合完全缓解(CRc, CR+CR伴血液学不完全恢复[CRi]+形态学无白血病状态[MLFS]),1例(7.7%)TP53突变患者未缓解(NR),且12例达到CRc的患者中有10例(81.8%)微小残留病(MRD)呈阴性(图4)。中位随访7.0个月,未达到中位OS和无事件生存期(EFS)(图5)。估算的12个月OS率为67.7%(95% CI,51-84),EFS率为69.2%(95% CI,57-81)(图5)。主要的严重不良事件为肺炎(2例[15.4%])和败血症(1例[7.7%])。结果提示VAC方案是一种有效的低强度方案,ND AML-M5患者耐受性良好。一个周期即可以产生高CR率和令人鼓舞的OS和EFS结果。

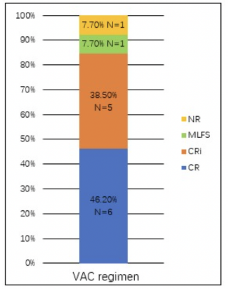
图4. VAC一个周期后缓解情况

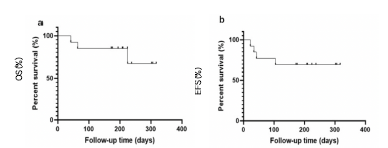
图5. 患者OS和EFS情况



研究7:高危T细胞急性淋巴细胞性白血病/淋巴瘤(T-ALL/LBL)患者移植后使用西达本胺维持治疗的回顾性研究
研究亮点:通过回顾性研究证实高危T-ALL/LBL患者移植后使用西达本胺维持治疗是安全且有效的。
一项回顾性研究,收集2019年11月至2023年2月接受异体造血干细胞移植(Allo-HSCT)和移植后维持西达本胺治疗的6例高危T-ALL/LBL患者的临床数据,旨在评估此方案的有效性和安全性。研究结果显示,6例患者均在移植后30天内获得CR,MRD为阴性。中位随访21个月,2/6例患者分别在移植后5个月和6个月复发,随后接受挽救性治疗,仍然存活,病情持续缓解。中位生存时间为21(12-37)个月,1年OS率为100%,1年PFS率为66.7%。安全性方面,主要不良反应为血液系统不良反应,主要表现为血小板减少(2~3级)、中性粒细胞减少(1~4级)和贫血(3级),通过延长西达本胺用药间隔时间而好转。本研究表明,对于高危T-ALL/LBL患者,移植后使用西达本胺维持治疗是安全有效的,需要进一步研究。



从王亮教授介绍的研究可见,HDACi联合用药用于PTCL、NKTCL的临床研究和真实世界展现出了较好的疗效,值得进一步集合全国的力量开展大型、前瞻性、头对头对照研究以验证HDACi联合方案的疗效和安全性。此外,HDACi在白血病中也进行了探索,展现出广阔的应用前景。
早期ENKTCL占比较多,且目前尚无标准治疗方案,培门冬酶诱导化疗联合放疗治疗效果较好,然而,约30%-40%患者仍未达到CR,预后较差,骨髓毒性和胃肠道毒性较重。又因黄慧强教授团队使用PD-1单抗治疗R/R NKTCL取得了良好的疗效,因此考虑为高危I/II期ENKTCL提供CTP方案联合放疗。初步研究结果显示,此方案取得了较好的疗效。目前,我们正在开展多中心临床研究,进一步探索此方案的疗效。
PTCL的标准一线治疗为CHOP方案,但疗效较差,5年OS率为30-40%,因此需进一步优化CHOP方案。本中心考虑使用西达本胺和阿扎胞苷双表观药物联合CHOP进行诱导治疗,待患者达到≥PR后行ASCT,并使用西达本胺进行维持治疗。目前,该研究入组顺利,患者安全性良好,此方案有望改善患者生存。
目前我们中心正在开展以及计划开展的研究包括,西达本胺联合多柔比星用于皮肤T细胞淋巴瘤治疗、西达本胺联合来那度胺治疗高龄无法耐受标准治疗的PTCL患者、西达本胺联合维奈克拉治疗低危急性白血病等。期望与在座专家携手共同开展更多的研究,造福更多患者。
VAC方案的设计来源于,既往研究发现两种表观遗传学药物具有协同效应,阿扎胞苷联合BCL-2i,以及HDACi联合BCL-2i亦带来了良好的疗效,此外,西达本胺已被证明可降低髓细胞白血病1(MCL1)的蛋白水平,克服BCL-2i耐药性,增强BCL-2i效能。又有研究发现,AML-M5患者接受维奈克拉联合阿扎胞苷治疗的ORR约为40%,远远低于VAC方案。因此,使用VAC方案在AML-M5一线治疗中进行了探索,早期试验取得了良好的疗效。
T-ALL/LBL发病率较低,是一种高度侵袭性的血液学肿瘤,预后较差。我们中心使用西达本胺对移植后患者进行维持治疗,疗效和安全性良好,但由于病例数较少,此数据仍需更多临床研究进行支持。一项由全国28家中心参与,使用西达本胺20mg,一周两次剂量进行维持治疗的临床研究正在开展中,期待此研究结果的公布。
会议末,朱军教授和牛挺教授总结道,此次“探为观智”会议让我们领略到了表观遗传学药物在淋巴瘤、白血病中的魅力,分享了我国学者在HDCAi创新应用方面的体会和经验,发出了中国学者的声音。拥有自主知识产权、国内首个上市的口服HDACi西达本胺具有与其他药物广泛协同作用的机制,可克服BCL-2i耐药,展现出了广阔的应用前景,其在双表达淋巴瘤中应用的数据也即将发布,期待西达本胺可继续拓展适应症,为全球血液肿瘤患者带来获益。感谢大家持续关注血液肿瘤领域新药研究,推动自主研发、传播、分享,为更多患者提供更好的更适合的治疗方案。我们一起努力,一起加油!








