

急性白血病领域:西达本胺协同多种药物提升治疗疗效

01
Preclinical Studies and Phase II Trial of Venetoclax in Combination with Chidamide and Azacitidine in Relapsed/Refractory Acute Myeloid Leukemia
西达本胺联合维奈克拉、阿扎胞苷治疗R/R AML的临床前研究和II期试验
主要作者:徐兵教授团队(厦门大学附属第一医院)
摘要编号:1428
展示形式:壁报
02
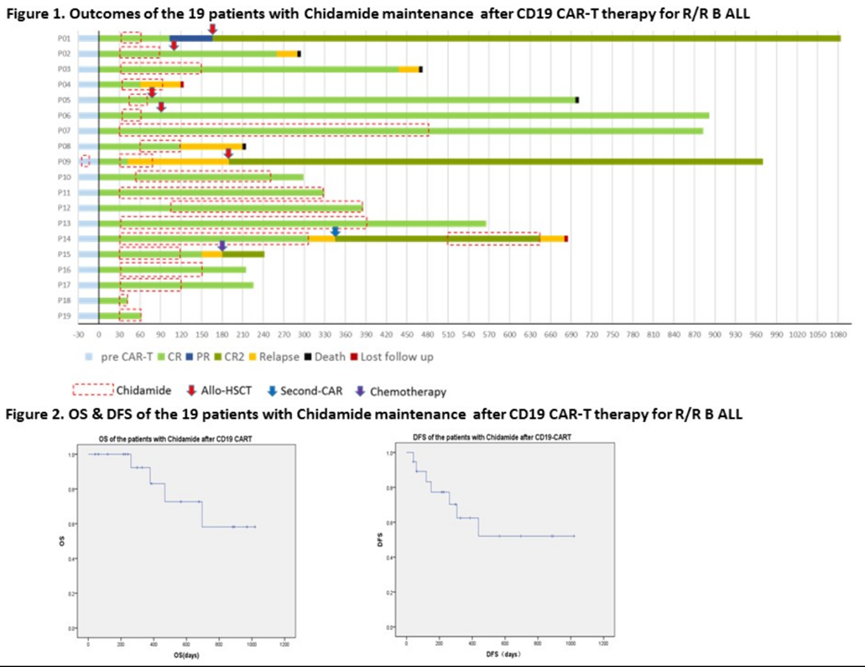
The Efficacy of Chidamide Maintenance Therapy after CAR-T Therapy for Refractory or Relapsed B-Cell Acute Lymphoblastic Leukemia
CAR-T细胞治疗后西达本胺维持治疗R/R B-ALL的疗效
主要作者:陆佩华教授团队(北京陆道培医院)
摘要编号:4005
展示形式:壁报
Synergistic Sensitivity of Selinexor with Chidamide By Targeting NF-Κb /c-FLIP Signaling Via Suppressing HDAC1/XPO1 Activity in T-ALL
西达本胺与Selinexor的联合敏感性:通过抑制T-ALL中HDAC1/XPO1活性靶向NF-Κb /c-FLIP信号
主要作者:葛峥教授团队(东南大学附属中大医院)
摘要编号:2665
展示形式:壁报
Histone Deacetylase Inhibitor Combined with Flumatinib Promotes Anti-Leukemia Sensitivity in Philadelphia-Positive ALL By Targeting PI3K/AKT Signaling
西达本胺联合氟马替尼通过靶向PI3K/AKT信号促进Ph+ALL的抗白血病敏感性
主要作者:葛峥教授团队(东南大学附属中大医院)
摘要编号:1345
展示形式:壁报
西达本胺联合方案:有望为R/R AML患者提供新的治疗选择
厦门大学附属第一医院徐兵教授团队前期使用高通量筛选平台选择维奈克拉、西达本胺和阿扎胞苷 (CVA) 的最佳联合疗法,在临床前研究中发现,CVA方案对CD34+CD38-KG-1α和Kasumi-1细胞的细胞活力减弱和诱导细胞凋亡表现出协同作用,进一步通过原代CD34+AML PDX小鼠模型,证实CVA方案降低了白血病负荷并改善了预后;从机制上讲,同时暴露于三种药物会抑制抗凋亡BCL-2家族蛋白(包括BCL2、BCL-XL和MCL-1),并与增强泛素化相关。
在一项多中心、单臂、开放性的 II 期研究中,纳入了29例R/R AML患者,25例患者(86.2%)对该方案有反应,一个疗程的ORR为75%(12/16:2例 CR,7例 CRi和3例PR),两个疗程的ORR为88.9%(8/9:5例 CR,2 例CRi和1例 PR)。
北京陆道培医院陆佩华教授团队使用西达本胺单药维持治疗接受CAR-T治疗后的R/R B-ALL患者,中位随访时间12个月(1-33个月),12个月OS率为83.1%,12个月DFS率为62.4%;5例患者在西达本胺维持后接受allo-HSCT,13例未接受移植患者的12个月OS为83.3%,12个月DFS为62.9%。对6例患者CAR-T细胞在T淋巴细胞中的比例进行了监测,CAR-T细胞比例均在西达本胺治疗后均有不同程度提高。
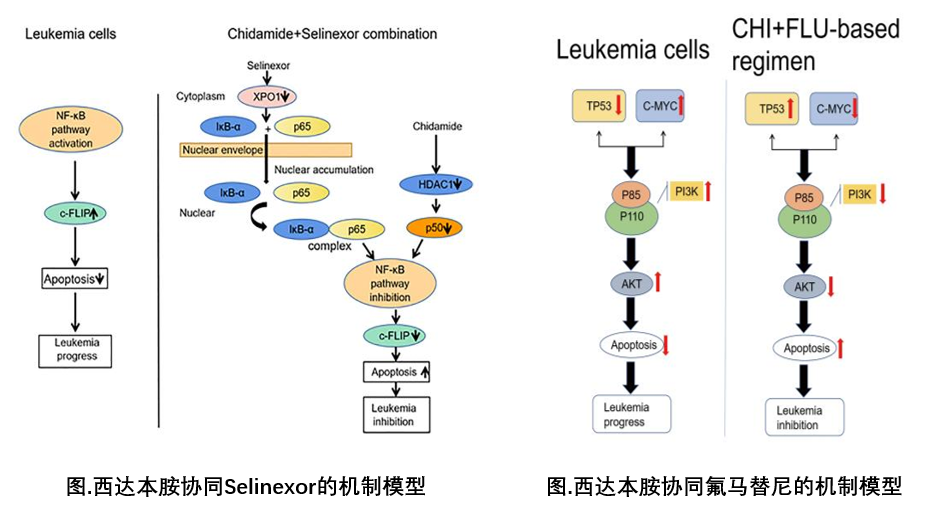
东南大学附属中大医院葛峥教授团队不仅发现Selinexor与西达本胺联合治疗可通过抑制XPO1/HDAC1活性靶向NF-kB/c-FLIP致癌信号传导,对T-ALL的细胞增殖停滞、凋亡和细胞周期停滞具有协同效应。此外,西达本胺联合氟马替尼能够通过p53 / c-MYC轴靶向PI3K / AKT信号传导,对Ph + ALL细胞的细胞增殖停滞和凋亡具有协同抗白血病作用,为ALL相关的临床研究提供了有利的基础研究数据支持。
淋巴瘤领域:HDACi联合治疗对多个亚型安全有效

01
A Preliminary Analysis of Chidamide Combined with R-GemOx (rituximab, gemcitabine and oxaliplatin) As Salvage Treatment for Transplant-Ineligible Patients with Relapsed/Refractory Diffuse Large B-Cell Lymphoma: A Prospective, Multicenter, Single-Arm, Phase II Study
西达本胺联合R-GemOx(利妥昔单抗、吉西他滨和奥沙利铂)挽救治疗不符合移植条件R/R DLBCL患者的初步分析:一项前瞻性、多中心、单臂、II期研究
主要作者:蔡清清教授团队(中山大学肿瘤防治中心)
摘要编号:4254
展示形式:壁报
02
Rituximab and Lenalidomide Plus Chidamide Can be an Effective Chemotherapy Regimen for Patients with Relapsed/Refractory Angioimmunoblastic T-Cell Lymphoma
西达本胺联合利妥昔单抗、来那度胺(RLC)方案是治疗R/R AITL的有效化疗方案
主要作者:杨海燕教授团队(浙江省肿瘤医院)
摘要编号:1600
展示形式:壁报
A Multicenter, Phase III Study of Chidamide, Azacitidine Combined with CHOP Versus CHOP in Patients with Untreated Peripheral T-Cell Lymphoma
西达本胺、阿扎胞苷联合CHOP(AC-CHOP)方案对比CHOP方案治疗初诊PTCL的多中心III期研究
主要作者:周道斌教授团队(中国医学科学院北京协和医院)
摘要编号:2922
展示形式:壁报
Chidamide Plus Prednisone, Cyclophosphamide, and Thalidomide (CPCT) for Relapsed or Refractory Peripheral T-Cell Lymphoma: A Multicenter Phase II Trial
西达本胺联合强的松、环磷酰胺和沙利度胺(CPCT)治疗R/R PTCL:一项多中心II期试验
主要作者:徐卫教授团队(南京医科大学附属第一医院)
摘要编号:4268
展示形式:壁报
Tucidinostat Maintenance after Achieving Objective Response to First-Line Therapy in Peripheral T-Cell Lymphoma: A Single-Center Retrospective Case-Control Study
PTCL患者一线治疗达到客观疗效后的Tucidinostat维持:一项单中心回顾性病例对照研究
主要作者:俞文娟教授团队(浙江大学医学院附属第一医院)
摘要编号:1603
展示形式:壁报
西达本胺联合方案,对不适合移植的 R/R DLBCL 安全有效
中山大学肿瘤防治中心蔡清清教授团队的一项前瞻性、多中心、单臂、II 期研究(NCT04022005),西达本胺联合 R-GemOx (CR-GemOx) 方案治疗不适合移植的 R/R DLBCL,41例患者的中位年龄为60岁(范围:26-74岁),复发疾病26例(63.4%),难治性疾病15例(36.6%),IPI 3-5分患者占比43.9%。研究结果显示ORR和CR率分别为61.0%和31.7%;14例bcl-2/c-myc双表达(DE)患者中,3例达到CR(21.4%),5例达到PR(35.7%),DE患者和非DE患者的ORR(57.1% vs 64.0%,p=0.673)差异无统计学意义;16例患者接受西达本胺维持治疗,中位PFS为7.6个月(95%CI:2.7 – 12.5个月);3/4级常见不良事件为中性粒细胞减少症和血小板减少症,可预防性处理。
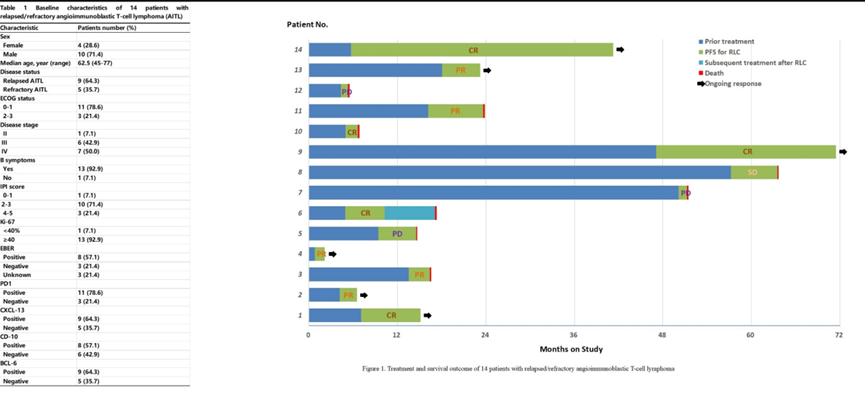
浙江省肿瘤医院杨海燕教授团队使用西达本胺联合利妥昔单抗、来那度胺(RLC)方案治疗R/R AITL患者,纳入的14例患者中,13例(92.9%)为III/IV期,患者的ORR为71.4%(10/14),CR率为35.7%(5/14),其中2例获得CR后序贯HSCT;中位PFS为6.3个月(4.6至8.0个月),中位OS为7.5个月(4.0至11.0个月);RLC方案治疗R/R AITL有效率高,不良反应可控。
中国医学科学院北京协和医院周道斌教授团队牵头开展了一项在国内4个中心进行的多中心、非随机的III期试验,使用西达本胺、阿扎胞苷联合CHOP(AC-CHOP)方案治疗外周T细胞淋巴瘤(PTCL),治疗结束时,AC-CHOP组的ORR和CR分别为60.0%和55.0%,而CHOP组分别为53.3%和26.7%(ORR的P=0.693,CR率的P=0.184)。中位随访时间9个月,AC-CHOP组的中位PFS为8个月,CHOP组为7个月(P=0.602)。目前研究纳入样本量较小,尚在继续入组中,AC-CHOP治疗方案中可观察到PTCL患者的CR率有改善趋势,值得进一步探索。
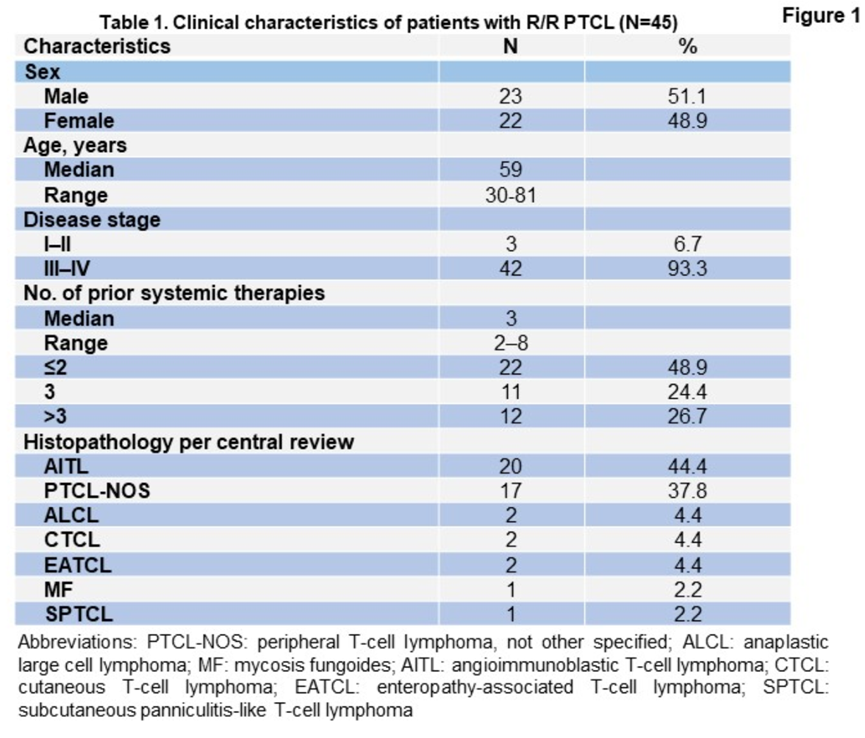
南京医科大学附属第一医院徐卫教授团队牵头开展了一项开放标签、单臂、多中心的关键II期研究,使用西达本胺联合强的松、环磷酰胺和沙利度胺(CPCT)治疗R/R PTCL,纳入45例患者,其中23例患者(51.1%)在入组前接受三线及以上大剂量化疗。在45例入组患者中,最佳ORR和CR/CR未确诊(CRu)分别为71.1%和28.9%,中位随访期56个月后,中位PFS和OS分别为8.5个月和17.2个月。中位缓解持续时间(DOR)为6个月(0.7-71.5个月),大多数缓解者(41名患者,91.1%)的DOR超过3个月。28例患者(62.2%)在6个月内持续缓解,17例患者(37.8%)在12个月内持续缓解。1年PFS和OS率分别为42.2%和57.8%,5年PFS和OS率分别为21.2%和43.8%。对于因各种原因不能耐受标准化疗的R/R PTCL患者,口服CPCT方案是一种耐受性良好且有效的治疗方案,但不同亚型的PTCL仍需进一步研究。
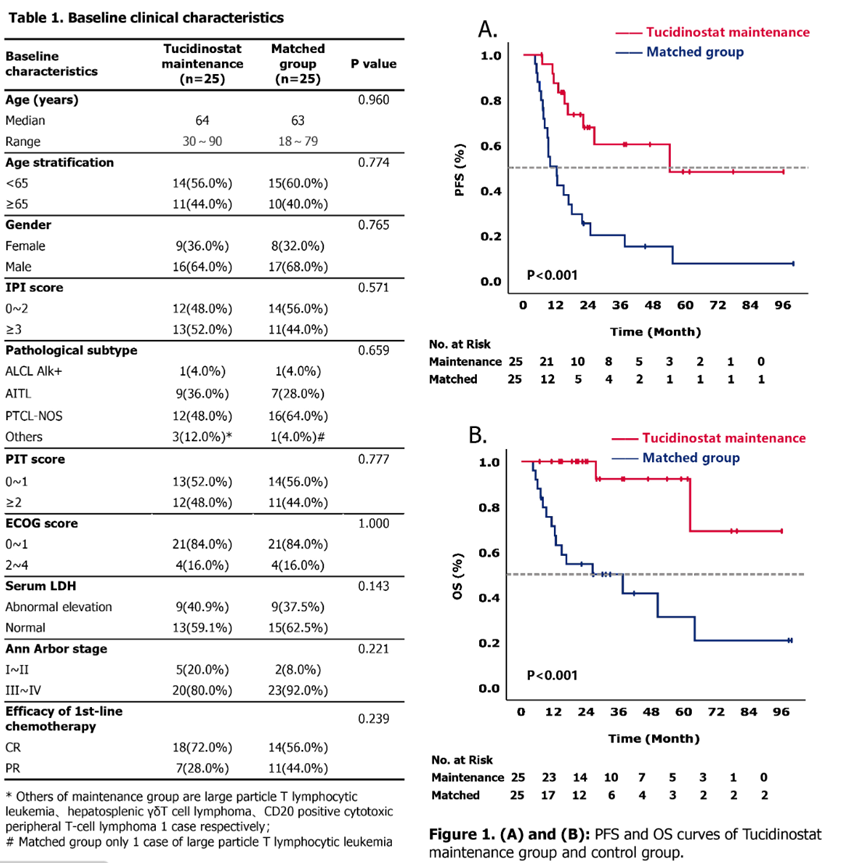
浙江大学医学院附属第一医院俞文娟、朱亚楠教授团队使用西达本胺维持治疗PTCL患者,根据国际预后指数(IPI)是否≥3分、病理亚型、患者是否> 65岁、性别,对473例初诊初治PTCL患者进行1:1倾向性评分匹配,共匹配25对(n = 50),研究终点包括无进展生存期(PFS)、总生存期(OS)和不良事件(AEs);西达本胺维持组和对照组CR率分别为72.0%(18/25)和56.0%(14/25)(P>0.05);中位随访时间分别为27.4(6.7-96.0)和22.2(4.3-99.6)个月,中位PFS分别为54.0个月和12.3个月,2年期PFS分别为67.9%和25.3%(P<0.01),中位OS分别为未达到和37.3个月,2年生存率分别为100%和54.6%。
表观遗传治疗是一种独特类型的靶向治疗,它不同于化疗和传统靶向治疗,而是靶向肿瘤发生、发展的全部特征性过程。西达本胺作为国产新型靶向选择性口服HDACi,以其独特且新颖的抗肿瘤机制,在血液肿瘤治疗领域不断开拓。本届ASH年会上,西达本胺的表现可圈可点:单药或联合方案治疗初治及复发/难治性PTCL/ DLBCL、复发/难治性AML/ALL等临床研究均取得了不错的成绩。C+联合探索为血液肿瘤的治疗带来无限可能。


张薇教授:回顾性分析中国血管免疫母细胞淋巴瘤,构建新型预后模型
蔡真教授:西达本胺联合方案可以通过上调BIM表达而发挥抗MM作用
孙自敏教授团队:西达本胺联合方案为R/R AML患者的桥接移植创造可能
1种维持选择,2年mPFS:HDAC抑制剂为淋巴瘤患者长期生存助力
苏州大学附属第一医院血液团队最新发表复发难治AML研究结果:双表观方案为复发/难治AML治疗另辟蹊径
