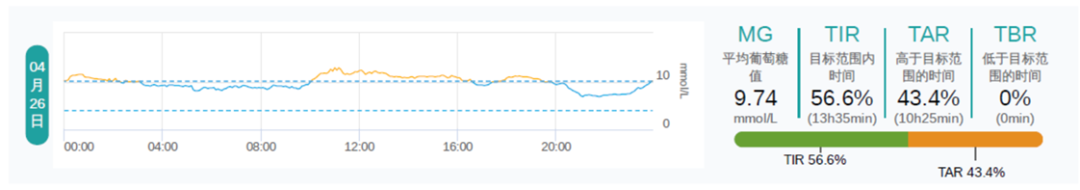
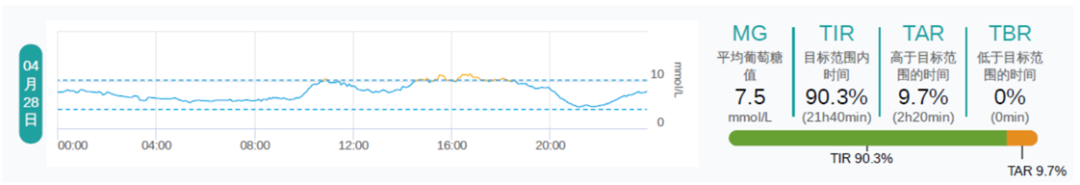
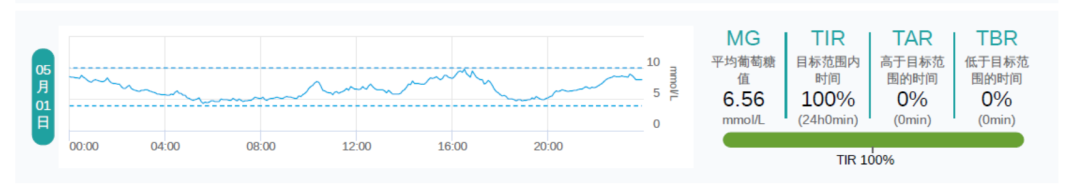
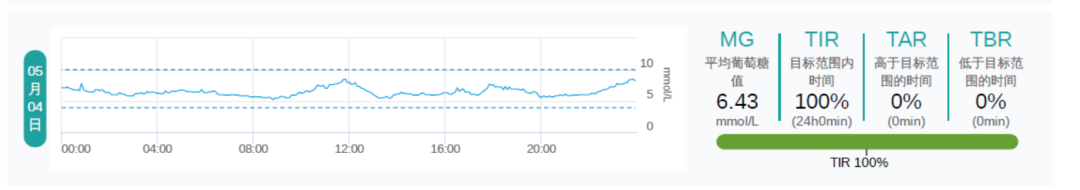
对于 2 型糖尿病(T2DM)患者来说,联合多种降糖药物治疗后血糖仍不达标,其问题的根源是什么?如果合并高胰岛素血症,停用胰岛素后的治疗方案如何优化?
上述所有问题的矛头,都指向了胰岛素抵抗(IR)。最新研究表明,IR 逐渐转变为中国糖尿病患病率增加的主要原因。而且,IR 的首要征象就是高胰岛素血症,伴随而来的是糖、脂代谢紊乱、脂肪肝、心血管损害、生活质量下降以及糖尿病进一步的发生发展[1]。
那么,在 T2DM 的管理中,针对 IR 的问题,如何治疗才能釜底抽薪?此次,辽宁省人民医院温滨红教授和青岛内分泌糖尿病医院王娜教授分享了典型病例的诊治过程,以及来自复旦大学附属华山医院李益明教授的精彩点评,一定会带来深刻的启示。
患者王某雅,女,42 岁,企业家。此次因[口干、多饮、多尿 10 年]就诊。
就诊前降糖方案:给予二甲双胍、恩格列净、格列美脲、利拉鲁肽降糖治疗,血糖控制欠佳。
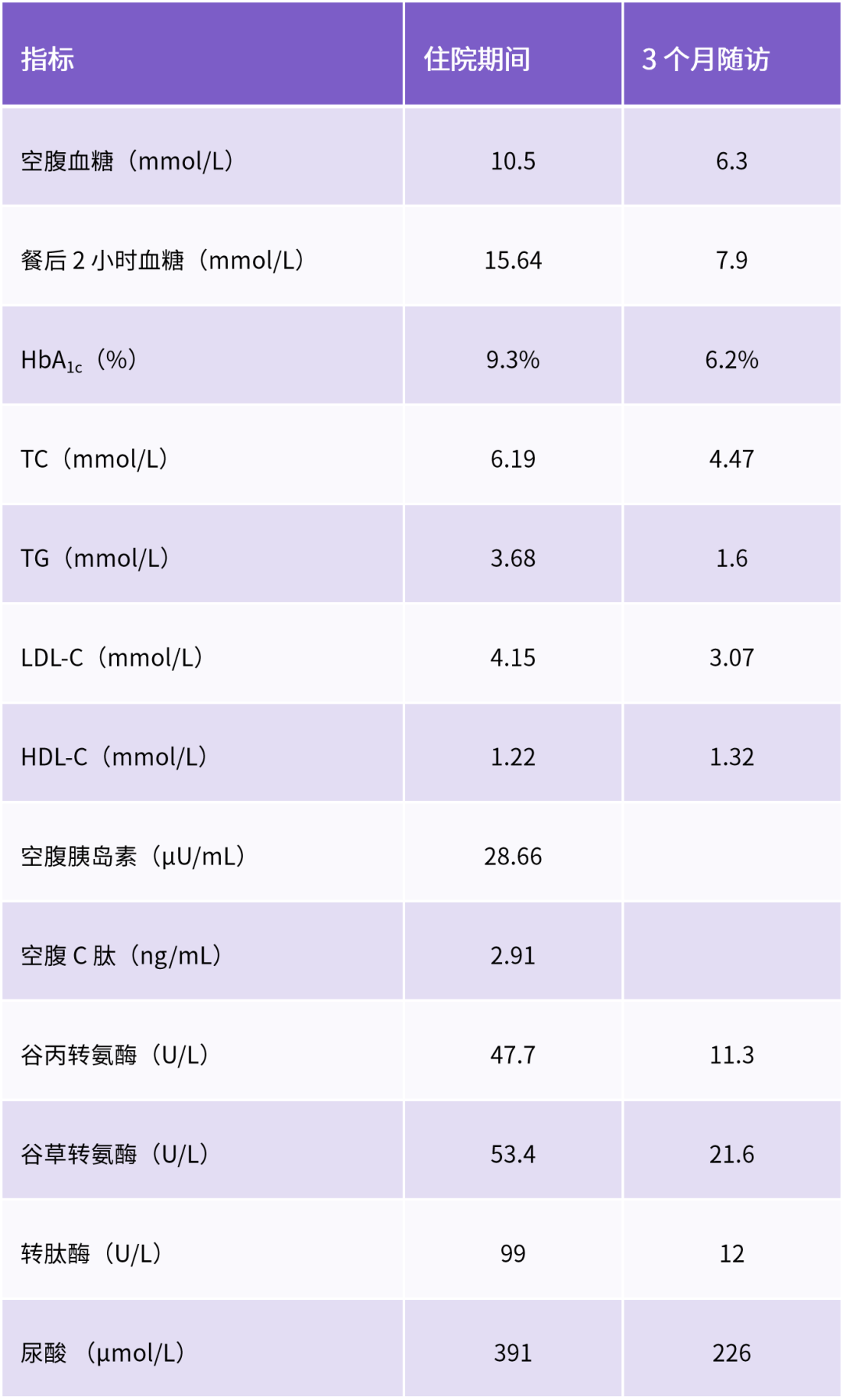
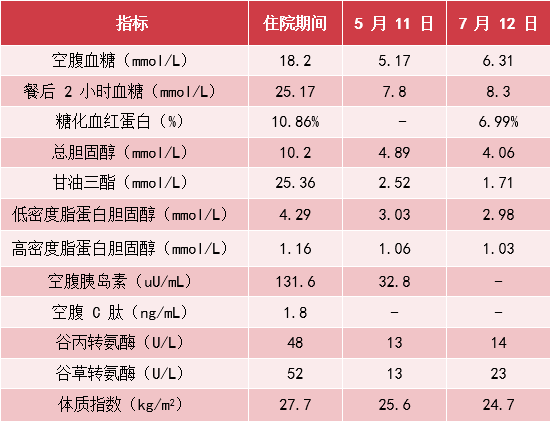
● 血糖控制差,合并肥胖:糖化血红蛋白(HbA1c)9.3%,空腹血糖 10.05 mmol/L,餐后 2 小时血糖 15.64 mmol/L;身高 166 cm,体重 100 kg,体质指数(BMI)36.28 kg/m2;腰围 138 cm,臀围 112 cm,腰臀比(WHR)1.23。
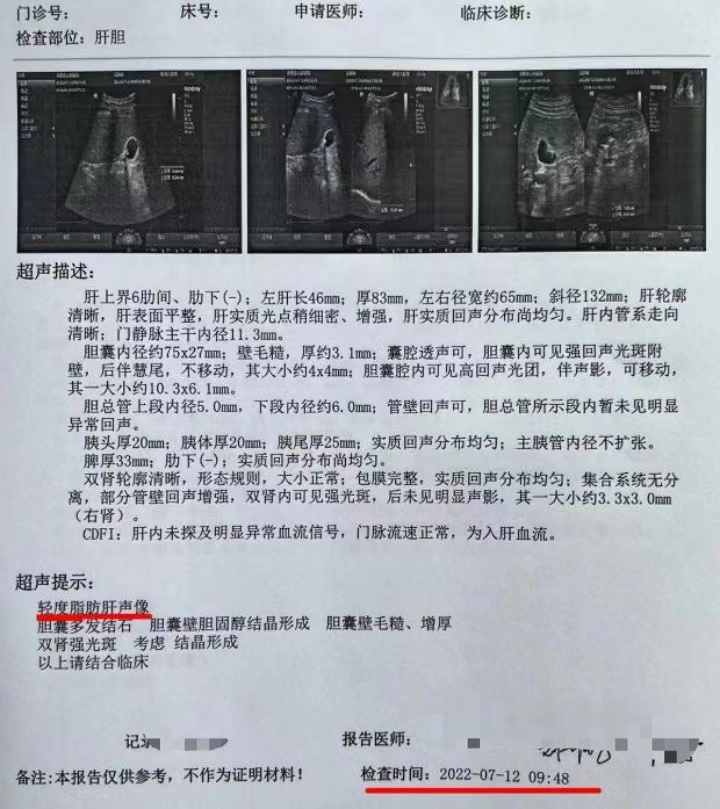
● 合并多个合并症/并发症:多囊卵巢综合征病史 20 余年,高血压病史 5 年,脂肪肝病史 15 年,伴有肝功能不全;谷丙转氨酶 47.7 U/L(7~40 U/L),谷草转氨酶 53.4 U/L(13~35 U/L);血尿酸 391 μmol/L(155~357 μmol/L),提示合并高尿酸血症;血脂谱示甘油三酯(TG)3.68 mmol/L(0~1.70 mmol/L),总胆固醇(TC)6.19 mmol/L(0~5.18 mmol/L),低密度脂蛋白胆固醇(LDL-C)4.15 mmol/L(0~3.37 mmol/L),高密度脂蛋白胆固醇(HDL-C)1.22 mmol/L(1.29~1.55 mmol/L),提示合并血脂异常;肝胆脾胰超声示肝大,脂肪肝,胆囊息肉,脾大。肌电图右正中神经传导速度减慢,提示糖尿病周围神经病变。
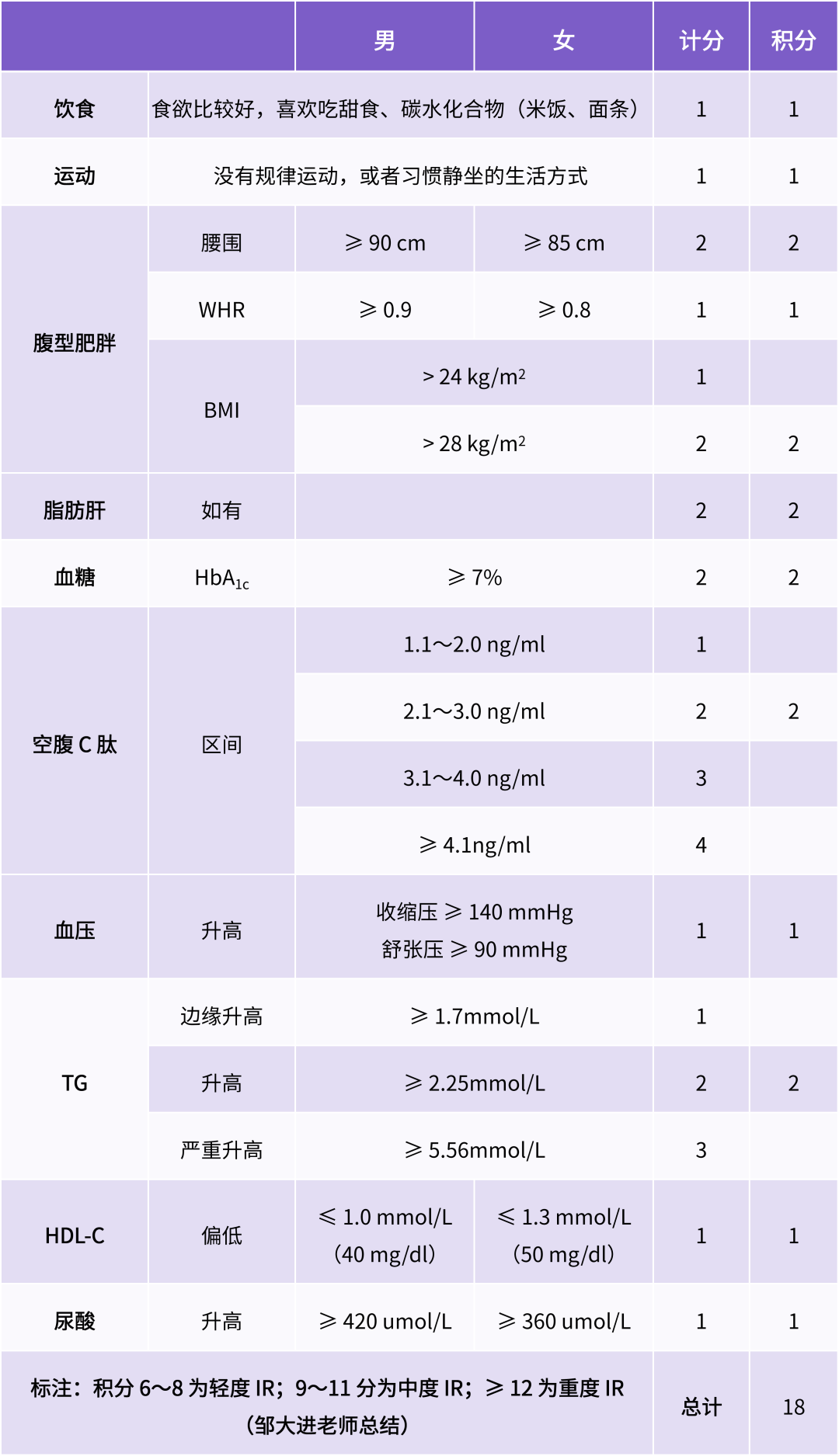
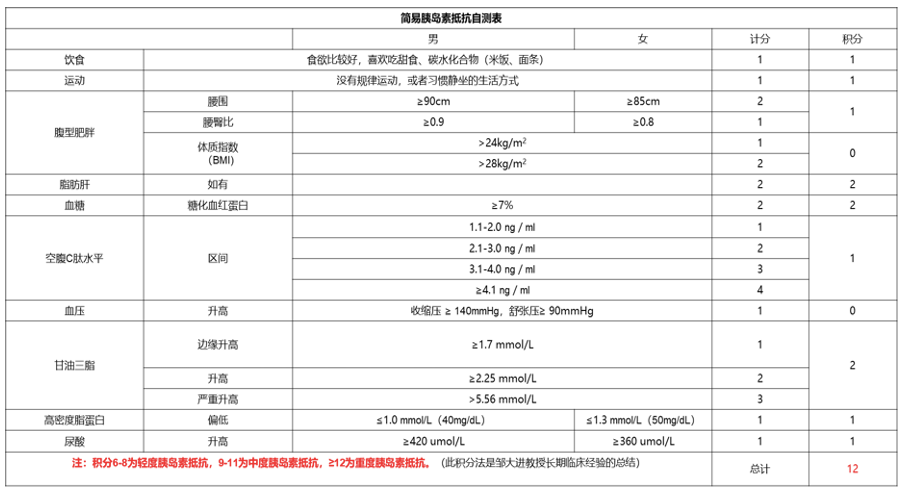
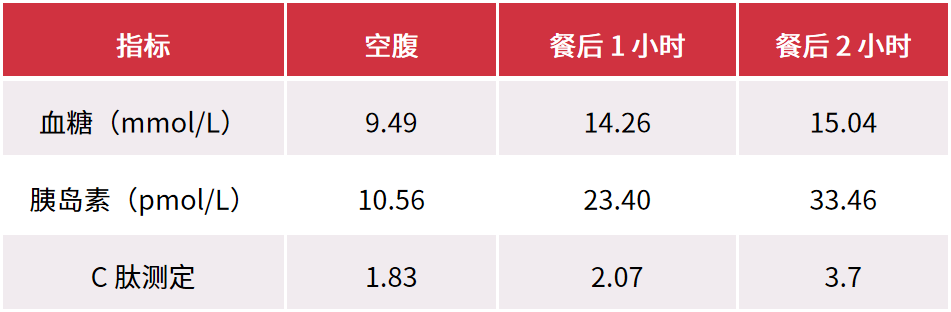
● IR 严重:IR 自测表评估提示重度 IR(表 1)。
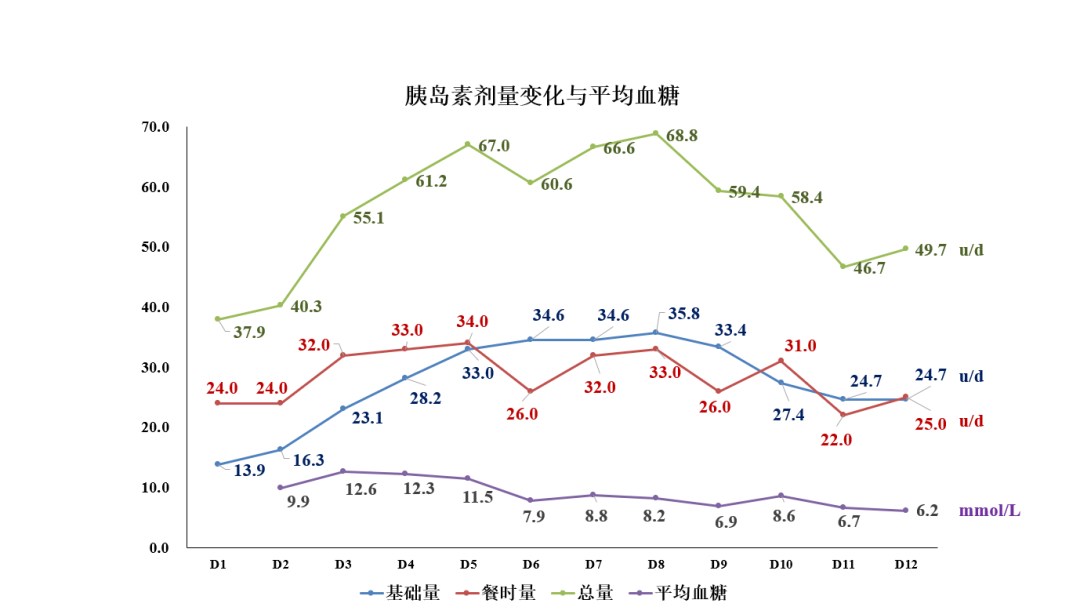
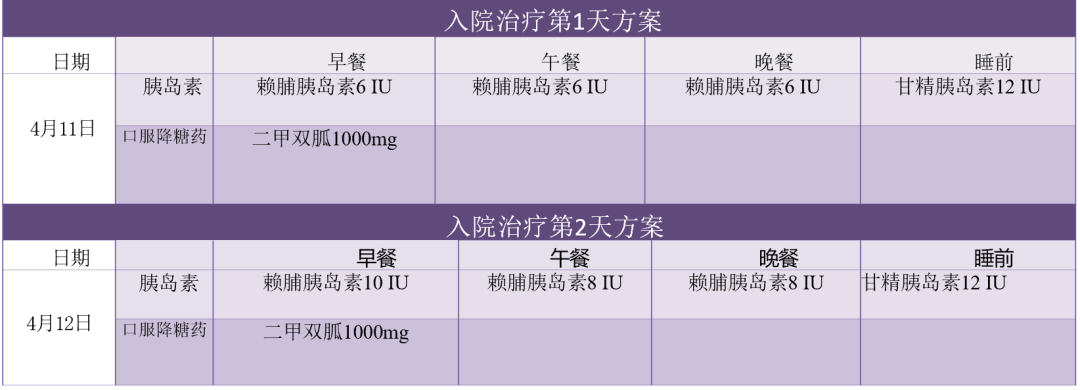
● 改善高血糖状态和 IR:住院期间经胰岛素泵强化治疗以去除高血糖毒性。
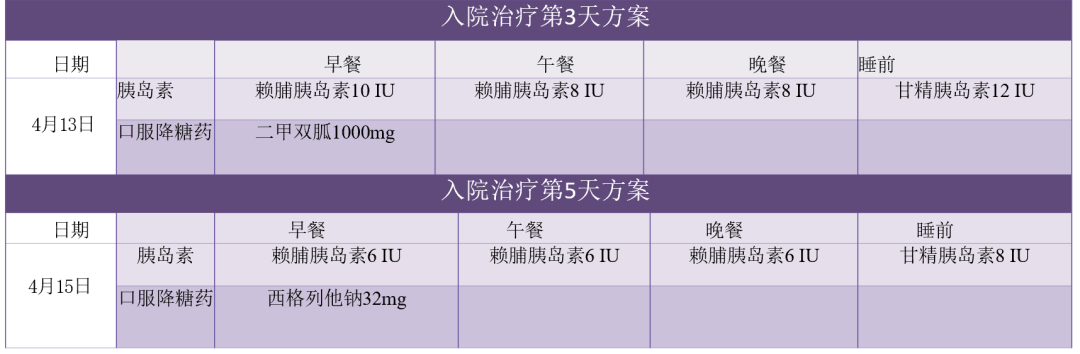
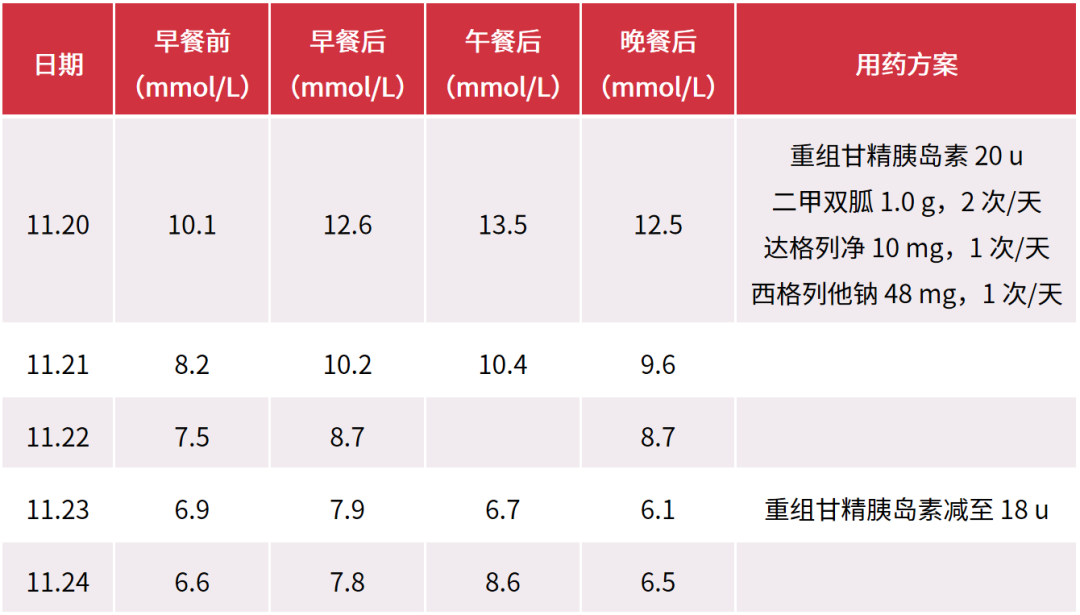
● 血糖控制平稳后,治疗方案:利拉鲁肽 1.8 mg/次,每日一次,皮下注射;二甲双胍 0.85 g/次, 每日三次,口服;恩格列净 10 mg/次,每日一次,口服;格列美脲 2 mg/次,每日 2 次,口服。
● 结合患者治疗病情特征,IR 明显、脂肪肝,需保护肝脏。治疗方案调整为:1. 停利拉鲁肽改为度拉糖肽 1.5 mg/次,每周一次,皮下注射;2. 停用格列美脲,维持二甲双胍及恩格列净治疗方案;3. 为了改善 IR,加用西格列他钠 48 mg/次,每日 1 次,口服。在全面降糖的同时,还具有控制体重、调节血脂、降低肝酶等保护作用。
● 改善血脂谱:在生活方式干预的基础上,加用阿托伐他汀 20 mg/次,每日一次,口服。
● 降压:培哚普利 8 mg/次,每日一次,口服。
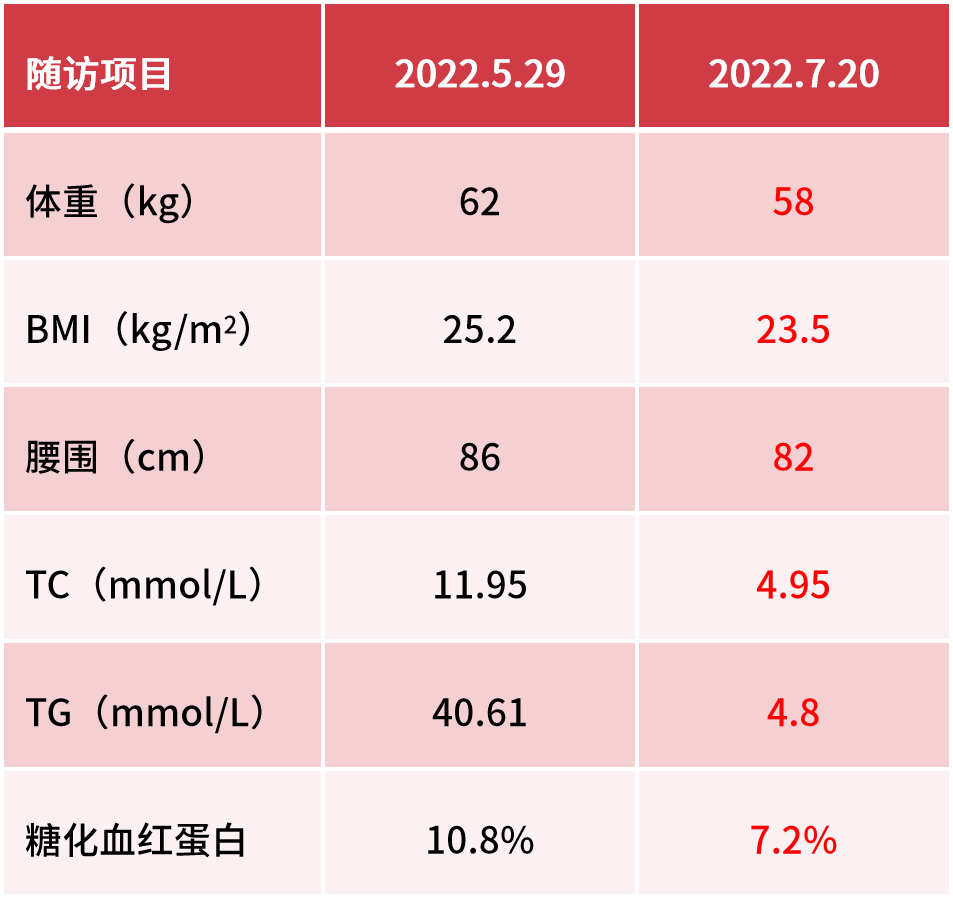
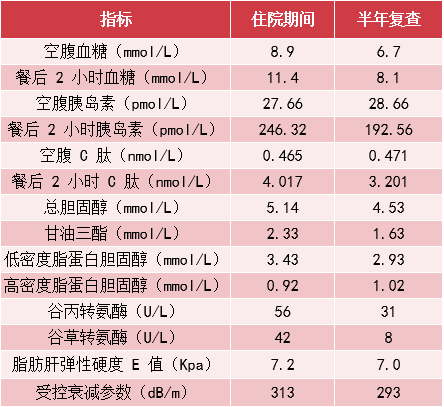
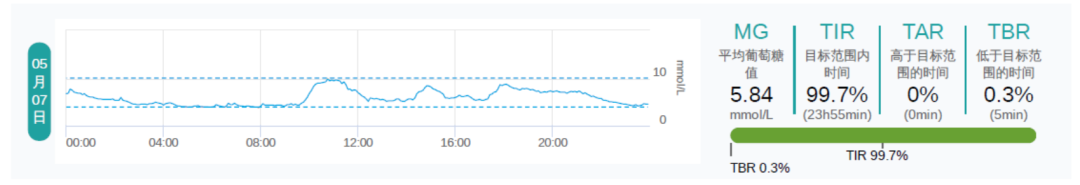
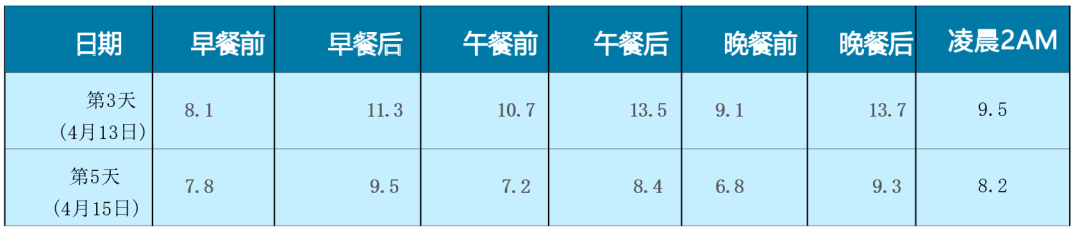
其他情况随访:肝肾功正常、无水肿,无低血糖发生、血压 130/74 mmHg,体重下降 3 kg、依从性良好。
诊疗体会: 患者 T2DM 发病早,10 年病程,IR 严重、合并肥胖及多个合并症/并发症,心血管风险高,曾使用口服联合注射降糖药物,血糖仍不达标,严重的 IR 是关键因素之一。降糖方案应在有效降糖的同时,兼顾改善 IR、控制体重、肝脏保护、心血管获益和提高用药依从性。
因此,除了使用二甲双胍、度拉糖肽、恩格列净以满足上述需求外,还加用了西格列他钠。作为 PPAR 全激动剂,西格列他钠直击高血糖和高血脂的核心病理生理异常机制,改善 IR,有效持久降低糖尿病患者的 HbA1c、空腹血糖和餐后 2 小时血糖。而且,有效调控血脂,降低 TG 及提高 HDL-C 水平。此外,还具有潜在的肝脏保护作用,不增加体重。每日仅需给药一次,简单方便。
最终,患者血糖控制理想,波动小,无低血糖和水肿发生,体重也得到改善。
男,57岁,私营业主。因[发现血糖升高 15 年]就诊。
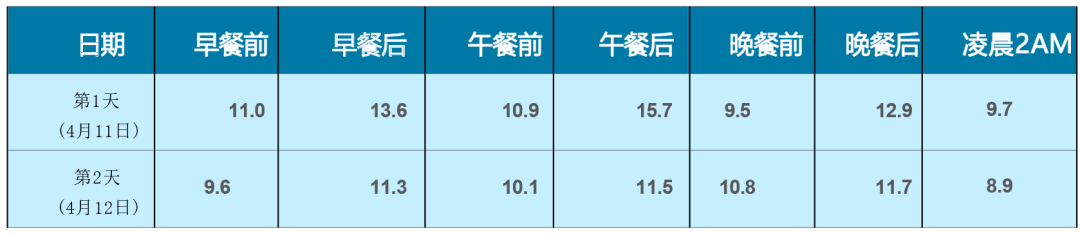
就诊前降糖方案:近期血糖控制不佳。使用胰岛素泵联合二甲双胍治疗 3 个月,血糖控制良好,HbA1c 在 6.5% 左右。近一周停用胰岛素泵,仅用二甲双胍治疗。治疗期间,体重增加约 1 kg,双眼视物模糊、手足麻木。
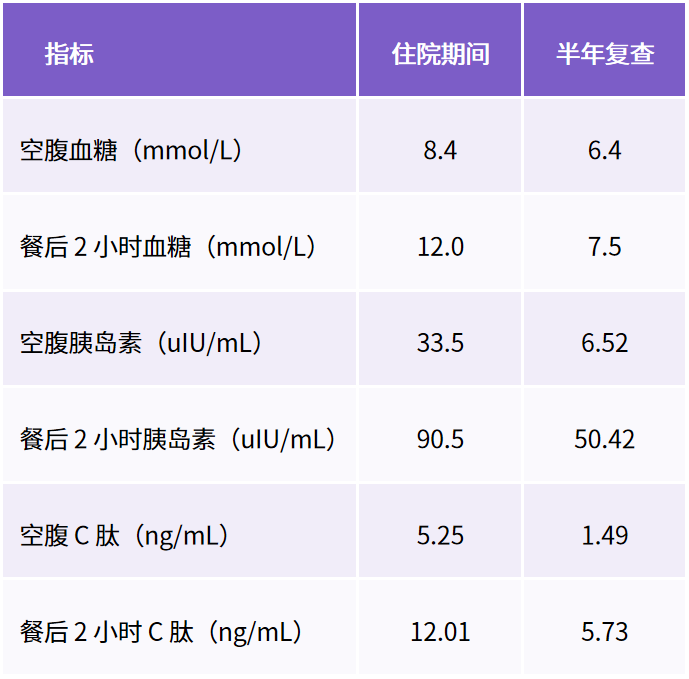
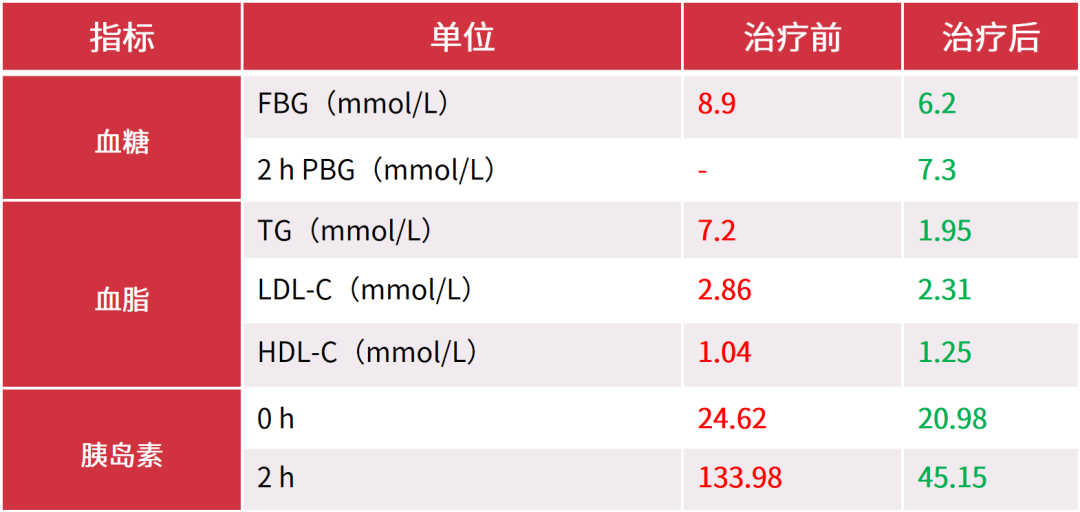
● 血糖控制良好,合并肥胖:HbA1c 6.8%;身高 176 cm,体重 90 kg,BMI 29.1 kg/m2;腰围 108 cm,臀围 114 cm,WHR 0.95。
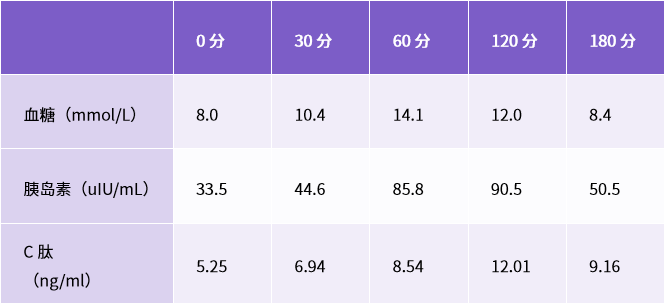
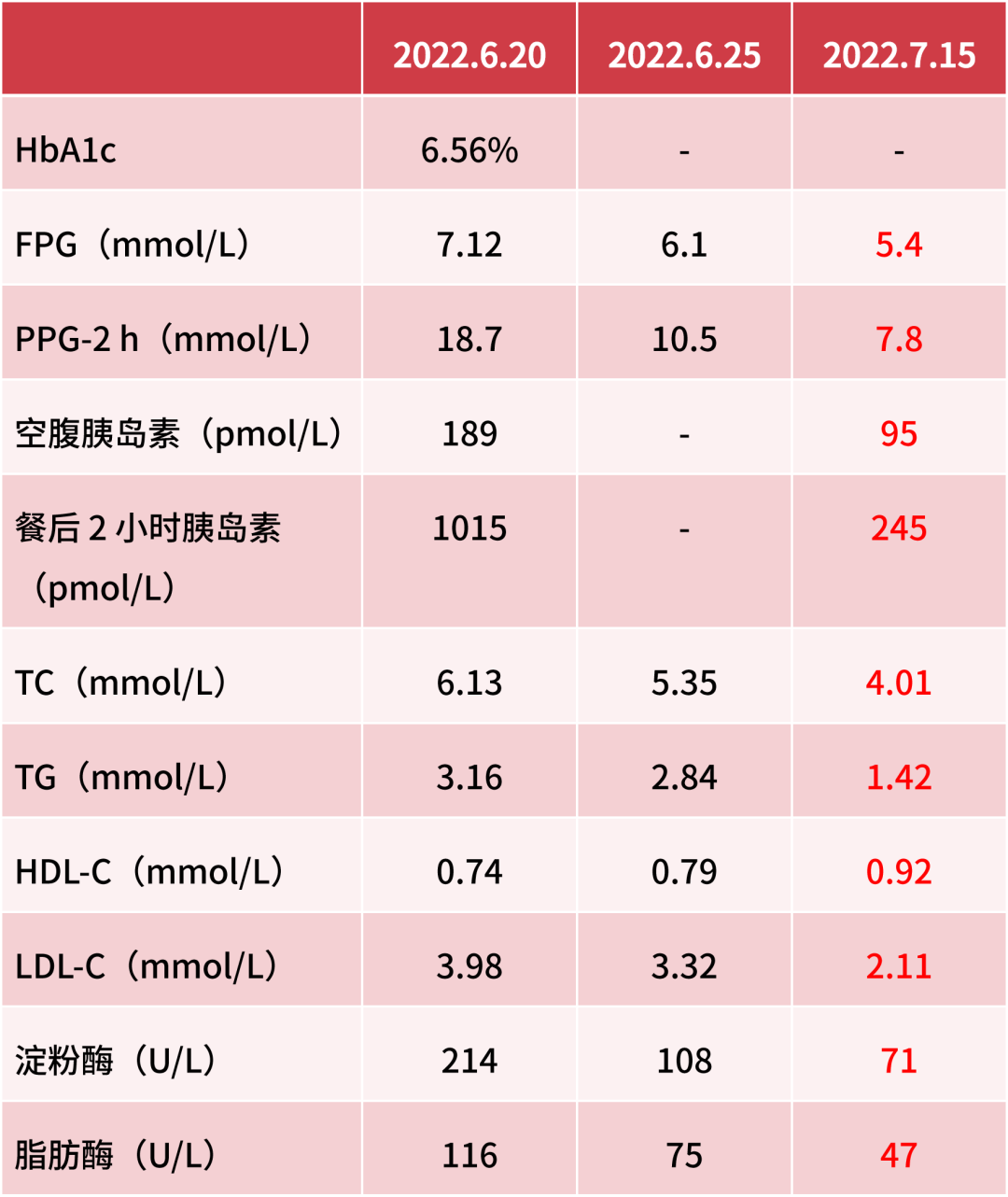
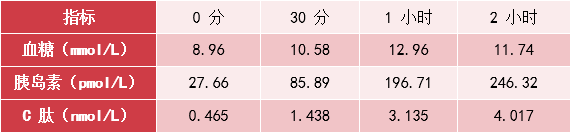
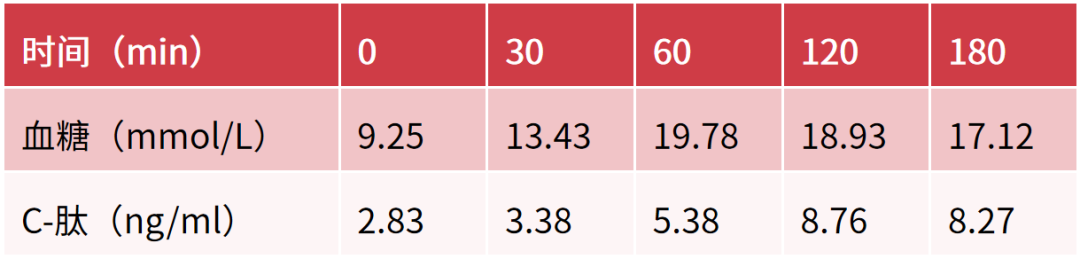
● 合并高胰岛素血症:口服葡萄糖耐量试验提示,血清胰岛素水平较高(表 3)。
● 合并多个合并症/并发症:腹部彩超示脂肪肝,双侧颈总动脉彩超:血管内膜毛糙,血管斑块形成(0.56 cm × 0.24 cm);血脂谱示 TC 5.33 mmol/L(0~5.18 mmol/L),TG 2.18 mmol/L(0~1.70 mmol/L),LDL-C 2.97 mmol/L(0~3.37 mmol/L),HDL-C 1.05 mmol/L(1.16~1.42 mmol/L);眼底检查示糖尿病性白内障、糖尿病视网膜病变;神经传导速度示中度神经损伤。
● 血糖控制达标。
● 减轻高胰岛素血症或不增加胰岛素的分泌。
● 控制或不增加体重。
● 不影响其他代谢指标。
● 不增加大血管病变风险。
● 继续生活方式干预。
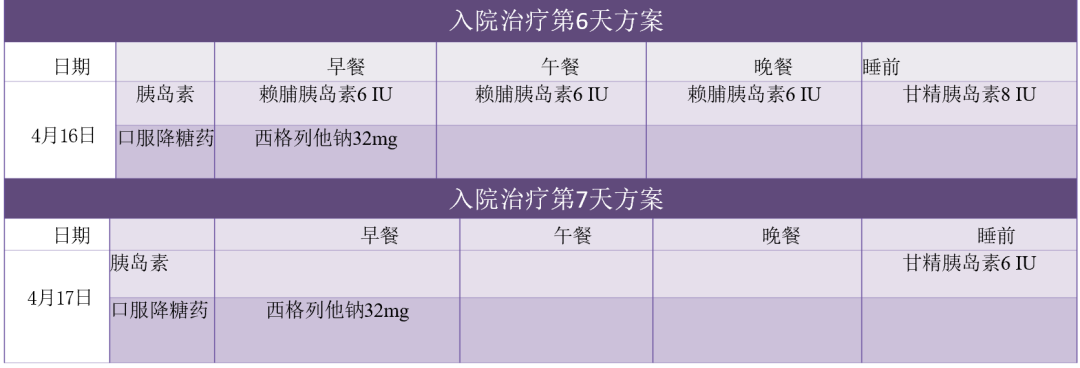
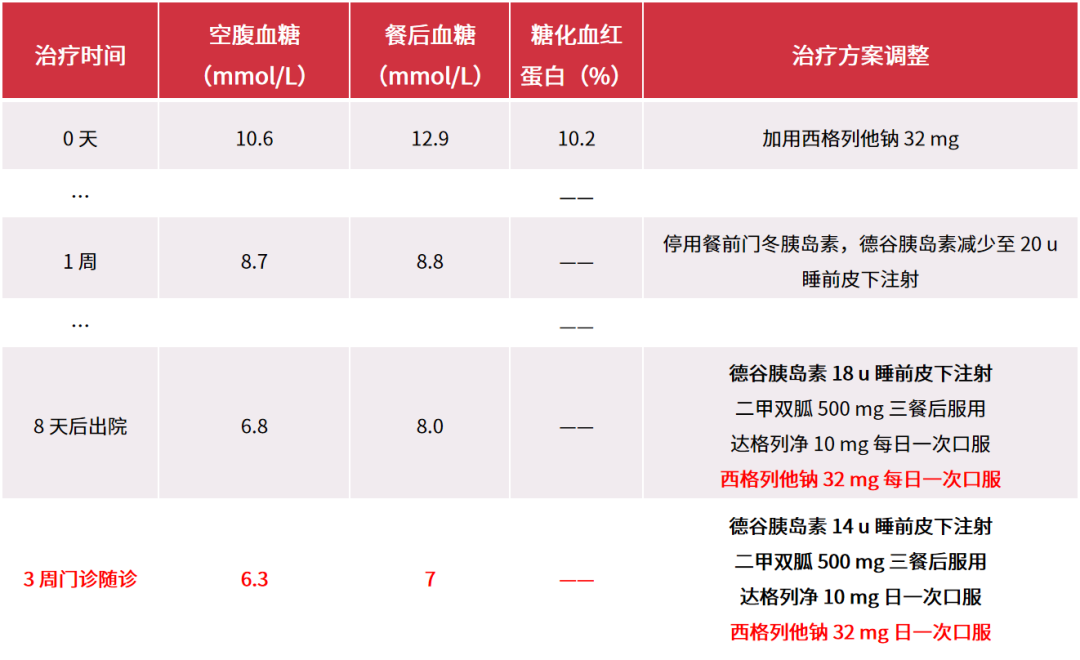
● 降糖药物调整:二甲双胍片 500 mg/次,每日三次,口服;曾尝试利拉鲁肽注射,因胃肠道不良反应严重而放弃;加用西格列他钠 48 mg/次,每日一次,口服。
● 因曾有反复龟头炎,未尝试 SGLT2 抑制剂。
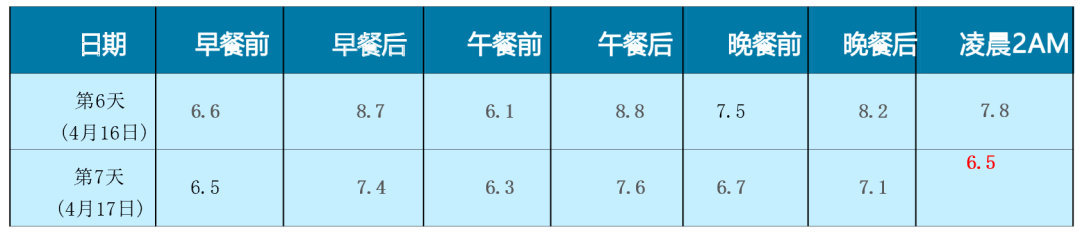
其他情况随访:体重逐渐下降了 5 kg;HbA1c 维持在 5.9%~6.2%;血压控制在 120/80 mmHg。
诊疗体会:
本例患者中年男性,T2DM 病程较长,长期使用胰岛素及二甲双胍控制血糖。虽然血糖控制达标,但合并肥胖(体重还在增加),高胰岛素血症提示存在 IR,且合并多个合并症及并发症。
降糖治疗方案不仅需要继续维持血糖达标,还要减少胰岛素水平或不必要的医源性高胰岛素血症,改善 IR,减轻体重。患者使用利拉鲁肽后因胃肠道不良反应严重而放弃;因曾有反复龟头炎,未尝试 SGLT2 抑制剂。
最后,给予患者 PPAR 全激动剂西格列他钠,通过改善 IR,有效降低患者的空腹血糖、餐后 2 小时血糖,并且停用了胰岛素,减轻了体重。
李益明教授 主任医师,博士生导师
复旦大学附属华山医院 内分泌科主任
● 中华医学会糖尿病学分会常委
● 糖尿病与相关内分泌病学组组长
● 糖尿病神经并发症学组副组长
● 中国医师协会内分泌代谢科医师分会委员
● 中国老年学和老年医学学会糖尿病分会副主委
● 上海市康复协会糖尿病分会主任委员
● 上海市医学会内分泌分会副主任委员
● 上海市中医药学会糖尿病分会副主任委员
● 上海市中西医结合学会内分泌代谢病专业委员会副主任委员
●《JCEM》、《中国糖尿病杂志》和《中华糖尿病杂志》编委
●《实用内科学》副主编、《harrisen 内分泌学》共同主译
主要的研究方向为神经内分泌疾病诊治、糖尿病神经病变和肥胖胰岛素抵抗。承担各级各类课题 19 项,发表 SCI 论文 120 余篇
IR 和胰岛素分泌缺陷是 T2DM 最核心的两大病理机制。研究证实,IR 的发生早于 T2DM 发病,在血糖正常时就已经存在。而且,IR 贯穿糖尿病发病全程,可导致胰岛 β 细胞负荷加重,最终引起血糖异常[2]。
IR 不仅会引发高血糖,也与动脉粥样硬化性心血管疾病、慢性肾脏病、代谢相关脂肪性肝病和肝硬化、癌症等疾病发生风险增加相关[3]。严重 IR 还会使微血管及大血管并发症的发生风险更高[2]。
第一个病例非常好地体现了上述疾病特征及诊疗要点。患者体型肥胖,高血糖合并血脂异常,还伴有多囊卵巢综合征、脂肪肝,这些都是典型的 IR 特点。因此,改善 IR 和糖脂代谢,并减轻体重是首要考虑的。
第二个病例有一个典型的特征,即出现明显的高胰岛素血症。高胰岛素血症是机体为了对抗 IR 的代偿性反应。但是,也会带来前述的一系列不良结局。因此,改善 IR 的治疗能起到釜底抽薪的作用[1]。
本次报道的两个病例,IR 严重,合并糖、脂代谢和脂肪肝是其共同特点。针对这两位患者的病例特点,缓解 IR 是治疗的当务之急。因此都采用了以新型 PPAR 全激动剂西格列他钠为基础、改善 IR 为主要手段的治疗方案。不仅患者的血糖、血脂等代谢指标得到改善,第一个病例患者的肝酶指标也得到改善,同时第二个病例患者的胰岛素水平也显著降低。
作为首个获批上市的、中国自主原创的 PPAR 全激动剂西格列他钠,采用了构象限制策略,适度均衡地激活 PPAR 三个亚型,改善 IR,也避免了传统胰岛素增敏剂的增加体重和水钠潴留的副作用,从而达到疗效及安全性的双向平衡[4]。目前,西格列他钠已纳入 2022 国家医保目录,相信会为更多 T2DM 患者带来治疗获益。
本内容仅供医疗专业人士阅读
内容策划:马腾
内容审核:周洁
题图来源:图虫创意
参考文献
1. 吕雪, 方琨, 郝文卿 , 等. 不同人群持续性高胰岛素血症的相关危害及其应对策略[J].临床荟萃, 2020, 35(12):1120-1125..
2. Ferrannini E, Gastaldelli A, Iozzo P. Pathophysiology of prediabetes[J]. Med Clin North Am, 2011, 95(2):327-39, vii-viii.
3. 邹大进. 消除胰岛素抵抗,去除慢病的“共同土壤” [J] . 中华全科医师杂志, 2022, 21(11) : 1007-1012..
4. Ji L, Song W, Fang H, et al. Efficacy and safety of chiglitazar, a novel peroxisome proliferatoractivated receptor pan-agonist, in patients with type 2 diabetes: a randomized, double-blind, placebo-controlled, phase 3 trial (CMAP)[J]. Science Bulletin, 2021, 66(15):1571-1580.