转自:良医汇-肿瘤医生APP
汇报医生:江苏省肿瘤医院 袁渊
点评专家:江苏省肿瘤医院 张莉莉
近年来虽然内分泌治疗策略不断更新发展,但约30%~40%的HR+乳腺癌患者经内分泌治疗后出现内分泌耐药,导致治疗失败,成为亟待解决的临床困境,内分泌治疗是指南推荐的HR+晚期乳腺癌的一线治疗方案。但是内分泌单药疗效有限,尤其对于有内脏转移的患者,缓解期短。随着CDK4/6抑制剂、mTOR抑制剂和HDAC抑制剂等靶向治疗的问世,突破了现有的治疗瓶颈,开启了HR+/HER2-晚期乳腺癌内分泌+靶向的治疗新时代。本文分享一例HR+/HER2-辅助内分泌治疗出现继发耐药的晚期乳腺癌病例,经一线氟维司群治疗进展后,使用西达本胺联合来曲唑治疗,肺、骨转移灶稳定,脑转移灶缩小,目前PFS已超过12个月,生活质量良好。

袁渊 医生
江苏省肿瘤医院副主任医师,医学博士,硕士生导师
江苏省肿瘤化疗与生物治疗委员会青年委员
江苏省区域与移植免疫专业委员会肿瘤诊疗多学科协作学组委员
江苏省抗癌协会肿瘤病因学及流行病学专业委员会委员
江苏省青年医学人才
2018-2019年在美国梅奥诊所研修一年
基本情况
患者,女,44岁。
2015.5(38岁)行左乳癌改良根治术,
术后病理:乳腺浸润性导管癌,II级,肿块直径1cm,淋巴结( 22/29 )见癌转移。
免疫组化:ER++90%,PR++90%,Ki 67+30%,HER-2(2+),FISH 检测HER-2(-),
术后分期:T1N3M0 IIIC期(Luminal B,高危)。
术后辅助治疗
辅助化疗:TEC方案化疗6周期;
辅助放疗;
辅助内分泌治疗:他莫西芬2年序贯OFS+依西美坦。
一线治疗
2019.8 CT:双肺新见散在结节,转移可能大;骨转移可能大。ECT:全身多发骨转移。
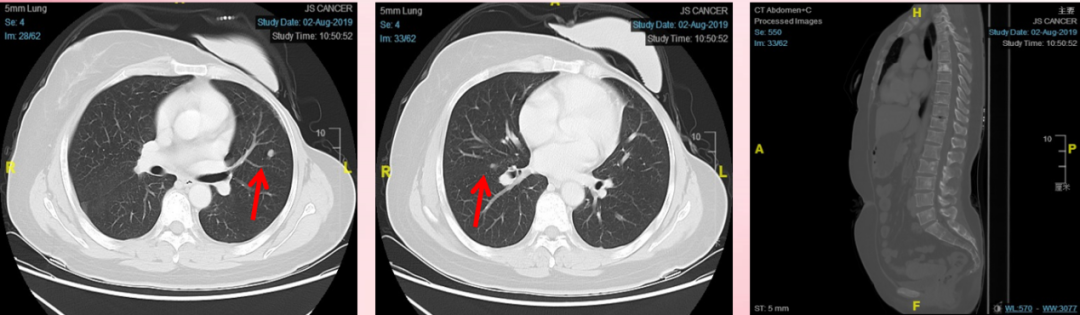
2019.8 基线影像学检查
诊断:左乳浸润性导管癌术后化放疗后,肺、骨转移IV期,DFS:50个月。
2019.8 开始亮丙瑞林3.75mg+氟维司群500mg+唑来膦酸 q4w治疗,同时口服碳酸钙D3 1片/日,治疗过程中无骨痛及SRE的发生。治疗3个月后(2019.11),影像学复查CT病情稳定。
2020.4复查,CT:大脑镰偏右侧强化结节,合并转移可能,双肺散在结节,部分增大,仍拟转移。多发骨转移,部分稍明显。患者病情进展,PFS 9个月。
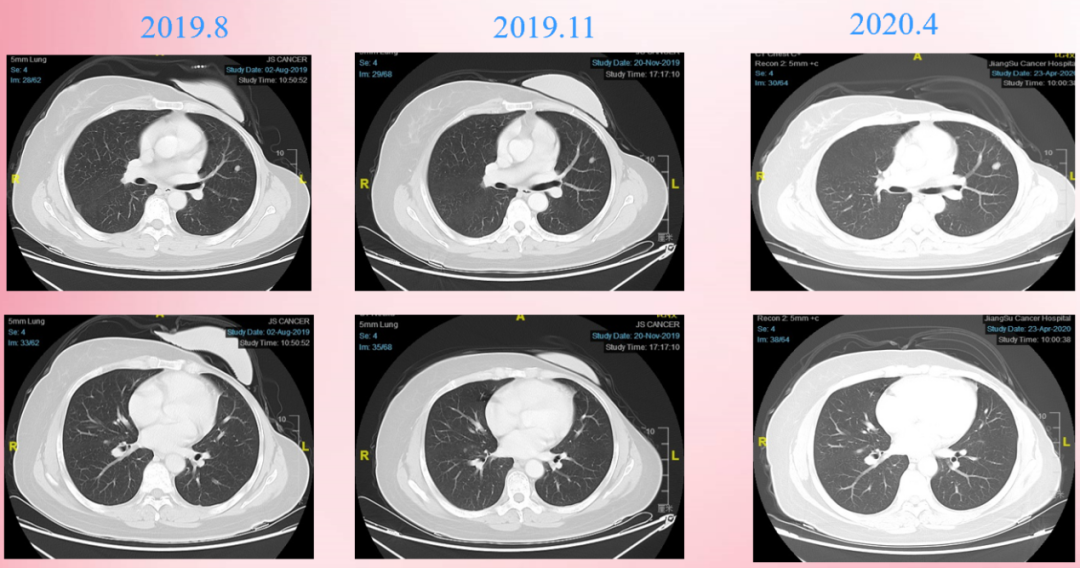
2019.8至2020.4肺部转移灶CT检查
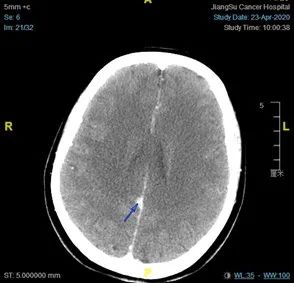
2020.4头颅CT检查
二线治疗方案
2020.5.19开始亮丙瑞林+西达本胺+来曲唑+唑来膦酸二线治疗,治疗过程中仅出现2级中性粒细胞下降,1级食欲下降,1级贫血,血糖、血脂、肝功能均正常,整体耐受性良好。
至2021.2复查CT: 大脑镰偏右侧转移灶较前缩小(后续复查已显示不清);双肺散在结节同前相仿;多发骨转移灶较前相仿,病情稳定,PFS已超过12个月,仍在治疗中。
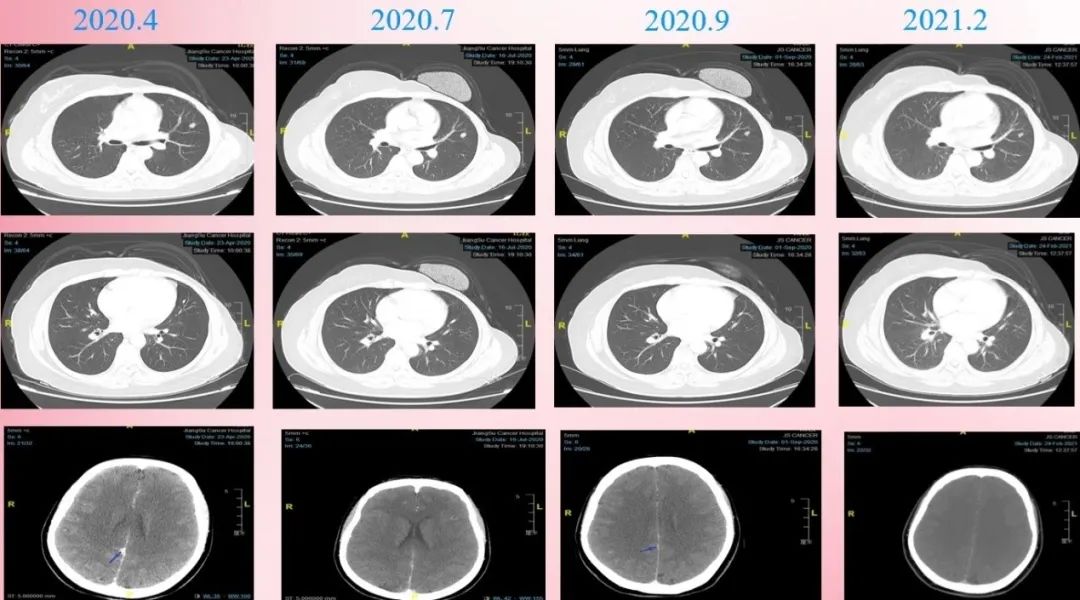
二线治疗前后,肺及脑转移灶CT检查

张莉莉 教授
江苏省肿瘤医院内科主任医师,硕士生导师,病区主任
中国抗癌协会乳腺癌专业委员会委员
中国医师协会肿瘤医师分会乳腺癌学组委员
中国女医师协会临床肿瘤专业委员会常委
江苏省医学会肿瘤化疗与生物治疗分会乳腺癌学组副组长
江苏省肿瘤防治联盟乳腺癌专家委员会委员
主要从事乳腺癌的临床、科研及教学工作,擅长乳腺癌的内科诊治,主持及参与多项乳腺癌相关的科研课题
承担多项乳腺癌相关新药、新方案的国际及国内多中心临床研究
这是一例初诊时为38岁的乳腺癌患者,接受左乳癌改良根治术,术后病理分期为IIIC期, Luminal B型,绝经前患者,复发风险为高危,术后给予辅助化放疗及内分泌治疗50个月后,CT检查提示肺部新见多发结节、骨扫描及CT提示多发骨转移,给予卵巢功能抑制联合氟维司群治疗,同时给予唑来膦酸治疗,期间评估病情稳定,9个月后患者新出现脑转移、肺部结节也较前增大;二线治疗选用西达本胺联合来曲唑及OFS治疗,病情稳定,治疗过程中耐受性良好,PFS已超过12月,目前仍在持续治疗中。在这例患者的治疗过程中,有如下体会:
1.HR+/HER2-且无内脏危象的晚期乳腺癌,一线治疗优选内分泌为主的治疗
患者术后分期IIIC期, Luminal B型乳腺癌,绝经前患者,复发风险为高危,予以辅助化疗、放疗及内分泌治疗(OFS+AI),DFS 达50个月。辅助内分泌治疗近4年时CT检查提示双肺新见多发结节,骨扫描及CT提示多发骨转移,因肺部结节较小未行穿刺检查,结合病史及影像学表现诊断为左乳癌术后双肺、多发骨转移,患者为HR+/HER2-转移性乳腺癌,虽有肺转移但无相关症状,骨转移亦无脊髓压迫等需要立即放疗的指证,复发转移发生在辅助内分泌治疗近4年时,属于内分泌继发耐药,此时应优选内分泌为主的治疗,可以选择内分泌联合靶向治疗或单用内分泌治疗,患者因经济原因无法接受靶向药物,因此选择了单用内分泌治疗。
根据多中心III期临床试验Global CONFIRM和China CONFIRM研究结果,对于经AI治疗后的HR+/HER2-晚期乳腺癌患者,使用500mg氟维司群具有临床获益的优势。该患者治疗选择了OFS+氟维司群治疗,期间复查病情稳定,耐受性良好,9个月后新出现脑转移,肺部病灶较前稍增大,考虑病情进展,氟维司群单药治疗PFS9个月,临床获益。
2. 一线内分泌单药进展后,靶向药物西达本胺与内分泌药物联用,是HR+HER2-晚期乳腺癌治疗的重要选择
患者氟维司群治疗9个月后新出现脑转移,但患者脑转移灶较小且无中枢神经系统相关症状,肺部转移灶也无转移相关症状,加之既往内分泌治疗获益,因此仍可考虑内分泌为主的治疗,应优选内分泌联合靶向治疗,可以选择的靶向药物包括CDK4/6抑制剂、西达本胺、依维莫司等,患者因经济原因无法接受CDK4/6抑制剂治疗。
基础研究提示表观遗传修饰的改变可能会导致耐药的发生和包括乳腺癌在内的不同类型癌症的复发,HDAC抑制剂(西达本胺)作为一种表观遗传调控剂实为复发转移患者的重要选择。同时,西达本胺除了抑制肿瘤细胞周期、诱导凋亡、增加抗肿瘤细胞免疫活性、诱导肿瘤微环境改变等一般性抗肿瘤机制外,还对乳腺癌细胞的激素受体通路、芳香化酶活性、NF-κB通路具有显著抑制作用,与抗激素治疗药物具有明确的机制互补作用。
值得一提的是,由江泽飞教授牵头,中国多个中心参与的ACE研究,在HR+/HER2-晚期乳腺癌患者中评估了西达本胺联合依西美坦的临床疗效和安全性。研究结果显示,西达本胺联合依西美坦治疗组的PFS明显优于安慰剂联合依西美坦组。总体人群中,研究者评估的西达本胺组中位PFS是7.4个月,而安慰剂组为3.8个月(HR=0.75;95%CI:0.58-0.98;P=0.033)。研究者评估的次要研究终点分析显示,西达本胺联合依西美坦组的ORR为18%,优于对照组的9%(P=0.026);同时,西达本胺联合依西美坦组的CBR为47%,优于对照组的36%(P=0.034)。基于这一研究结果,2019年11月西达本胺获批HR+/HER2-晚期乳腺癌的适应症, 结合患者病情、循证医学证据、药物可及性等因素给予西达本胺联合内分泌治疗。
患者经西达本胺+来曲唑+OFS的治疗后,多发肺、骨转移灶较前相似,脑转移灶缩小,病情稳定,目前PFS已超过12个月,仍在获益中。通常情况下,药物治疗对于脑转移病灶疗效有限,该患者经上述治疗后,脑部病灶较前缩小,是否与西达本胺特殊的作用机制相关值得进一步研究。另外,晚期患者尤其需要关注患者的生活质量和用药安全性,该患者整体耐受性良好,仅出现了2级中性粒细胞下降,1级食欲下降,1级贫血,血糖、血脂、肝功能均正常,兼顾了患者获益与生活质量。相对于CDK4/6抑制剂联合内分泌治疗,中国原创靶向药物西达本胺的药物可及性更高,是HR+/HER2-晚期乳腺癌有效的治疗选择。
西达本胺适应证:
联合芳香化酶抑制剂用于激素受体阳性、人表皮生长因子受体-2阴性、绝经后、经内分泌治疗复发或进展的局部晚期或转移性乳腺癌患者。
适用于既往至少接受过一次全身化疗的复发或难治的外周T细胞淋巴瘤(PTCL)患者。
参考文献:
1.中国临床肿瘤学会指南工作委员会.《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南2019》
2.Di Leo A, Jerusalem G, PetruzelkaL,etal. Final overall survival: fulvestrant 500 mg vs 250 mg in the randomized CONFIRM trial. J Natl Cancer Inst. 2014 Jan;106(1):djt337.
3.Zhang Q, Shao Z, Shen K, etal. Fulvestrant 500 mg vs 250 mg in postmenopausal women with estrogen receptor-positive advanced breast cancer: a randomized, double-blind registrational trial in China. Oncotarget. 2016 Aug 30;7(35):57301-57309.
4.Jiang ZF et al. Tucidinostat plus exemestane for postmenopausal patients with advanced, hormone receptor-positive breast cancer (ACE): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol 2019; 20: 806–15.
5.Wander SA etal. Genetics to epigenetics: targeting histone deacetylases in hormone receptor-positive metastatic breast cancer. Lancet Oncol. 2019 Jun;20(6):746-748.
责任编辑:Jo
排版编辑:Jason
版权声明
版权归肿瘤资讯所有。欢迎个人转发分享,其他任何媒体、网站如需转载或引用本网版权所有内容,须获得授权,且在醒目位置处注明。