近期,国家药典委员会发布了关于组建第十二届药典委员会的通知,引发业内热切关注。药典作为国家药品标准的重要组成部分,对于一个国家的药品的研发、生产以及上市具有强制约束力,是所有药品生产、检验、使用和监管的基本遵循。也正因如此,组建新一届药典委员会的通知才会受到如此关注。
我国现行的最新版药典为2020年版《中华人民共和国药典》(以下简称:《中国药典》),新版药典在2015版的基础上扩大了药品品种和药用辅料标准的收载,并在相关标准的制定上与时俱进,尤其在化学药品杂质控制方面制定了更高的要求,突显了《中国药典》对杂质控制的更加重视以及对于药品安全性的监管更加严格。
本文将为大家简要梳理《中国药典》的编撰历程以及新版更新亮点,并以临床常见药物为例,为大家呈现在《中国药典》这一“国考”之下,药品是如何以高标准交出满意答卷的。
作者简介

药典是所有药品必须遵守之标准
新版《中国药典》以更高要求保障公众用药安全
药典是国家药品标准的重要组成部分,是药品生产、检验、使用和监管的基本遵循。国家药典对一个国家的药品的研发、生产以及上市具有强制约束力。回望历史,首版《中国药典》的编纂工作几乎与新中国的成立同步。迄今为止,《中国药典》已经历十一次版本更迭。最新的2020版《中国药典》也即第十一版《中国药典》,是目前所有在我国生产上市的药品应当符合的技术要求。
其中值得一提的是,新版药典在化学药品杂质检测这一部分有了较大程度的修订和增加。针对“药品杂质分析指导原则”,新版药典明确了原料药和制剂质量标准应包括已鉴定杂质、未鉴定杂质、非特定杂质以及杂质总量,对整体药品杂质的质量控制提出了更高的要求。此外,对于药品常见的残留溶剂列表及其限度进行了增加和修改,对相关金属元素杂质也给予了明确。
针对药品杂质检测的标准只是其中之一,但可以一斑窥豹,看出2020版《中国药典》以一以贯之的高标准,为我国上市的药品立好规矩,为我国民众的用药安全把好关。
杂质含量高标准下
经典老药必需以技术保证符合药典标准
新版药典针对药品杂质制定了较高的标准,这也给我国上市的各类药品提出了新的要求。
以地奥司明这一临床应用近五十年之久的老药为例,该药具有保护血管、提高静脉张力、增加淋巴回流和改善毛细血管通透性等药理活性,在慢性静脉功能不全、静脉溃疡和痔疮等疾病的治疗中应用广泛[1]。地奥司明原研药物已在国外应用多年,国内地奥司明仿制药也有广泛应用。
地奥司明源自橙皮苷,属于类黄酮物质。橙皮苷作为地奥司明的主要原料,其在不同的药物制剂中经常作为天然杂质伴随地奥司明。然而研究表明,当黄酮类化合物杂质含量很大时,可能会对活性物质地奥司明产生不利影响或影响其分解代谢。因此,为了保障地奥司明的疗效及安全,各国药典都对地奥司明药品制剂的纯度及杂质控制有着严格要求。
欧洲药典[2]及美国药典[3]均规定,地奥司明药品制剂含活性成分地奥司明应为标示量的90.0%~102.0%;杂质(如乙酰异香草酮、橙皮苷、异野漆树苷、蒙花苷/里那苷、香叶木素等)总量不得超10.0%。2020版《中国药典》规定[4],地奥司明药品制剂含地奥司明应为标示量的90.0%~110.0%;含橙皮苷不得超标示量的5.0%;除橙皮苷外,单个杂质含量不得大于3.0%,含量在1.0%~3.0%的单个杂质不得多于3个;杂质总量不得超8.0%。
表1 中国、美国和欧洲药典关于有效成分地奥司明纯度和杂质总量的标准规定
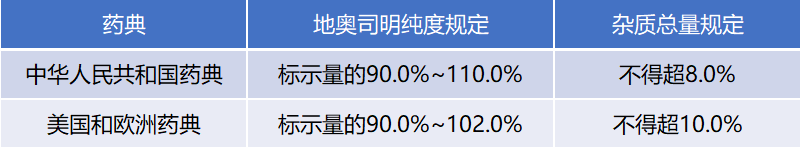
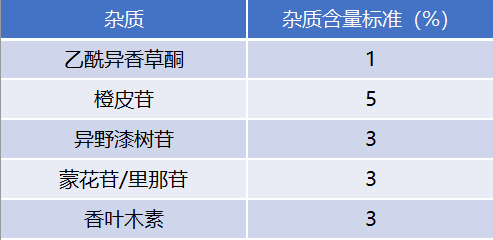
表2 美国和欧洲药典关于地奥司明具体杂质的标准规定
纯度和杂质的高标准对于药品制剂的提纯工艺提出了较高的要求,这样的标准对所有地奥司明药品来说都是必需达标的考验。
各项杂质含量均达标
纯化微粉化地奥司明通过中国药典“国考”
尽管我国地奥司明药品不止一种,但由于纯度和杂质的高标准与药品制剂的提纯工艺相关,因此真正完美符合《中国药典》标准的地奥司明品类其实并不多见,纯化微粉化地奥司明(葛泰®)则是其中交出满意答卷的那一个。
据纯化微粉化地奥司明片2020年8月的检测报告显示,按干燥品计,其地奥司明的含量为95.6%,橙皮苷含量为0.11%,杂质总量为3.7%,这几项关键指标均通过《中国药典》的考核,且其它各项也均达《中国药典》标准。
结语:药典是保证药品质量,确保人民用药安全、有效,质量可控,依法制定的药品法典。2020版《中国药典》以与时俱进的高标准,对我国的药品生产、上市制定了准则。面临药典的“国考”,唯有保持高水准的生产工艺,才能生产出符合药典标准、满足临床需求、最终为广大患者带来切实获益的好药。
参考文献
1. Katherine A,Lyseng-Williamson,Caroline M. Perry, et al. ADIS DRUG EVALUATION.2003; 63 (1): 71-100.
2. European Pharmacopoeia, Volumn10.0.
3. 2018 U.S. Pharmacopoeia National Formulary.USP41 NF36.
4. 2020版《中华人民共和国药典》.
转载于中国医学论坛报


