MRD
#01
问
什么是MRD?
答
MRD(Minimal Residual Disease)的概念源于白血病在诱导化疗达到完全缓解(或骨髓移植治疗)后,在患者体内依然残留着痕量白血病细胞的状态。转换到实体瘤的应用中,一般泛指在根治性治疗(如手术切除)后,传统影像学或实验室方法不能发现病灶,但通过液态活检技术可检出癌细胞来源分子的情况。实体瘤患者检出MRD,代表癌细胞在体内持续存在,癌症复发的风险较高。
Minimal Residual Disease(MRD)微小残留病灶
指癌症患者在治疗中或治疗后体内仍有残留的恶性肿瘤细胞存在,细胞坏死或凋亡过程中释放出肿瘤循环DNA(Circulating tumor DNA,ctDNA)。在NCCN指南和欧洲专家共识中,MRD即指可测量残留病灶,即Measurable Residual Disease。MRD阳性患者通常比阴性患者预后更差、复发更早、死亡更早。
Molecular Residual Disease(MRD)分子残留病灶
目前,MRD指的是经过治疗后,传统影像学(包括PET/CT)或实验室方法不能发现,但通过分子诊断发现的肿瘤来源分子异常(肿瘤分子异常:指的是外周血可稳定检出丰度≥0.02%的ctDNA,包括驱动基因或其他的I/II 类基因变异),代表着肿瘤的持续存在和临床进展可能。
#02
问
什么是肺癌MRD检测和临床应用共识?
答
在第18届中国肺癌高峰论坛上,全国肺癌临床、基础和检测领域的顶尖专家围绕“肺癌微小/分子残留病灶(MRD)研究进展和临床应用”进行了深入地交流和探讨,最终达成“肺癌MRD的检测和临床应用共识”。
共识一:MRD的概念
①肺癌分子残留病变,指的是经过治疗后,传统影像学(包括PET/CT)或实验室方法不能发现,但通过液体活检发现的癌来源分子异常,代表着肺癌的持续存在和临床进展可能;
②肺癌分子异常:指的是外周血可稳定检出丰度≥0.02%的ctDNA,包括肺癌驱动基因或其他的I/II 类基因变异。
共识二:MRD检测的基本技术要求
①MRD检测的基本技术,包括tumor-informed assays(个体化定制)和Tumor-agnostic assays(NGS Panel和多组学技术),目前均处于探索阶段,需要前瞻性研究确定其敏感性、特异性和预测价值;
②采用二代测序技术(NGS),所选用的多基因Panel中必须覆盖患者Ⅰ/Ⅱ类基因变异,基本技术标准是可稳定检测出丰度≥0.02%的ctDNA;
③驱动基因阳性的非小细胞肺癌,MRD的分子Panel应包括该驱动基因;
④MRD评估报告中必须包括cfDNA丰度、ctDNA丰度,所检测基因VAF值;
⑤需要建立针对免疫治疗的MRD标准。
共识三:可手术早期肺癌MRD的应用
①早期非小细胞肺癌患者根治性切除术后,MRD阳性提示复发风险高,需进行密切随访管理。建议每3-6个月进行一次MRD检测;
②建议基于MRD开展可手术非小细胞肺癌的围手术期临床试验,尽可能提供围手术期精准治疗方案;
③建议分别探索MRD在驱动基因阳性和驱动基因阴性两种类型患者中的作用。
共识四:局部晚期非小细胞肺癌MRD的应用
①局部晚期非小细胞肺癌根治性放化疗后完全缓解患者,建议检测MRD,有助于判断预后和制定进一步的治疗策略;
②建议开展基于MRD的放化疗后巩固治疗的临床试验,尽可能提供精准的巩固治疗方案。
共识五:晚期非小细胞肺癌MRD的应用
①晚期非小细胞肺癌目前缺乏针对MRD的相关研究;
②晚期非小细胞肺癌系统治疗后完全缓解患者,建议检测MRD,有助于判断预后和制定进一步的治疗策略;
③建议在完全缓解患者中开展基于MRD的治疗策略研究,尽可能延长完全缓解持续时间,使患者能最大获益。
#03
问
什么是MRD的技术难度和技术边界?
答
目前实体肿瘤MRD的检测难度较大,主要体现在两方面:
1. 不同实体瘤个体化差异大,即每个患者个体中仅携带非常少量、相同的基因突变,对panel的设计要求高。
2. 早期实体瘤释放到外周血的ctDNA含量非常少(低于1%),对检测灵敏度要求极高。TracerX研究表明,每cm3肿瘤病灶(直径1.2cm)相当于每毫升血浆里面具有0.19个肿瘤基因组的拷贝,意味着ctDNA丰度大约在0.01-0.02%。进行一个微小残留病灶的检测时,ctDNA检测的敏感性需要触达万分位的数量级。
#04
问
什么是MRD技术路线?
答
针对上述难题,目前采用ctDNA检测MRD主要存在两大技术路线: tumor-informed(基于肿瘤组织测序的ctDNA个性化定制方案)和tumor-agnostic(仅基于血浆检测的固定panel)。
1.tumor informed路线(WES+个性化panel)
现成的panel能够覆盖的位点相对比较有限,除了在单点上增加敏感性之外,可以通过增加更多有潜力、可监控的阳性位点来增加整个样本的敏感性。通常先采集患者肿瘤组织进行全外显子测序(WES)检测,针对每位患者选取肿瘤特异性的克隆位点进行个性化定制NGS Panel(或使用多重PCR方法),在监测时提取血浆中的ctDNA进行超高深度测序,通常在术后约四周进行MRD检测。
2.tumor-agnostic路线(固定panel)
用固定panel设计覆盖的位点虽然多,但是针对每位患者的有效监控位点数量不及tumor-informed assays方法,所以很多采用此策略的检测方法加入表观基因组学特征提高检测灵敏度。鉴于甲基化在肿瘤发生早期已有显著变异、变异位点数目丰富,这些表观基因组“标记”在不同患者之间甚至在不同癌症之间更相似,使其成为新MRD检测方法的可能(尤其是针对早期患者)。
#05
问
MRD在肺癌中的应用有哪些?
答
1. MRD超前预判早期肺癌复发轨迹
2017年引人瞩目的TRACERx研究中,通过追踪前期入组100例早期非小细胞肺癌(non⁃small cell lung cancer,NSCLC)患者术后血液标本,揭示了早期肺癌术后复发ctDNA系统进化轨迹。该研究在原发灶多点测序确定其单核苷酸变异(single nucleotide variant,SNV)克隆结构的基础上,通过个体化定制的多重聚合酶链式反应技术对其中24例早期NSCLC患者术后外周血ctDNA进行动态监测。在14例复发患者中,其中13例在影像学复发前即可在动态ctDNA中检测出至少两个SNV;而仅有1例无复发患者的血浆ctDNA检测出两个以上SNV。这一研究也很好地体现了ctDNA的复发超前预判效能,中位超前预判时间窗为70天(10~346天)。值得关注的是,动态ctDNA负荷变化也反映了辅助化疗的疗效。3例患者在术后30天内即检测ctDNA阳性,并且在辅助治疗期内,其血浆SNV负荷仍不断升高,并在术后1年内出现复发;与此相反,有1例患者,虽然术后3天、辅助化疗前ctDNA检测阳性,但辅助治疗完成后以及术后457天、667天均检测阴性,而术后688天时仍无肿瘤复发。由此提示动态血浆ctDNA检测能够超前预判肿瘤复发,同时与辅助治疗疗效具有一定相关性。
2. MRD预测巩固免疫治疗疗效
随着PACIFIC临床试验里程碑式成功,同步放化疗后免疫检查点抑制剂(immune checkpoint inhibitor,ICI)巩固治疗已成为不可手术局部晚NSCLC的标准治疗。在此基础上,Moding等进行了一项通过MRD来预测巩固疗效的探索性研究,该研究回顾性入组65例局部晚期NSCLC根治性放化疗(chemoradiation therapy,CRT)后患者,其中28例患者接受了巩固ICI,利用CAPP⁃seq技术对患者不同治疗时间点进行动态ctDNA 监测以评估其MRD状态。在疗效预测方面,在巩固ICI早期血液样本中ctDNA阳性的患者在CRT 1年内全部都发生了疾病进展,而ctDNA阴性患者87.5%免于疾病进展;更值得关注的是,研究者通过CRT后ctDNA状态以及有无接受巩固ICI进行不同组间生存分析比较,发现CRT后ctDNA阴性患者可能无法从巩固ICI治疗中获益,而CRT后ctDNA阳性患者接受ICI则明显优于未接受ICI巩固治疗患者(P=0.04)。
3. MRD干预性临床试验进展
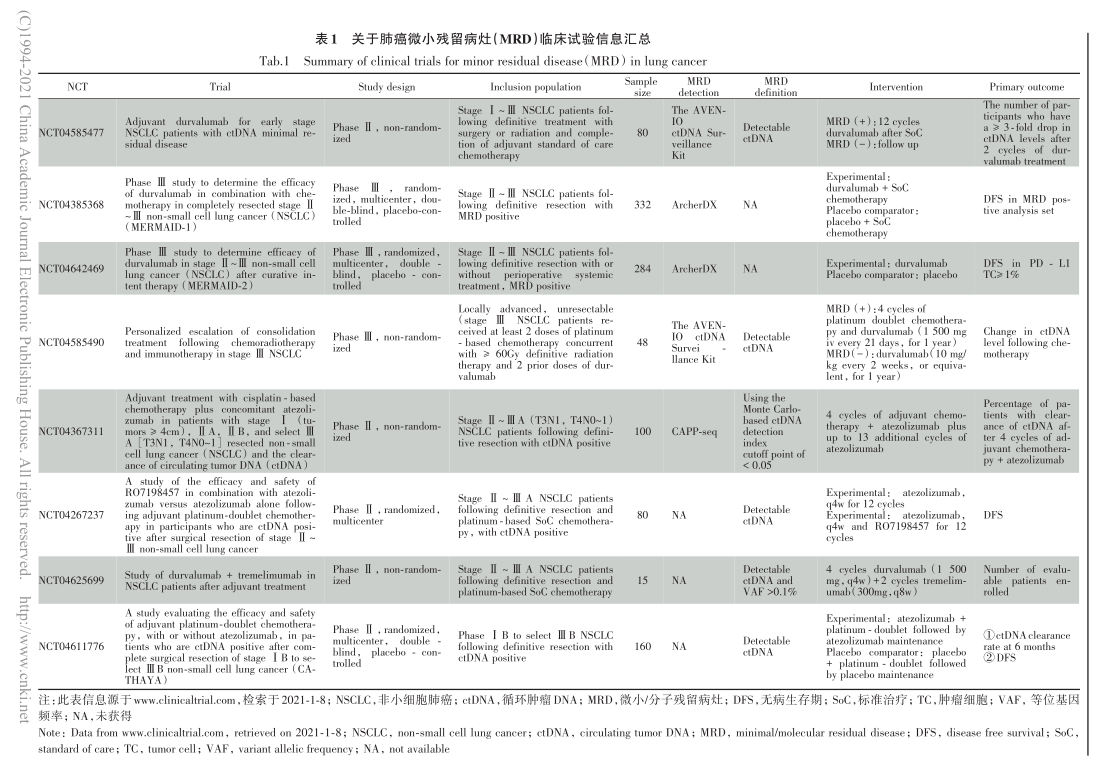
从表1所列举的临床试验信息,可以进一步总结以下几个特点:(1)目前临床试验均是通过ctDNA 检测来评估肺癌MRD状态,多采用的是多基因高通量检测模式;(2)大部分临床试验定义只要检测到ctDNA即判定为MRD阳性;(3)入组人群多为 ctDNA 阳性患者,即为根治性治疗后复发高风险人群,而随机治疗组多为较标准治疗更为积极的系统巩固治疗。因此,目前大部 分肺癌MRD临床试验突出的是MRD的阳性预测价值,其广义上代表患者体内累积的肿瘤负荷,为该患者群体中高复发风险人群;而以MRD作为治疗预测标志物的研究仍然不多。
4. MRD改写治疗新格局
随着测序技术水平进一步提高,当可以通过ctDNA检测准确评估患者体内肿瘤负荷时,我们可以科学、合理地通过MRD监测给予肺癌患者药物假期(drug holiday)。从ADAURA临床试验出发,早期表皮生长因子受体(EGFR)突变肺癌患者根治性切除术后,通过MRD监测予以指导奥希替尼用药,而非连续性用药模式,理论上是否可以延缓肿瘤 EGFR 靶向治疗耐药克隆的发展,从而延缓耐药?同时可以减轻患者治疗负担,享受一段时间的“药物假期”;从PACIFIC临床试验出发,不可手术局部晚期NSCLC患者,经过根治性放化疗后,通过 MRD 监测予以指导度伐利尤单抗维持治疗,既可以预测ICI巩固治疗获益人群,又可以减轻治疗负担,享受“药物假期”;从晚期靶向治疗患者群体出发,在患者获得完全缓解或者寡转移经局部治疗后,通过
MRD阴性情况下暂停靶向治疗的进行,让患者享受药物假期。
参考文献:
1.Minimal Residual Disease (MRD). (n.d.). Minimal Residual Disease (MRD). Leukemia & Lymphoma Society.
2.Coombes RC, Page K, Salari R, et al. Personalized Detection of Circulating Tumor DNA Antedates Breast Cancer Metastatic Recurrence. Clin Cancer Res. 2019;25(14):4255-4263. doi:10.1158/1078-0432.CCR-18-3663
3.Schuurhuis Gerrit J,Heuser Michael,Freeman Sylvie et al. Minimal/measurable residual disease in AML: a consensus document from the European LeukemiaNet MRD Working Party.[J] .Blood, 2018, 131: 1275-1291.
4.Coakley Maria,Garcia-Murillas Isaac,Turner Nicholas C,Molecular Residual Disease and Adjuvant Trial Design in Solid Tumors.[J] .Clin Cancer Res, 2019, 25: 6026-6034
5.Abbosh C, Birkbak NJ, Wilson GA, et al. Phylogenetic ctDNA analysis depicts early-stage lung cancer evolution [published correction appears in Nature. 2017 Dec 20]. Nature. 2017;545(7655):446-451. doi:10.1038/nature22364
6.Prof.Jeanne Tie, 2020.ASCO-GI
7. 吴一龙等.引领肺癌治疗新时代的标志物–微小残留病灶[J]. 循证医学,2021,02:21.
