2020年第43届美国圣安东尼奥乳腺癌研讨会(SABCS)于当地时间12月8至11日以线上会议的形式召开。SABCS是乳腺领域规模最大、最具影响力的国际性会议。其中,多项研究值得关注。今天,一嘉医课为大家总结三阴性乳腺癌、HER2阳性/阴性乳腺癌免疫治疗、分子诊断和内分泌辅助治疗等方面的重磅研究。本文较长,阅读时间大约15分钟,建议收藏学习。
III期IMpassion130试验:一项在三阴性乳腺癌中一线阿替利珠单抗和白蛋白结合型紫杉醇的基因组分析
在早先公布的IMpassion130试验结果中,与安慰剂(P)+ 白蛋白结合型紫杉醇(nP)相比,阿替利珠单抗(A)+ nP在PD-L1阳性的转移性三阴性乳腺癌(mTNBC)中显示出无进展生存(PFS)的改善和具有临床意义的总生存(OS)获益。但mTNBC基因改变的临床意义尚未明确。
研究人员通过二代测序(NGS)产品 Foundation One集中检测IMpassion130生物标志物可评价人群(BEP)中患者的原发性或转移性肿瘤样本,包括染色体结构变异(SV)、拷贝数改变(CNA)和重排。使用VENTANA SP142检测评价PD-L1状态(PD-L1阳性定义为≥1%肿瘤区域有PD-L1表达免疫细胞)。本探索性研究的目的是评价基因改变的发生率及其与PD-L1状态的关系,并确定在随机数据集中A+nP是否存在这些因素的预后或预测作用。使用Cox回归模型分析PFS和OS(共同主要终点)。
结果表明:BEP共614例患者(占意向性分析人群的68%),其中605例接受治疗。最常见的致病性改变见于以下基因:TP53 (SV, 85%)、MYC (CAN, 21%)、PIK3CA (SV, 18%)、PTEN (SV/CAN, 18%)、RB1 (SV, 7%)和BRCA1 (SV, 9%)。
与转移性肿瘤(n=195)相比,原发性肿瘤(n=419)更有可能携带BRCA1的改变(11.9% vs 5.6%),更少携带PIK3R1的改变(4.8%vs 9.2%)。PD-L1阳性状态与TP53功能缺失突变相关,而与VEGFA和CCND3基因扩增的相关性较低,这些改变都不是A+nP疗效的有利因素。
RB1缺失(频率5%)与PFS(HR:2.09,95%CI:1.42-3.07)和OS(HR:1.98,95%CI:1.26-3.11)预后降低相关,而与治疗无关和)。CDKN2A (12%)和CDKN2B (11%)中的CNA与A+nP组对比P+nP组的PFS和OS改善相关。584例微卫星BEP中有3例为MSI-H状态,与PD-L1状态无关;3例MSI-H患者均来自P+nP组。514例BEP中共有220例(42.8%)PIK3CA/AKT1/PTEN改变状态,与PD-L1状态或A+nP临床结局无显著相关性。
结论:在这项使用NGS的探索性分析中发现,初治mTNBC患者的肿瘤在基线时具有与报道中早期TNBC肿瘤相似的基因组特征。PD-L1相关的少数突变与临床结局无关。细胞周期基因(如RB1)中的CNA具有潜在的预后价值,而CDKN2A和CDKN2B可能预示A+nP的A+nP临床获益。这些数据只是产生假设,需在独立数据集进一步验证。
KEYNOTE-355:帕博利珠单抗联合化疗一线治疗,带来PFS、ORR等多方位获益
KEYNOTE-355研究显示帕博利珠单抗(P)联合化疗用于局部晚期或晚期TNBC较单独化疗有明显的PFS改善。
研究纳入847例根据RECIST v1.1有可测量病灶、ECOG PS评分 0~1、无病间期(DFI)≥6个月的局部晚期或晚期TNBC患者,按2:1随机分配接受P+化疗或安慰剂+化疗,两组均最多给药35次,或直至进展或出现无法耐受的毒性。双重主要终点为PD-L1 阳性 (CPS ≥10 和≥1)和总体人群的PFS和OS。
截至2019年12月11日,P+化疗组的中位随访时间为25.9 个月,安慰剂+化疗组的中位随访时间为26.3 个月。
结果显示,与安慰剂+化疗相比,P+化疗在改善PFS、客观缓解率(ORR)、疾病控制率(DCR)和缓解持续时间(DOR)上都有显著优势。在亚组分析中,与安慰剂+化疗相比,P+化疗改善了转移性TNBC患者的PFS,与伴随化疗方案无关。对于ORR、DCR和DOR终点,观察到P+化疗改善PD-L1高表达患者疗效的趋势。这些数据进一步支持帕博利珠单抗联合化疗作为转移性TNBC一线治疗选择的潜力。
Ipatasertib+化疗治疗PIK3CA/AKT1/PTEN异常TNBC
II期LOTUS研究得到一个大致结论:在紫杉醇中添加依帕他塞(ipatasertib)可改善晚期TNBC患者PFS,尤其是对于PIK3CA/AKT1/PTEN突变的患者。
III期IPATunity130研究纳入255例有PIK3CA/AKT1/PTEN突变、ECOG PS评分 0~1的晚期TNBC患者,2:1随机接受依帕他塞联合紫杉醇或安慰剂联合紫杉醇治疗。主要研究终点为研究者评估的PFS,次要研究终点包括OS、ORR、DOR和安全性等。
中位随访时间8.3个月,33%的患者仍在接受治疗。在两组总体人群和预先指定的任何亚组中都没有观察到PFS差异,与LOTUS II期研究结果相反。目前OS结果尚不成熟。
SWOGS9313研究:DDIR和HRD可预测TNBC对于DNA损伤药物的疗效
DNA损伤免疫反应(DDIR)、同源重组缺陷(HRD)与早期TNBC预后良好相关。通过对SWOG S9313研究中接受AC(阿霉素+环磷酰胺)辅助治疗的425例早期TNBC患者分析发现,HRD+/DDIR+患者的接受AC辅助治疗可以获得更好的DFS和OS。60%的早期TNBC患者表现为DDIR+,而且该表型患者无论HRD状态如何,接受AC辅助治疗都能显著改善生存率。
DESTINY-breast01研究:DS-8201后线治疗晚期乳腺癌,ORR超60%,PFS达19.4个月
DESTINY-breast01研究共纳入253例在T-DM1治疗中或治疗后进展的晚期乳腺癌患者,接受DS-8201治疗。本次更新的数据截止日期(2020年6月8日),与之前的数据截止日期(2019年8月1日)相比,中位随访时间从11.1个月增加至20.5个月;37例(20.1%)仍在接受治疗。
确认的ORR为61.4%(12例达到完全缓解),中位缓解持续时间为20.8个月,疾病控制率为97.3%。更新后的中位PFS为19.4个月,12个月时OS率为85%,18个月OS率为74%。初步评估的中位OS为24.6个月(估计35%的成熟度,24个月时只有17例患者处于风险状态)。
来那替尼用于早期乳腺癌术后的延长辅助治疗,8年生存结果揭晓
ExteNET是一项多中心、随机、双盲、安慰剂对照的III期研究,共纳入2840例既往接受过曲妥珠单抗+化疗作为新辅助或辅助治疗的HER2 +早期乳腺癌患者,1:1随机分配接受来那替尼或安慰剂作为延长辅助治疗,持续1年。
中位随访8.1年,来那替尼和安慰剂ITT组分别有127例(8.9%)和137例(9.6%)患者死亡。来那替尼组的8年OS率为90.1%(95%CI:88.3-91.6)和安慰剂组是90.2%(95%CI:88.4-91.7)(8年绝对差异-0.1%;分层HR=0.95,p=0.6914)。
在HR+且接受曲妥珠单抗后1年内开始使用来那替尼,以及新辅助治疗后残留病灶亚组中,来那替尼带来的OS改善更大,HR为0.79(0.55-1.13)和0.47(0.23-0.92)。
SOLAR-1研究更新:Alpelisib+氟维司群可为PIK3CA突变各亚组患者带来获益
PIK3CA突变会导致PI3K信号通路的异常激活,而导致细胞增殖、药物耐药性和不良预后。HR+/HER2-晚期乳腺癌患者中约有40%患者为PIK3CA突变。
Alpelisib是一种选择性PI3Kα抑制剂,SOLAR-1是一项随机双盲、安慰剂对照的III期研究,旨在评估Alpelisib(300mg)或安慰剂+氟维司群(500mg)用于男性和绝经后HR+/HER2-晚期女性乳腺癌的疗效和安全性。本研究通过NGS和PCR检测肿瘤组织和ctDNA中的PIK3CA突变(具体为Foundation Medicine 324基因ctDNA panel检测基线收集的血浆ctDNA的PIK3CA基因的完整外显子区域序列),并回顾性分析Alpelisib在PIK3CA突变亚组中的有效性。
研究显示,Alpelisib+氟维司群可明显改善芳香酶抑制剂治疗进展的PIK3CA突变、HR+/HER2-晚期乳腺癌患者的PFS。
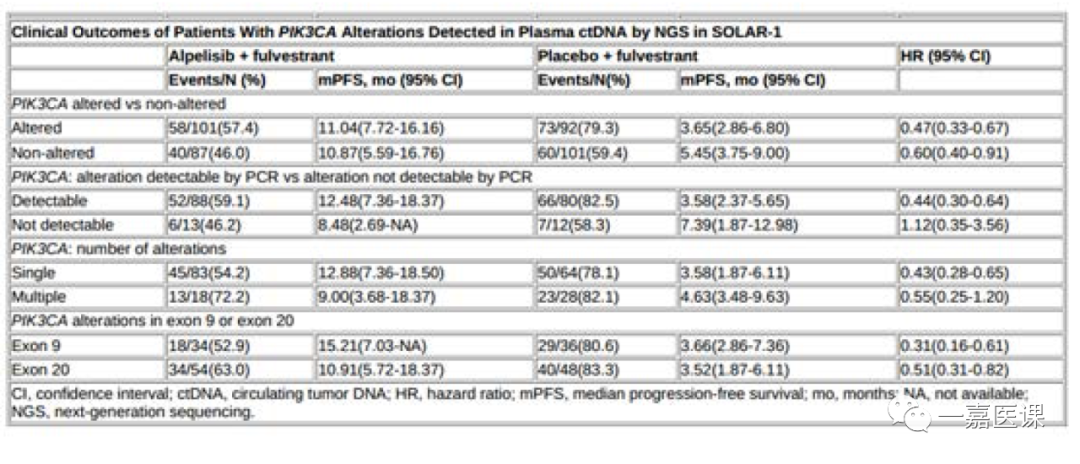
具体结果:在572例患者中,PIK3CA突变和非突变组有381例(66.6%)患者的血浆ctDNA数据可用。其中,193例(50.7%)患者为PIK3CA突变,168例(87%)患者具有PCR可检测的突变,147例(76%)患者为单突变。分别有70 例(36%)和102例(53%)患者为外显子9和20的PIK3CA突变。Alpelisib+氟维司群可延长PIK3CA突变(通过NGS检测ctDNA)患者(n=101)的PFS(表1)。在PCR检测的PIK3CA突变、单突变(n=83)、外显子9(n=34)和外显子20(n=54)突变患者中也能观察到联合治疗的临床获益。
ALTERNATE研究:探索最合适新辅助内分泌治疗模型
新辅助内分泌治疗为II/III ER+/HER2-绝经后乳腺癌患者增加了保乳手术机会。
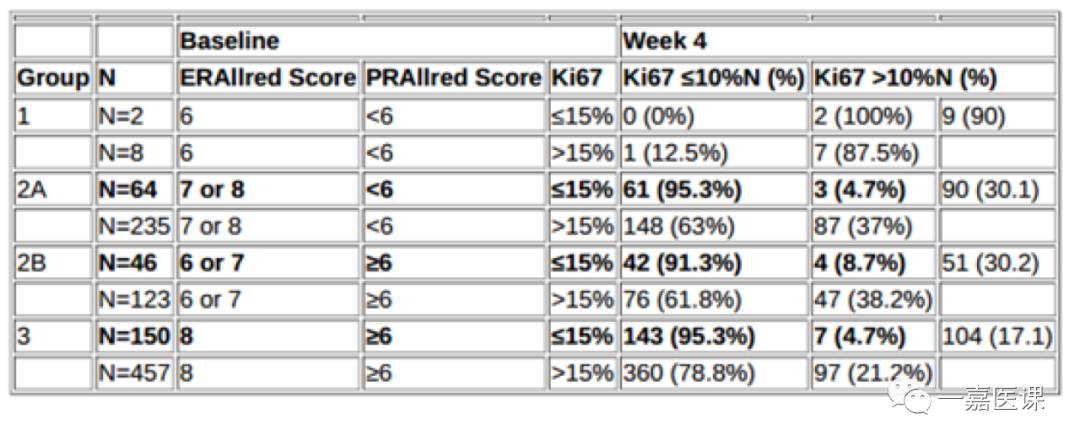
2020 SABCS报告的ALTERNATE研究,基于ER、PR和Ki67的预测模型将适合进行新辅助内分泌治疗的ER+/HER2-患者分为3组:第1组是可能不合适新辅助内分泌治疗(Allred ER <6或ER 6和PgR <6);第2组是可能适合新辅助内分泌治疗,考虑在内分泌治疗后2-4周时进行Ki67分析(基于治疗过程中,Ki67>10%与预后较差相关)(2A:ER 7或8且PgR <6;2B:ER 6或7且PgR≥6);第3组是适合新辅助内分泌治疗(ER 8且PgR≥6)。
结果发现,在随机接受6个月新辅助内分泌治疗的1085例合格患者中,第1、2和3组患者分别占1%(n = 10)、43%(n = 468)和56%(n = 607)。治疗期间Ki67> 10%使90%(9/10,1组)、30%(141/468,2组)、17%(104/607,3组)患者从新辅助内分泌治疗转为新辅助化疗或手术(表2)。在第2组和第3组的1075例患者中,260例(24%)患者基线时Ki67≤15%,其中仅14例(5.4%)患者4周时Ki67> 10%,相比之下,28.3%患者(231/815)基线时Ki67>15%,4周时Ki67>10%,其中2%患者因治疗时Ki67<10%仍接受内分泌治疗而发生疾病进展。
我们看到,ALTERNATE研究支持该模型,该模型可将诊断时的ER、PR和Ki67水平用于识别原发性绝经后ER+/HER2-乳腺癌是否适合新辅助内分泌治疗。基线ER Allred评分> 6且Ki67≤15%时,患者对内分泌治疗耐药的可能性很小;基线Ki67> 15%时,内分泌治疗的敏感性可变,治疗期间活检检测Ki67值可能有助于指导新辅助治疗,特别是当Ki67<10%时,局部疾病进展率极低。
https://www.sabcs.org/2020-SABCS/2020-SABCS-Overview

版权信息
本文由一嘉医课编辑部负责编写或约稿。如需转载,请联系jmre@jmre.org。未经授权使用文章内容及部分内容是侵权行为,版权方保留追究法律责任的权利。