第29届欧洲血液学会(EHA)年会将于2024年6月13日-16日在西班牙马德里盛大召开。EHA年会是欧洲血液学领域规模最大的国际会议,来自世界各地的专家学者齐聚一堂,分享及讨论血液领域的最新科研成果。
组蛋白去乙酰化酶抑制剂(HDACi)西达本胺作为新型抗肿瘤的表观遗传调控药物,继2014年获批用于复发难治性外周T细胞淋巴瘤(PTCL)后,其用于初治MYC及BCL2表达阳性弥漫大B细胞淋巴瘤(DLBCL)的适应症也已于2024年4月30日获得中国国家药品监督管理局(NMPA)批准,其在白血病等多种血液系统肿瘤的研究也正在如火如荼开展。本次大会将公布多项其在PTCL、DLBCL和白血病领域的应用新进展。小编特将相关内容汇总成文,以飨读者!

标题:CHIDAMIDE WITH AZACITIDINE AND CHOP TREATMENT PLUS AUTO-ASCT FOR PATIENTS WITH NEWLY DIAGNOSED PERIPHERAL T-CELL LYMPHOMA: INTERIM ANALYSIS OF A PROSPECTIVE,SINGLE CENTER,SINGLE-ARM, PHASE 2 TRIAL
AC-CHOP方案序贯自体造血干细胞移植(ASCT)在PTCL治疗中可行且安全,其中在AITL亚组的诱导治疗阶段,患者的总缓解率(ORR)达86.9%,完全缓解(CR)率达60.8%。
关键作者:刘耀
单位:重庆大学附属肿瘤医院
结果:本研究为一项正在进行的前瞻性、单中心、单臂、2期临床试验,旨在评估西达本胺+阿扎胞苷+CHOP方案(AC-CHOP)联合治疗,以及西达本胺维持治疗在新诊断PTCL患者中的疗效和安全性。从2021年3月至2023年12月,共招募了45例新诊断的PTCL患者;行每21天一个周期的AC-CHOP方案,完成4至6个周期的诱导治疗后,评估为部分缓解(PR)或CR的患者将进行ASCT,随后接受西达本胺维持治疗。
研究入组时,60%的患者为血管免疫母细胞性T细胞淋巴瘤(AITL),中位年龄为45岁。大多数患者(93.3%)处于III/IV期,62.2%的患者国际预后指数(IPI)评分为3-5。41例患者至少接受了2个周期的AC-CHOP方案治疗,中位治疗周期为5个周期。17例患者接受了ASCT,治疗后的ORR为85.3%,CR率为48.7%。ASCT后,ORR达到100%,CR率为88.2%。AITL患者的ORR为86.9%,CR率为60.8%。安全性良好,最常见3-4级血液学不良事件为中性粒细胞减少症(52.9%)和中性粒细胞减少伴发热(35.4%)。3-4级非血液学毒性包括低钾血症、恶心、呕吐、疲劳和谷丙转氨酶升高。目前尚未报告治疗相关死亡。
结论:西达本胺联合阿扎胞苷和CHOP方案诱导治疗,并序贯ASCT在PTCL治疗中是可行且安全的。特别是在AITL的诱导治疗阶段,实现了高CR率且安全可控。
标题:A RETROSPECTIVE STUDY ON THE EFFICACY AND SAFETY OF CHIDAMIDE AS MAINTENANCE THERAPY OF PERIPHERAL T-CELL LYMPHOMA(PTCL) (NCT05967949)
PTCL缓解后西达本胺维持治疗,中位PFS达33个月,中位OS未达到,预后改善明显且安全性可控。
关键作者:徐卫
单位:江苏省人民医院
结果:本研究是一项关于西达本胺作为PTCL维持治疗的疗效和安全性的回顾性研究,旨在评估西达本胺作为PTCL维持治疗的效果。从2015年1月至2022年7月,共纳入58例患者,所有患者在至少达到PR后开始西达本胺维持治疗。患者中位年龄为66岁,58.6%为III-IV期,AITL占58.6%。在一线治疗后接受西达本胺维持治疗的39例患者中,维持治疗期间,8例患者从PR达到CR。11例(28.2%)患者在维持期间出现疾病进展(PD)。在挽救治疗后接受维持治疗的19例患者中,末次随访时,8例患者评估为CR,2例为PR。9例(47.4%)患者在维持期间出现PD。所有患者中位随访时间为39个月(2-79),中位PFS为33个月,中位OS尚未达。使用西达本胺作为一线维持治疗的患者,中位PFS和OS均未达到,预后明显优于挽救治疗后使用西达本胺维持治疗的患者(中位PFS和OS分别为7个月和67个月,P<0.001,P=0.009)。最常见的毒性是血液学毒性,大多数不良事件为1或2级。
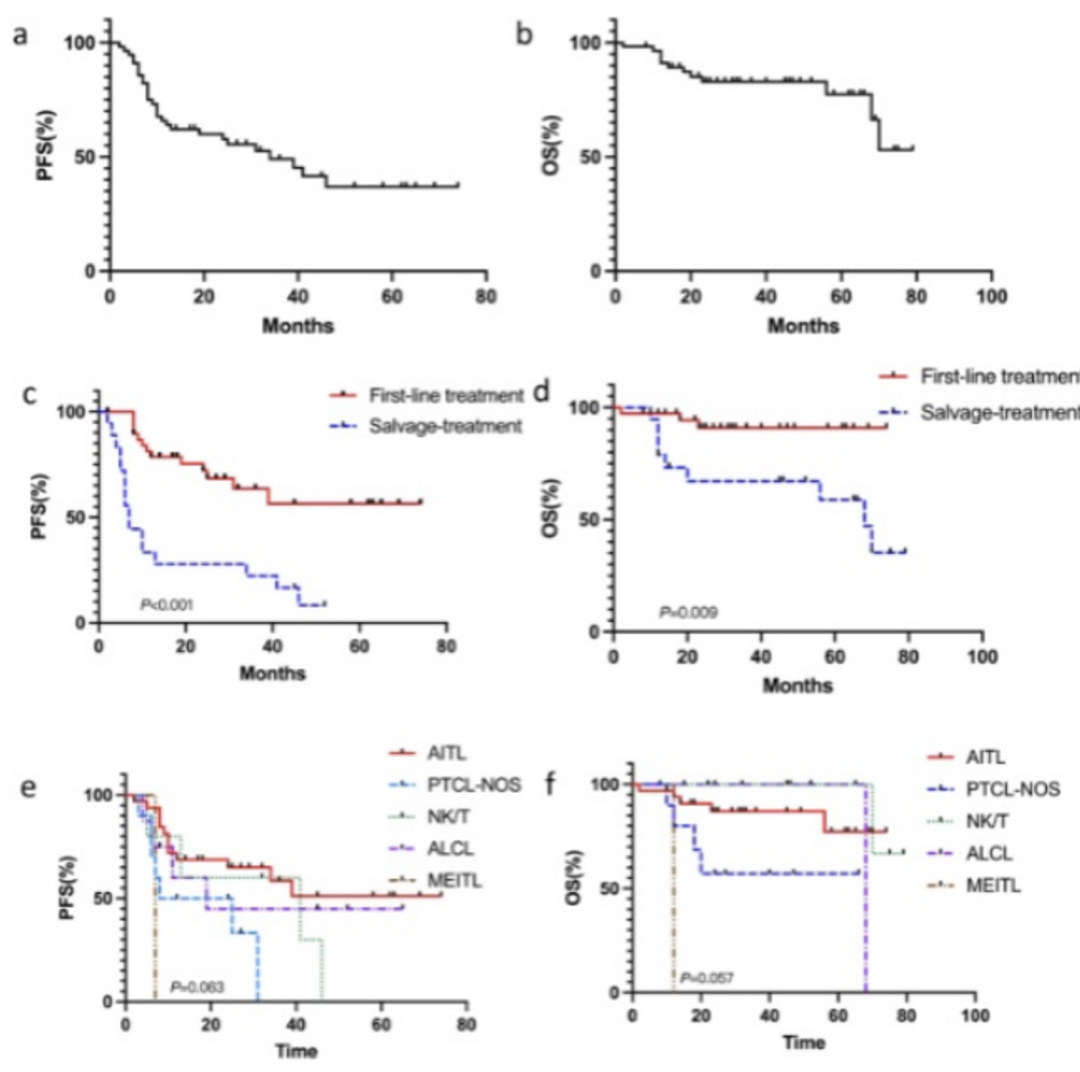
图1 58例患者的PFS(a)和OS(b);一线西达本胺维持治疗和挽救治疗西达本胺维持患者的PFS(c)和OS(d);PTCL不同亚型的PFS(e)和OS(f)
结论:西达本胺维持治疗在PTCL患者中具有较好的PFS和OS,尤其是作为一线维持治疗,安全可控。

标题:BRUTON TYROSINE KINASE INHIBITORS AND CHIDAMIDE-COMBINED THERAPY IN RELAPSED OR REFRACTORY DIFFUSE LARGE B-CELL LYMPHOMA
西达本胺联合布鲁顿酪氨酸激酶抑制剂(BTKi)治疗复发难治性DLBCL(R/R DLBCL)最佳ORR达68.42%,中位PFS可达6.5个月,且耐受性可控
关键作者:梁爱斌
单位:上海市同济医院(同济大学附属同济医院)
结果:本II期研究旨在探讨西达本胺联合BTKi治疗R/R DLBCL的疗效和安全性。研究共纳入19例患者,14例患者为非生发中心B细胞(non-GCB)DLBCL,4例为生发中心B细胞(GCB)DLBCL,1例为转化型DLBCL。10例患者发生TP53缺失/突变。中位既往治疗线数为3线(1-9),共有14例患者既往接受过BTKi治疗,6例未能完成嵌合抗原受体T细胞/NK细胞(CAR-T/CAR-NK)治疗。最佳ORR为68.42%,13例患者在治疗1-2个周期后获得客观缓解,其中5例(26.32%)获得CR,8例(42.10%)获得PR。中位随访9个月,中位PFS为6.5个月(95%CI:5.28-7.72),中位OS未达到。
在安全性方面,最常见血液学毒性为≥3级中性粒细胞减少症(26.32%)和≥3级血小板减少症(21.05%)。2例(10.53%)发生肺炎,1例(5.26%)发生带状疱疹。
结论:西达本胺联合BTKi治疗R/R DLBCL疗效良好,耐受性可控。尽管大多数患者接受BTKi治疗后出现复发和耐药,但联用西达本胺使患者重新缓解,表明西达本胺可增强BTKi的疗效并克服获得性耐药。
标题:CHIDAMIDE IN COMBINATION WITH R-CHOP FOR NEWLY DIAGNOSED B‑CELL NON-HODGKIN LYMPHOMA WITH EPIGENETIC MUTATIONS: PRELIMINARY ANALYSIS FROM THE RESULTS OF A PHASE II STUDY
西达本胺联合R-CHOP治疗伴表观遗传突变的初治B细胞非霍奇金淋巴瘤(B-NHL)患者CR率达81.8%,预估12个月PFS和OS率分别为89.5%和100%,且耐受性良好。
关键作者:景红梅
单位:北京大学第三医院
结果:本研究旨在评估西达本胺联合R-CHOP治疗初治伴表观遗传突变的B-NHL患者的疗效和安全性。研究共纳入22例患者,中位年龄49岁,59%为女性,大多为晚期患者,59%为IPI 2-5。治疗结束时,18例患者(81.8%)达到CR,2例患者(9.1%)达到PR。中位随访9.1个月,2例患者复发或进展(9.1%)。估计12个月PFS和OS率分别为89.5%(95%CI:75.5%-100%)和100%。
亚组分析显示,组蛋白甲基化突变(KMT2C/KMT2D/EZH2)患者的CR率为83.3%(15/18);组蛋白乙酰化突变(CREBBP/EP300/IRF4)患者的CR率为70%(7/10);TP53突变患者的CR率为100%(4/4)。
最常见不良事件(AE,所有等级)为中性粒细胞减少症(14%)、COVID-19感染(23%)、肺炎(9%)、腹泻(5%)和上呼吸道感染(5%)。15%的患者发生≥3级AE,主要为血液学AE,包括中性粒细胞减少症(9%)和腹泻(5%)。
结论:西达本胺联合R-CHOP方案治疗初治表观遗传突变的B-NHL患者是可行的且耐受性良好。本试验的初步疗效结果提示该联合治疗方案值得进一步探究,包括进行相关研究,来确定基于表观遗传生物标志物分析可能应答的DLBCL亚组。
标题:CHIDAMIDE IN COMBINATION WITH R-CHOP-LIKE CHEMOTHERAPY FOR PREVIOUSLY UNTREATED GERMINAL CENTER B-CELL-LIKE MYC/BCL2 DOUBLE-EXPRESSER DIFFUSE LARGE B-CELL LYMPHOMA
西达本胺联合R-CHOP治疗初治GCB亚型MYC/BCL2双表达(DE)DLBCL患者疗效可观,ORR达94.1%,较化疗组显著提高。中位PFS可达37.9个月。
关键作者:李文瑜
单位:广东省人民医院
结果:本回顾性研究旨在评价西达本胺联合R-CHOP方案与单用R-CHOP方案治疗初治GCB DE-DLBCL患者的临床疗效和安全性。研究共纳入42例患者,中位年龄59岁,64.3%为晚期。西达本胺联合治疗组CR/未证实的完全缓解(CRu)率为76.47%;PR率为17.65%,PD率为5.9%。化疗组CR/Cru率为52%,PR率为12%,PD率为36%。西达本胺联合治疗组与化疗组的ORR具有显著统计学差异,分别为94.1%和74%(p=0.03),但两组间的CR/CRu率未达到统计学差异,分别为76.5%和52%(p=0.109)。
中位随访56.8个月,西达本胺联合治疗组和化疗组的3年PFS率为58.8%和39.0%(p=0.303),3年OS率为81.9%和62.0%(p=0.176),中位PFS为37.9个月和19.3个月。CR/CRu率、PFS率和OS率无统计学显著差异,但西达本胺联合治疗组CR率,3年PFS率和OS率数值上明显改善。研究结果表明西达本胺联合治疗改善了GCB DE-DLBCL患者的临床疗效。
结论:在这项单中心回顾性研究中,西达本胺联合R-CHOP方案显示出有前景的疗效结果,提示GCB DE-DLBCL患者的长期生存结局有改善趋势。这一治疗方案需要通过大规模研究进一步验证。
标题:CHIDAMIDE ENHANCES T-CELL-MEDIATED ANTI-TUMOR IMMUNE FUNCTION BY INHIBITING NOTCH1/NFATC1 SIGNALING PATHWAY IN ABCTYPE DIFFUSE LARGE B-CELL LYMPHOMA
西达本胺通过靶向NOTCH1和NFATC1信号通路,改善异常的DLBCL微环境,防止免疫逃逸,从而有效抑制DLBCL细胞系的细胞活性。
关键作者:李莉
单位:大连医科大学附属第二医院
结果:本研究使用患者源性ABC型DLBCL细胞系(OCI-LY3、OCI-LY10和HBL-1细胞)、BALB/c裸鼠中患者源性DLBCL细胞系异种移植模型和A20淋巴瘤模型作为实验对象。研究结果显示,西达本胺通过抑制HDAC蛋白表达,上调组蛋白乙酰化,显著抑制ABC型DLBCL细胞系增殖。在线粒体凋亡途径中发挥促进细胞凋亡的作用;此外,干扰NOTCH1表达后,DLBCL细胞中NFATC1的表达明显下调,DLBCL细胞的生长活性受到明显抑制,提示NOTCH1和NFATC1共同维持肿瘤活性。西达本胺可以通过抑制NOTCH1和NFATC1通路,调节相关信号通路抑制肿瘤增殖。西达本胺能有效抑制小鼠肿瘤的生长,下调肿瘤组织细胞NOTCH1蛋白表达。西达本胺治疗组小鼠血清IFN-γ、IL-2和TNF-α水平显著升高,小鼠脾脏和肿瘤组织中CD4+或CD8+T细胞比例显著升高,CD4+或CD8+T细胞上PD1和TIM3表达下调。这些结果表明,西达本胺能增强小鼠肿瘤微环境中效应T细胞的增殖和功能,恢复机体耗竭T细胞的免疫功能,减轻T细胞功能障碍,显著抑制肿瘤生长。
结论:研究结果表明,西达本胺通过靶向NOTCH1和NFATC1信号通路,改善异常的DLBCL微环境,防止免疫逃逸,从而有效抑制DLBCL细胞系的细胞活性。本研究为探索恶性淋巴瘤患者个体化精准治疗提供了新的治疗思路。

标题:SELINEXOR AND CHIDAMIDE TREATMENT IN PATIENTS WITH RELAPSED/REFRACTORY ACUTE MYELOID LEUKEMIA EXPOSED TO VENETOCLAX: A SINGLE-ARM, PHASE 2 STUDY
西达本胺联合塞利尼索作为复发/难治性急性髓系白血病(R/R AML)患者的挽救治疗方案,使得45.5%患者达到复合完全缓解(CRc),18.2%患者获得部分缓解(PR),客观缓解率ORR高达63.6%,且安全性良好。
关键作者:仇惠英
单位:苏州大学附属第一医院
结果:2022年12月至2024年2月,共11例R/R AML患者入组,接受西达本胺联合塞利尼索治疗,其中9例患者于治疗之后接受造血干细胞移植。患者中位年龄为40岁(22-54岁)。所有患者既往接受维奈克拉或去甲基化药物(HMA)治疗,且8例患者(72.7%)患者既往接受过三种以上治疗方案。10例患者(90.9%)接受初始剂量为40mg每周2次的塞利尼索治疗;1例患者(9.1%)接受初始剂量为60mg的塞利尼索治疗。所有患者均接受每日10mg西达本胺治疗。结果显示,5例患者(45.5%)达到了CRc,包括3例CR和2例完全缓解伴血液学不完全恢复(CRi),2例患者(18.2%)获得PR;ORR为63.6%;中位随访时间为11.4个月(1.9-13.8个月),中位无事件生存期(EFS)为3.3个月。达到CRc/PR的7例患者均在缓解后进行了移植。截至2024年2月,4例患者仍然存活。在该研究中,未观察到剂量限制性毒性。
结论:在该研究中,将西达本胺联合塞利尼索作为R/R AML患者的挽救治疗方案,获得较高的缓解率,且展现出良好的安全性,或将为患者提供一种潜在的桥接移植途径。仍需要更大样本量和更长随访时间的研究,以进一步验证其疗效。
标题:SYNERGISTIC EFFECT OF CHIDAMIDE AND VENETOCLAX IN IKZF1 DELETION ACUTE B LYMPHOBLASTIC LEUKEMIA CELLS AND ITS MECHANISM
西达本胺联合维奈克拉在IKZF1基因缺失急性B淋巴细胞白血病细胞(B-ALL)中表现出显著的协同作用。
关键作者:周红升
单位:南方医科大学南方医院
结果:与IKZF1wtB-ALL相比,IKZF1delB-ALL细胞系和原发性患者样本对维奈克拉表现出耐药性。然而,当维奈克拉与西达本胺联合使用时,观察到显著的协同效应。西达本胺不仅显著增强了维奈克拉的促凋亡作用,还降低了线粒体膜电位(MMP)效应。在两个IKZF1delB-ALL细胞系MHH-CALL-4和MUTZ-5中,维奈克拉单独处理时会上调Mcl-1表达,而西达本胺则下调Mcl-1表达。当两者联合处理时,Mcl-1表达会进一步下调,同时Bcl-2和Bcl-xl的表达也在联合治疗后下调。此外,西达本胺联合维奈克拉治疗还促进BIM的上调和DNA双链断裂标记物γ-H2AX的增加。在糖代谢酶方面,维奈克拉与西达本胺联用会促使PKM2、PFKM和GLUT1的表达下调。
结论:该研究揭示了西达本胺联合维奈克拉治疗IKZF1delB-ALL的协同作用,或为IKZF1delB-ALL患者临床前试验带来新的启示。
标题:ABC-14 REGIMEN (AZACITIDINE, VENETOCLAX AND CHIDAMIDE) IS COMPARABLE TO “3+7” REGIMEN IN DE NOVO AML: A REAL-WORLD EXPERIENCE FROM ABC-14 COLLABORATION GROUP
真实世界研究显示,初治急性髓系白血病(AML)患者,接受西达本胺联合阿扎胞苷和维奈克拉(ABC-14)方案治疗后,CRc率达到77.4%,且60%的患者实现微小残留病(MRD)转阴。
关键作者:翁建宇教授 & 华南ABC-14协作组专家
单位:广东省人民医院,华南ABC-14协作组
结果:本多中心回顾性研究中,53例患者接受ABC-14(阿扎胞苷、维奈克拉和西达本胺)方案,81例患者接受“3+7”方案。与接受“3+7”强化化疗(IC)方案的患者相比,ABC-14组中老年患者和不良风险患者比例较高(表1、图1)。ABC-14治疗一个周期后,AML患者CRc率为77.4%,60%患者达到MRD阴性。根据2022欧洲白血病网(ELN)分层,良好、中等和不良风险患者的CRc率分别为71.4%、70.6%和82.1%。ABC-14组与IC组的CRc率(77.4% VS 66.7%,P=0.183)无统计学差异。ABC-14组的ORR(CRc+PR)显著较高(92.5% VS 75.3%,P=0.012)。M4/M5无统计学差异(73.9% VS 76.2%,P=0.838)。此外,ABC-14组的血小板恢复时间显著短于IC组(10.86±14.73 vs 20.87±9.83,P=0.002)。
结论:该研究初步表明,对于初治AML患者,ABC-14方案的疗效与传统的“3+7”方案相当,甚至ABC-14方案的耐受性更佳,未来将进一步深入探索。
表1 接受ABC-14或IC患者的基线特征和缓解率
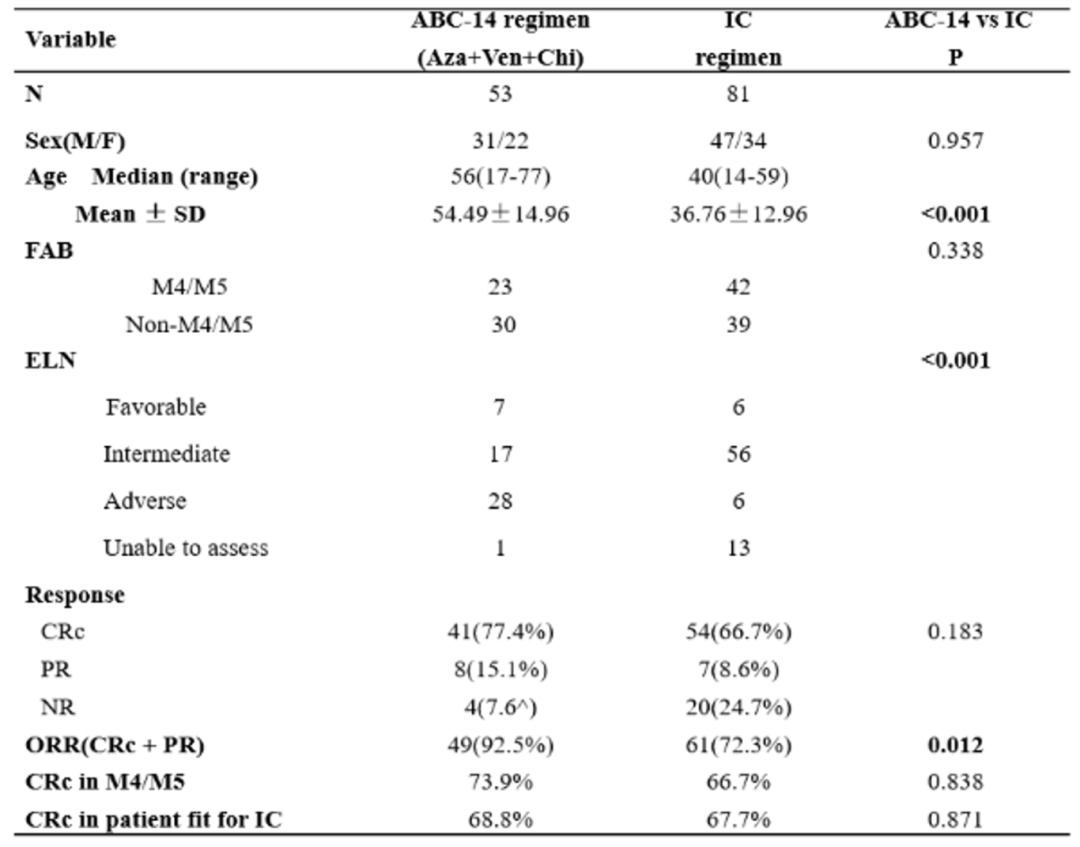
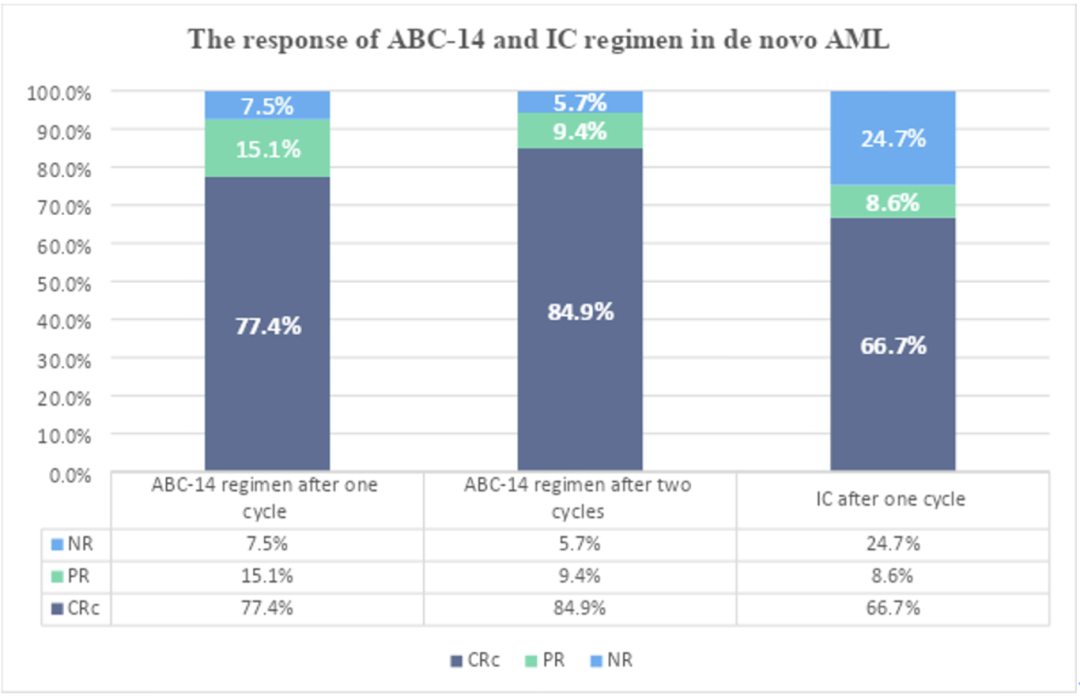
图2 初治AML中ABC-14和IC方案的缓解率
