
近日,据外媒披露,FDA公布了2024财年的《处方药使用者付费法案》(Prescription Drug User Fee Act,PDUFA)费用计划。具体内容为,2024财年,对于需要临床数据的新药申请,药企需向FDA支付超400万美元,较2023年的320万美元同比增长约25%。费用之高昂,是有史以来的第一次。
对于不需要临床数据的新药申请,费用也将从2023财年的160万美元涨到约200万美元。
PDUFA由美国国会于1992年制定,授权FDA向药品开发商收取费用,从而加快药物上市申请的审评审批。FDA会对每一项申请设置一个审批截止日期,即PDUFA date,在此时间之前FDA必须对申报药品做出审评决定——批准、不批准、补充资料后再考虑是否批准。
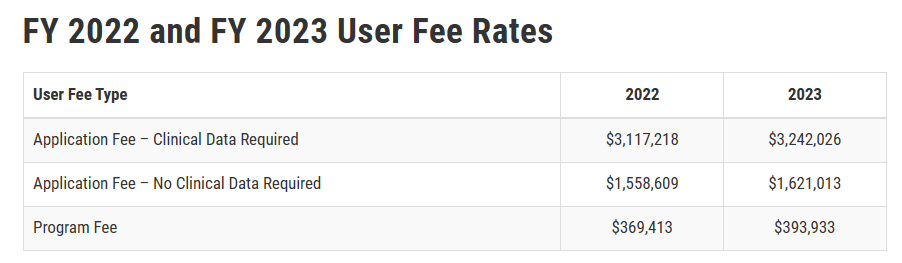
数据显示,FDA对需要临床数据的新药申请费用已在近6年上涨了120万美元,从2017年的200万美元左右增加到2023年的320万美元。
来源:医药魔方
责编:Adam