
外周T细胞淋巴瘤(PTCL)是一组异质性强的侵袭性恶性肿瘤,传统化疗预后不佳,特别是复发难治性(R/R)患者。异常的表观遗传修饰是PTCL最常见的遗传改变类型之一,其中DNA甲基化和组蛋白修饰最为突出,这凸显了表观遗传药物的治疗潜力。近日,发表于Cell子刊的一项多中心Ⅱ期临床试验1,揭示了通过结合表观遗传修饰药物来优化联合疗法可有效治疗PTCL。值此之际,医脉通特邀本文作者江苏省人民医院范磊教授和安徽省肿瘤医院丁凯阳教授解读该项研究,共探表观遗传学药物西达本胺联合阿扎胞苷±GemOx方案治疗R/R PTCL患者的疗效。

范磊 教授:
大多数R/R PTCL患者预后较差,生存期较短,文献报道首次复发或进展后患者接受挽救化疗的中位总生存期(OS)和中位无进展生存期(PFS)仅为5.5个月和3.1个月2。尽管挽救化疗后以自体或异基因造血干细胞移植(HSCT)作为巩固治疗仍是R/R PTCL可能改善预后的治疗选择,但大多数R/R PTCL患者情况较差,不能满足移植条件3。近20年来,已有普拉曲沙、组蛋白去乙酰化酶抑制剂(HDACi)和维布妥昔单抗(BV)等多个药物在国内外获批用于治疗R/R PTCL,但单药总体有效率仍有限,尚待进一步研究药物组合及新药与传统化疗方案的联用,以提高疗效。其中HDACi仍然是R/R PTCL 的重要且有效的治疗药物,以HDACi为基础的联合治疗策略是目前重要的临床探索方向。此外,随着双特异性抗体、新型抗体靶点和CAR-T细胞疗法出现在PTCL的治疗领域和临床探索,有望推动PTCL的免疫疗法发展。随着对PTCL分子亚型和发生机制的认识不断深入,表观遗传修饰药物、小分子抑制剂以及新型生物制剂/免疫治疗正在成为新兴的研究方向,探索用于治疗 R/R PTCL,为患者提供更适合的治疗选择,最终提高疗效,延长生存。
医脉通:近年来,表观遗传学药物作为一种新兴的治疗手段,在多种肿瘤治疗中显示出潜力。这类药物通过调控DNA甲基化、组蛋白修饰等影响基因表达和功能,以达到抗肿瘤效果。然而,关于表观遗传学药物在PTCL患者中的具体作用机制仍需进一步探讨。请您简要介绍您的团队基于临床实践进行表观遗传学药物研究中的创新探索与进展?

范磊 教授:
近年来,表观遗传失调在PTCL发生和发展中的作用引起广泛关注,其中DNA甲基化和组蛋白修饰最为突出。目前已有的表观遗传学调控药物包括DNMTi(如阿扎胞苷、地西他滨)、HDACi(如西达本胺)等。DNMTi通过抑制DNA甲基转移酶活性,减少DNA甲基化,从而恢复基因的正常表达;HDACi可选择性地抑制组蛋白去乙酰化酶(HDAC),以增加组蛋白乙酰化,恢复基因表达。
PTCL的临床前模型表明,DNMTi和HDACi的组合通过靶向更大比例的基因可以协同改善治疗效果。一项Ⅰ期临床研究表明,阿扎胞苷和罗米地辛联合方案具有显著的谱系选择性活性,该联合方案在R/R PTCL中总缓解率(ORR)为73%,显著高于非PTCL患者。除了HDACi联合DNMTi方案外,研究人员还在积极探索将HDACi与其他既定治疗药物相结合的方案。既往研究报道,HDACi已显示出在体外增强含铂药物抗肿瘤活性的能力,可能与HDACi改变基因表达模式增敏化疗有关。此外,HDACi诱导染色质开放还可能促进化疗药物更多的结合位点和靶向耐药细胞亚群,从而克服化疗耐药性。一项真实世界研究发现,在R/R PTCL的治疗中,西达本胺与化疗的联合较单药治疗具有更好的治疗效果。传统的化疗方案 GemOx(吉西他滨、奥沙利铂)因其良好的治疗效果和安全性得到认可,在PTCL的治疗中越来越多地与靶向药物联合使用。基于此,我们研究团队启动了一项多中心Ⅱ期临床试验,以评估基于HDACi和DNMTi的双表观遗传疗法联合或不联合GemOx方案治疗R/R PTCL患者的疗效及安全性。

本研究是一项前瞻性Ⅱ期多中心临床试验,旨在评估西达本胺联合阿扎胞苷±GemOx在治疗R/R PTCL的疗效和安全性。共纳入30例患者,中位年龄为59岁,其中19例(63.3%)患者为AITL,4例(13.3%)为PTCL-非特指型(PTCL-NOS),25例(83.3%)为难治性,12例(40%)既往治疗≥2线。所有患者均接受最多8个周期的西达本胺+阿扎胞苷±GemOx诱导治疗(每21天为1周期),其中11例患者因身体状况不佳或既往接受GemOx治疗后疾病进展而未联合化疗;9例患者完成诱导治疗后继续接受每2月一次的西达本胺+阿扎胞苷方案的维持治疗,直到疾病进展(PD)或患者无法耐受。本研究主要终点是ORR、完全缓解(CR)率、中位PFS和中位OS。

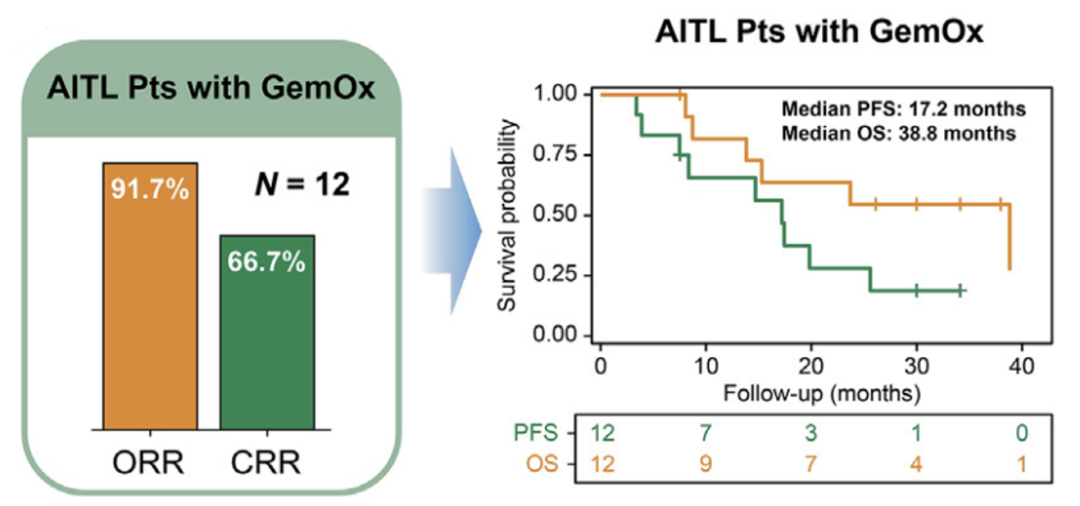
图1 西达本胺+阿扎胞苷±GemOx方案治疗AITL患者的ORR及CR率

HDACi和DNMTi联合可协同靶向DNA高甲基化和组蛋白去乙酰化导致的基因表达抑制和染色质紧缩,发挥显著的抗淋巴瘤作用。体外实验还支持HDACi与传统细胞毒性药物具有协同作用的观点。本研究结果显示,西达本胺联合阿扎胞苷和GemOx方案治疗R/R PTCL患者观察到较高的缓解率以及PFS和OS改善,在AITL患者中结果尤为理想。需要强调的是,本研究纳入难治性患者比例为83.3%,此类患者通常对化疗和HSCT没有反应,表明双表观遗传疗法联合GemOx方案可能更有效地减轻肿瘤负荷和克服耐药性。此外,在本研究中,采用了西达本胺联合阿扎胞苷作为维持治疗策略,使得患者可在较长一段时间内持续进行表观遗传调控,并在缓解患者中观察到持久的缓解,中位DoR达14.2个月。研究结果初步表明,双表观遗传药物与化疗联合可能会提供显著的治疗优势,为R/R PTCL患者提供更有效的治疗选择。

范磊 教授:
本项临床试验使用双表观药物联合化疗治疗大多为难治性的R/R PTCL取得了积极结果,提示此联合治疗策略可能更有效减轻PTCL肿瘤负荷和克服耐药性。目前PTCL一线治疗方案通常采用CHOP或CHOP样方案,然而此方案的治疗效果有限,约70%的PTCL患者在一线治疗后出现复发或难治性疾病。因此,探索预防和克服PTCL治疗耐药性的潜在策略是一项困难且尚未解决的医学挑战。随着对表观遗传复杂性的理解和不断深入,研究发现表观遗传调控因子突变对淋巴瘤的发展和药物敏感性具有整体影响,并且通过调控大量基因能够同时沉默多个基因,从而导致多基因耐药性。一项西达本胺联合诱导化疗序贯西达本胺维持治疗初治PTCL的meta分析结果显示,西达本胺联合诱导化疗的合并ORR和CR率分别为83.7%和59.7%,合并2年PFS和OS率分别为60.9%和85.6%,相较单纯化疗明显提高,显示出其减少或延缓复发、实现长期生存的作用4。此外,一项Ⅱ期研究初步结果显示,采用西达本胺联合阿扎胞苷和CHOP方案序贯ASCT治疗初诊PTCL,移植后ORR为100%,CR率为88.2%5。因此,双表观遗传药物联合化疗的治疗策略有望为PTCL一线治疗患者带来预后改善,未来有必要对双表观遗传药物联合化疗方案进行更大规模、前瞻性研究,并在优化联合疗法的组合、剂量和给药顺序,为PTCL患者预后改善提供更强有力的证据。


范磊 教授
-
江苏省人民医院血液科主任
-
医学博士、主任医师、教授
-
中国抗癌协会第一届青年常务理事
-
中国抗癌协会血液肿瘤专业委员会常务委员
-
中华医学会血液分会第十一届青年委员
-
中国免疫学会血液免疫分会委员
-
江苏省抗癌协会淋巴瘤专委会副主委
-
美国纽约哥伦比亚和康奈尔大学附属纽约长老会医院博士后
-
研究方向为淋巴肿瘤的精确诊疗


丁凯阳 教授
-
博士,主任医师,副教授,硕导
-
中科大附一院西区血液肿瘤科主任
-
中科大附一院血液科淋巴瘤/骨髓瘤亚专科主任
-
中华医学会血液学分会淋巴细胞疾病学组委员
-
中国抗癌协会淋巴瘤专业委员会委员
-
CSCO抗淋巴瘤联盟委员
-
中国抗癌协会血液肿瘤专委会淋巴瘤学组委员
-
中国老年医学学会血液学分会淋巴瘤委员会委员
-
安徽省血液学分会候任主委
-
安徽省医师协会血液学分会常委
-
安徽省淋巴瘤专科联盟理事长
-
安徽省抗癌协会血液肿瘤学分会副主任委员
-
安徽省抗癌协会血液病转化医学专委会主任委员
-
获省级科技进步二等奖2项
-
专长:淋巴瘤/骨髓瘤诊治,白血病及出凝血疾病诊治。
参考文献
1 Ding K, et al. Med. 2024 Jul 25:S2666-6340(24)00289-7.
2 Mak V, et al. J Clin Oncol. 2013 Jun 1;31(16):1970-6.
3 Chang EWY, et al. J Hematol Oncol. 2024 Jun 1;17(1):38.
4 Ma J, et al. 2024 Annual T-cell Lymphoma Forum.
5 Xiao CY, Liu Y, et al. 2024 EHA abstract: P2106.






